Clear Sky Science · nl
Tumor-intrinsieke kenmerken bepalen T-celdifferentiatie van precursor naar symptomatische multipel myeloom
Waarom dit onderzoek belangrijk is
Multipel myeloom is een bloedkanker die ontstaat in het beenmerg en bijna altijd voorafgegaan wordt door rustigere, vroege toestanden die wel of niet uitmonden in een volwaardige ziekte. Veel mensen leven jaren met deze precursoren zonder te weten of en wanneer ze zullen voortschrijden. Deze studie stelt een actuele vraag: kunnen we de “stemming” en geschiedenis van het immuunsysteem—vooral van T-cellen—aflezen om te begrijpen hoe myeloom zich ontwikkelt, hoe het op behandeling reageert en wie het grootste risico loopt op progressie?
De verkenners van het lichaam tegen kanker
T-cellen zijn veelzijdige immuuncellen die abnormale cellen, waaronder kankercellen, kunnen herkennen en vernietigen. In solide tumoren zoals long- of huidkanker kan aanhoudende stimulatie T-cellen in een uitgeputte toestand duwen waarin ze ineffectief worden, een verandering die moderne immuuntherapieën proberen om te keren. De auteurs stelden een enorme single-cell kaart samen van meer dan een miljoen cellen uit het beenmerg en bloed van mensen met multipel myeloom, de voorstadia (MGUS en smoldering myeloom) en niet-kanker controlepersonen. Door zowel genactiviteit als de unieke receptorsequenties die elke T-cellenklon definiëren uit te lezen, reconstrueerden ze hoe T-cellen georganiseerd zijn, hoe “oud” of “ervaren” ze lijken, en hoe nauwgezet ze het onderliggende tumorproces volgen.
Niet moe, maar voortijdig verouderd
Tegenovergesteld aan wat bij veel solide kankers wordt gezien, vonden de onderzoekers dat T-cellen bij myeloom zelden echt uitgeput zijn. Cellen met klassieke uitputtingskenmerken waren grotendeels beperkt tot één ongebruikelijke patiënt. In plaats daarvan verschilden beenmerg-T-cellen bij smoldering en symptomatisch myeloom van naïeve, vroege stadia naar zeer ervaren “terminaal geheugen”-typen die lijken op T-cellen bij oudere individuen. Dit patroon—genoemd T-celvervorming—liep parallel aan de natuurlijke veroudering van het immuunsysteem maar leek bij patiënten versterkt, alsof hun T-cellen sneller verouderd waren dan de rest van hen. Hoe geavanceerder de ziekte en hoe hoger de tumorbelasting, des te sterker deze verschuiving naar laatstadium geheugen-cellen, en vergelijkbare veranderingen waren ook zichtbaar in het bloed.
Aanwijzingen uit T-celvingersporen
Elke T-cel draagt een unieke receptor, en cellen die dezelfde receptorsequentie delen horen bij een kloon die is uitgebreid in reactie op een trigger. Door deze receptoren te volgen toonden de onderzoekers aan dat myeloom-beenmergen veel uitgebreide T-cellenklonen bevatten met kenmerken van krachtige doder-cellen. Deze klonen herkenden niet voornamelijk veelvoorkomende virussen. In plaats daarvan droegen ze een distinctief “niet-viraal” genhandtekening gekoppeld aan sterke cytotoxische mechanismen en waren ze verrijkt bij mensen met myeloom vergeleken met de precursorstadia. Tumoren die beter in staat waren eiwitfragmenten op hun oppervlak te tonen—via hogere activiteit van antigen-presentatiegenen—hadden vaker deze niet-virale, sterk gedifferentieerde T-cellen. Patiënten waarvan de tumoren deze sterkere immuunbetrokkenheid toonden hadden over het algemeen een betere overleving, wat doet vermoeden dat deze T-cellen ten minste deels echt antitumoraal zijn.
Behandeling, terugkeer en vroege waarschuwingssignalen
De studie volgde ook patiënten die een autologe stamceltransplantatie ondergingen, een veelgebruikte intensieve therapie. Na transplantatie werd het repertoire van T-celreceptoren meer gedomineerd door enkele grote klonen. Veel van deze uitbreidende klonen waren herleidbaar tot terminàal gedifferentieerde CD8-T-cellen die al vóór de behandeling aanwezig waren en dezelfde niet-virale, myeloom-geassocieerde signatuur droegen. Patiënten die na transplantatie nog residuele kanker hadden, hadden doorgaans bijzonder klonale, scheefgetrokken T-celrepertoires, wat suggereert dat een krachtige maar verouderingsachtige T-celrespons mogelijk niet in staat is de ziekte volledig te elimineren. Bij eerder onderzoek in het ziekteverloop vonden de auteurs dat smoldering-patiënten die later tot actief myeloom vorderden vaak een daling hadden van regulerende CD4-T-cellen—cellen die normaal helpen immuunreacties en de beenmergomgeving in balans te houden. Lage niveaus van deze cellen voorzagen in snellere progressie, onafhankelijk van bestaande klinische risicoscores.
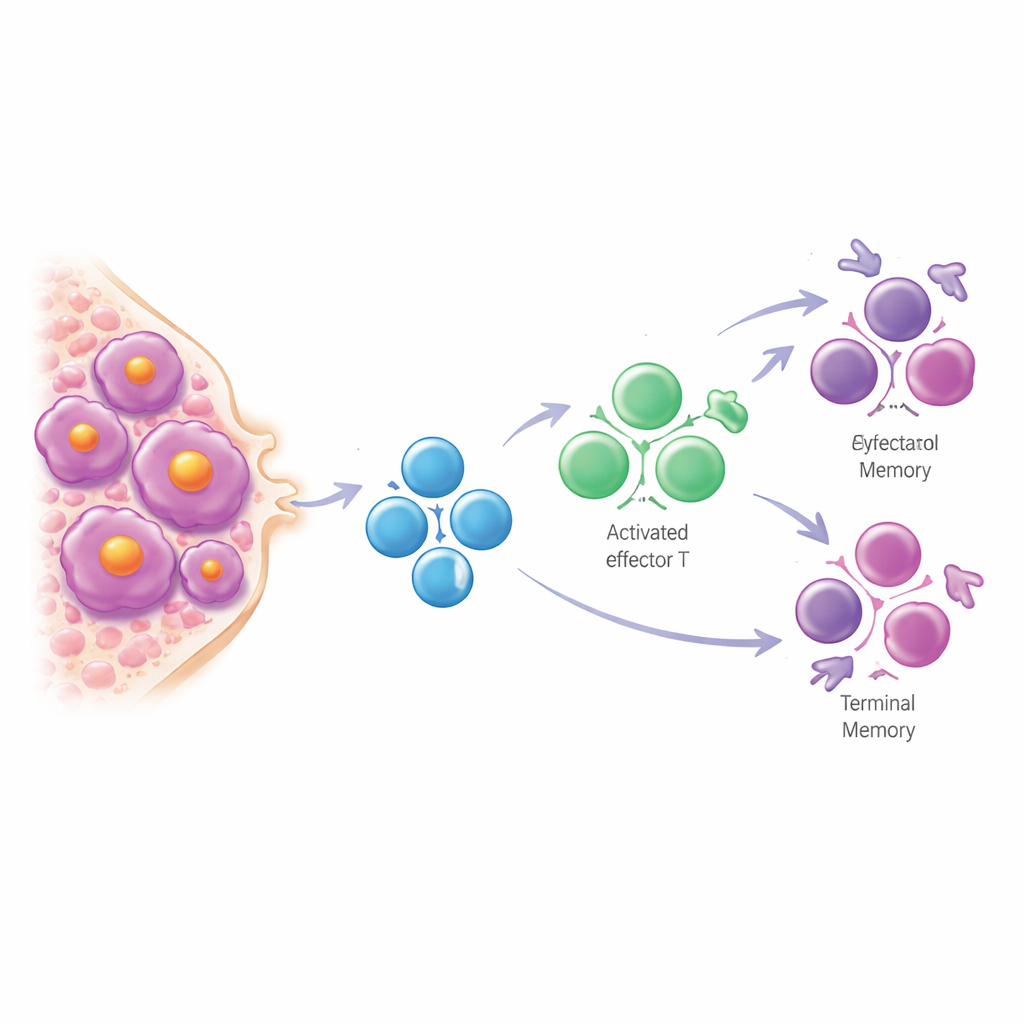
Wat dit betekent voor patiënten
Voor mensen die leven met myeloom en de precursorstadia herplaatst dit werk hoe het immuunsysteem op de kanker reageert. In plaats van simpelweg uitgeput te raken, lijken T-cellen bij myeloom chronisch geduwd te worden naar een laat, verouderd stadium door voortdurende confrontaties met tumoren. Dit scheve, klonale T-cellandschap weerspiegelt de tumorbelasting, bepaalt de reactie op behandelingen zoals transplantatie en T-cel-activerende geneesmiddelen, en kan, in het geval van verlies van regulerende T-cellen, zelfs personen aanwijzen met een verhoogd risico op progressie van smoldering naar symptomatische ziekte. Op de lange termijn kunnen deze inzichten leiden tot nieuwe immuuntherapieën die T-cellen vernieuwen of heroriënteren, en clínici helpen immuunkenmerken naast traditionele markers te gebruiken om monitoring en vroege interventie preciezer te timen.
Bronvermelding: Foster, K.A., Rees, E., Ainley, L. et al. Tumour-intrinsic features shape T cell differentiation through precursor to symptomatic multiple myeloma. Nat Commun 17, 2400 (2026). https://doi.org/10.1038/s41467-026-68718-4
Trefwoorden: multipel myeloom, T-cellen, immunologisch verouderen, single-cell sequencing, kankerimmunologie