Clear Sky Science · nl
Click-gebaseerde bepaling van accumulatie van moleculen in Escherichia coli
Waarom kleine geneesmiddelen moeite hebben gevaarlijke bacteriën te bereiken
De moderne geneeskunde is afhankelijk van antibiotica, maar sommige van de gevaarlijkste bacteriën worden nu beschermd door stevige buitenwanden die veel geneesmiddelen buiten houden. Gram‑negatieve bacteriën zoals Escherichia coli hebben een bijzonder effectieve buitenmembraanbarrière, wat het moeilijk maakt medicijnen te ontwerpen die daadwerkelijk binnendringen en hun doelen bereiken. Dit artikel introduceert een nieuwe laboratoriumtest, de CHAMP‑assay, waarmee wetenschappers snel kunnen meten hoe goed duizenden verschillende kleine moleculen deze verdedigingslinies passeren en zich ophopen in levende E. coli‑cellen.
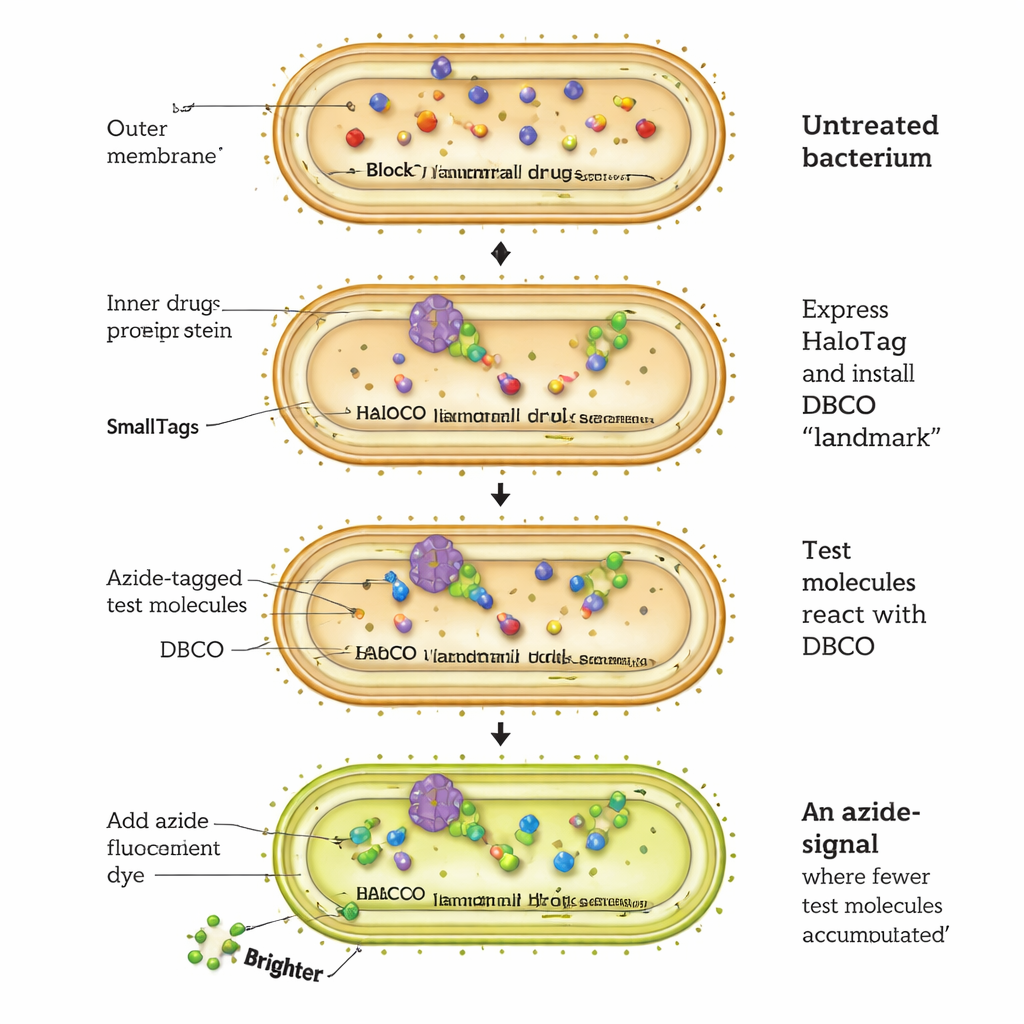
Een nieuwe manier om te zien hoe geneesmiddelen bacteriële cellen binnendringen
Traditionele antibioticaontdekking berustte op natuurlijk voorkomende verbindingen en eenvoudige groeiproeven om te zien of bacteriën leefden of stierven. Die tests tonen niet hoeveel van het geneesmiddel daadwerkelijk de cel binnenkwam, of waar het zich binnenin bevond. De auteurs gingen op zoek naar een directe, breed toepasbare methode om de toegang van geneesmiddelen tot het bacteriële cytosol te volgen — het vloeibare binnenste waar veel antibioticadoelen zitten. Hun doel was verder te gaan dan ruwe meetwaarden zoals de minimale remmende concentratie, die opname, doelbinding en downstream biologie door elkaar halen, en in plaats daarvan een zuivere meting van intracellulaire accumulatie te verkrijgen.
Bacteriën omvormen tot kleine chemische registreerders
De CHAMP‑assay werkt door een bacterieel eiwit genaamd HaloTag om te bouwen tot een soort moleculair landingsplatform. E. coli‑cellen worden genetisch aangepast om HaloTag in hun cytosol te produceren. Onderzoekers brengen eerst een speciaal chemisch handvat aan — een “gestrengde” alkyne genaamd DBCO — op HaloTag met een korte chloroalkaan‑linker. Vervolgens worden de bacteriën blootgesteld aan testmoleculen die elk een zeer kleine azide‑tag dragen. Alleen die testmoleculen die de buitenmembraan passeren, de binnenmembraan doorkruisen en het cytosol bereiken, kunnen reageren met het DBCO‑handvat in een zeer selectieve "click"‑reactie en HaloTag permanent markeren. Ten slotte worden de cellen behandeld met een azide‑getagde fluorescente kleurstof die alleen bindt aan eventueel nog vrije DBCO. Hoe feller de fluorescentie, hoe minder testmoleculen het cytosol bereikten; zwakkere cellen duiden op betere accumulatie.
Onderzoeken hoe chemie en biologie de toegang van geneesmiddelen vormen
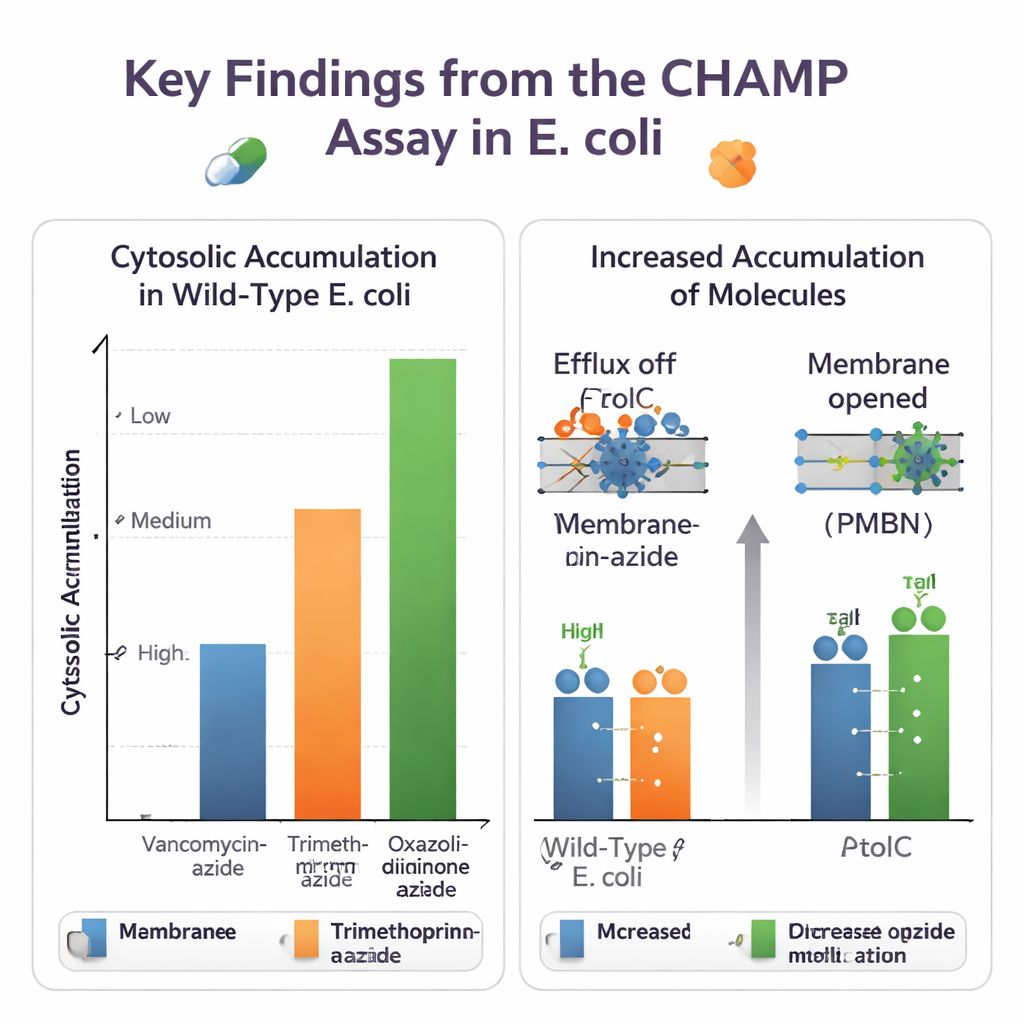
Met CHAMP stelde het team eerst de expressie van HaloTag, de hoeveelheid DBCO‑anker en de keuze van fluorescente kleurstoffen fijn af om een groot en betrouwbaar signaalvenster te krijgen. Daarna gebruikten ze sets nauw verwante kleine moleculen om te zien hoe chemische aanpassingen de toegang beïnvloeden. Het omzetten van carboxylzuren in amiden en het toevoegen of verwijderen van basische aminogroepen kon de cytosolische niveaus merkbaar veranderen. In veel gevallen verbeterden primaire aminen de accumulatie, wat echo’s gaf van onafhankelijke "eNTRy‑regels" die door andere groepen zijn ontwikkeld. De assay kon ook azide‑getagde versies van echte antibiotica verwerken en onthulde grote verschillen: omvangrijke geneesmiddelen zoals vancomycine bereikten het cytosol nauwelijks, terwijl kleinere antibiotica zoals trimethoprim‑derivaten en sommige oxazolidinonverbindingen veel gemakkelijker binnendrongen.
Het ontmaskeren van bacteriële verdedigingen die geneesmiddelen weer naar buiten pompen
Aangezien de methode wordt uitgevoerd in levende, genetisch programmeerbare bacteriën, kan zij de rollen van verschillende cellulaire verdedigingsmechanismen uit elkaar halen. De auteurs vergeleken normale E. coli met stammen die TolC misten, een belangrijk onderdeel van een grote multidrug‑effluxpomp, of met cellen behandeld met een kleine molecuul‑inhibitor van TolC. Voor novobiocine en verschillende andere azide‑getagde antibiotica toonde CHAMP duidelijk hogere cytosolische accumulatie wanneer TolC uitgeschakeld was, waarmee deze verbindingen als effluxsubstraten werden bevestigd. Ze testten ook manieren om de buitenmembraanbarrière losser te maken, hetzij chemisch met het peptide PMBN, hetzij genetisch door overexpressie van een wijd open poriekanaal. Veel moleculen die eerder slecht accumuleerden, lieten grote winst zien wanneer het membraan permeabiliseerde, wat benadrukt hoe binnenkomst en efflux samen de interne geneesmiddelniveaus bepalen.
Opschalen naar duizenden moleculen om patronen en regels te vinden
Om echte hoge doorvoer te demonstreren, screenden de onderzoekers een commercieel pakket van 404 azide‑getagde verbindingen en een aangepaste bibliotheek van 1.152 azide‑dragende moleculen. Ze maten accumulatie in meerdere bacteriële contexten, waaronder onbehandelde cellen, PMBN‑behandelde cellen, hyperporineerde cellen en hyperporineerde cellen zonder TolC. Door hetzelfde molecuul over deze condities te vergelijken, konden ze zien welke veranderingen kwamen door de celbiologie in plaats van door eigenaardigheden van click‑reactiesnelheid. Door CHAMP‑gegevens te combineren met computationele analyse, koppelden ze bepaalde fysisch‑chemische kenmerken — zoals polair oppervlak, waterstofbrugcapaciteit en specifieke ring‑scaffolds — aan sterkere herkenning door TolC‑gebaseerde efflux. Dit soort grootschalige profilering begint ontwerprichtlijnen te schetsen voor moleculen die ofwel pompen ontwijken of porines effectiever benutten.
Wat dit betekent voor toekomstige antibiotica
In eenvoudige bewoordingen verandert dit werk E. coli in een hoogdoorvoersensor die precies rapporteert hoeveel van een testverbinding in het deel van de cel terechtkomt waar veel geneesmiddeldoelen zitten. CHAMP vervangt geen tests die aantonen of bacteriën worden gedood, maar het vult een cruciaal gat door "binnenkomen" te scheiden van "schade aanrichten." Met de mogelijkheid om binnen enkele dagen meer dan duizend moleculen in verschillende mutante of chemisch gewijzigde stammen te meten, kunnen onderzoekers nu systematisch leren welke chemische kenmerken opname bevorderen, efflux verminderen of baat hebben bij membraan‑verstorende partners. Die kennis zou het ontwerp van nieuwe antibiotica en hulpgeneesmiddelen die de formidabele verdedigingen van gramnegatieve pathogenen kunnen doorbreken, moeten versnellen voordat resistentie nog meer van het antibiotica‑arsenaal opeist.
Bronvermelding: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Trefwoorden: antibioticaresistentie, Escherichia coli, doorlaatbaarheid van geneesmiddelen, effluxpompen, click-chemie