Clear Sky Science · nl
Het expressieniveau van TREM2 is cruciaal voor microgliale toestand, metabolische capaciteit en de werkzaamheid van TREM2-agonisten
Waarom opruimcellen in de hersenen belangrijk zijn bij Alzheimer
De ziekte van Alzheimer staat vooral bekend om plakkerige eiwitkluwens in de hersenen, maar even belangrijk is hoe de eigen immuuncellen van de hersenen op die schade reageren. Deze cellen, microglia genoemd, fungeren als schoonmakers en EHBO’ers: ze ruimen rommel op, regelen ontsteking en helpen neuronen te overleven. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties voor toekomstige behandelingen: hoeveel van een belangrijke microgliaire receptor, TREM2, is “precies goed” om de hersenen te beschermen — en wanneer kunnen middelen die TREM2 versterken helpen of juist schade veroorzaken?
Een dimmer, geen aan/uit-knop
Eerder genetisch onderzoek liet zien dat mensen met bepaalde verlies-van-functie-veranderingen in het TREM2-gen een hoger risico lopen op late-onset Alzheimer. Toch werd TREM2 vaak behandeld als een aan/uit-schakelaar: aanwezig of afwezig. De onderzoekers bouwden in plaats daarvan een speciale “reporter”-muis waarin microglia oplichten in verhouding tot hoeveel TREM2 ze maken. Daarmee konden ze microglia sorteren in lage, middelmatige en hoge TREM2-groepen en onderzoeken wat elke groep deed. Ze bestudeerden deze cellen zowel in gezonde muizen als in muizen die amyloïde plaques ontwikkelen, een kenmerk van Alzheimerachtige pathologie. 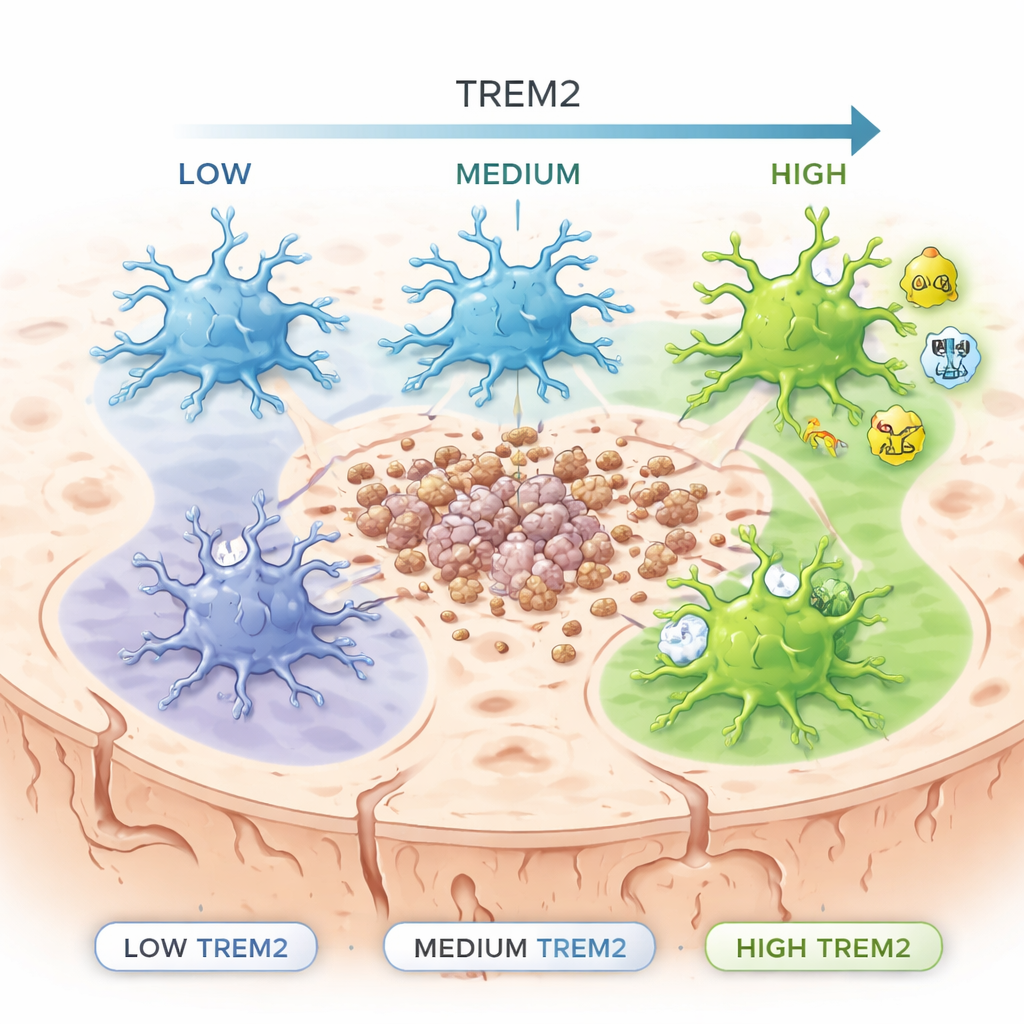
Energiegebruik en cholesterolverwerking verschuiven met TREM2-niveau
Zodra ze deze microgliale subgroepen konden scheiden, analyseerden de onderzoekers welke genen actief waren, welke metabolieten aanwezig waren en hoe actief de cellen energie gebruikten. Microglia met meer TREM2 toonden sterkere activiteit in routes gekoppeld aan oxidatieve fosforylering (het belangrijkste energieproducerende systeem van de cel) en aan cholesterol- en lipidenmetabolisme. Metingen van gelabelde glucose-opname bevestigden dat cellen met hoger TREM2 meer suiker opnemen, vooral in aangedane hersenen. Gedetailleerde metaboliet- en lipideprofielen toonden dat microglia met veel TREM2 meer bouwstenen hadden voor cellulaire energie en antioxidantverdediging, en minder vrij cholesterol en bepaalde vetmoleculen — wat duidt op efficiënter brandstofgebruik en betere cholesterolafvoer.
Van metabolisme naar opruimkracht
Deze moleculaire handtekeningen vertaalden zich naar echte functionele verschillen. In gecontroleerde laboratoriumtesten blootstelden de onderzoekers microglia aan fluorescent gelabelde myelinefragmenten — een model voor het type debris dat microglia in aangedaan hersenweefsel moeten opruimen. Microglia met weinig TREM2 namen het minste debris op; die met middelmatige niveaus deden het beter; en de hoge-TREM2-cellen waren het meest vraatzuchtig. Hetzelfde patroon verscheen in twee verschillende Alzheimerachtige muismodellen, wat onderstreept dat het TREM2-niveau sterk verbonden is met de “opruimcapaciteit” van de cel. Tegelijkertijd toonden genennetwerkanalyses dat hoger TREM2 niet alleen geassocieerd was met verbeterd metabolisme, maar ook met bepaalde immuunresponsprogramma’s, waaronder interferon-gerelateerde signalen die in sommige contexten gunstig en in andere schadelijk kunnen zijn. 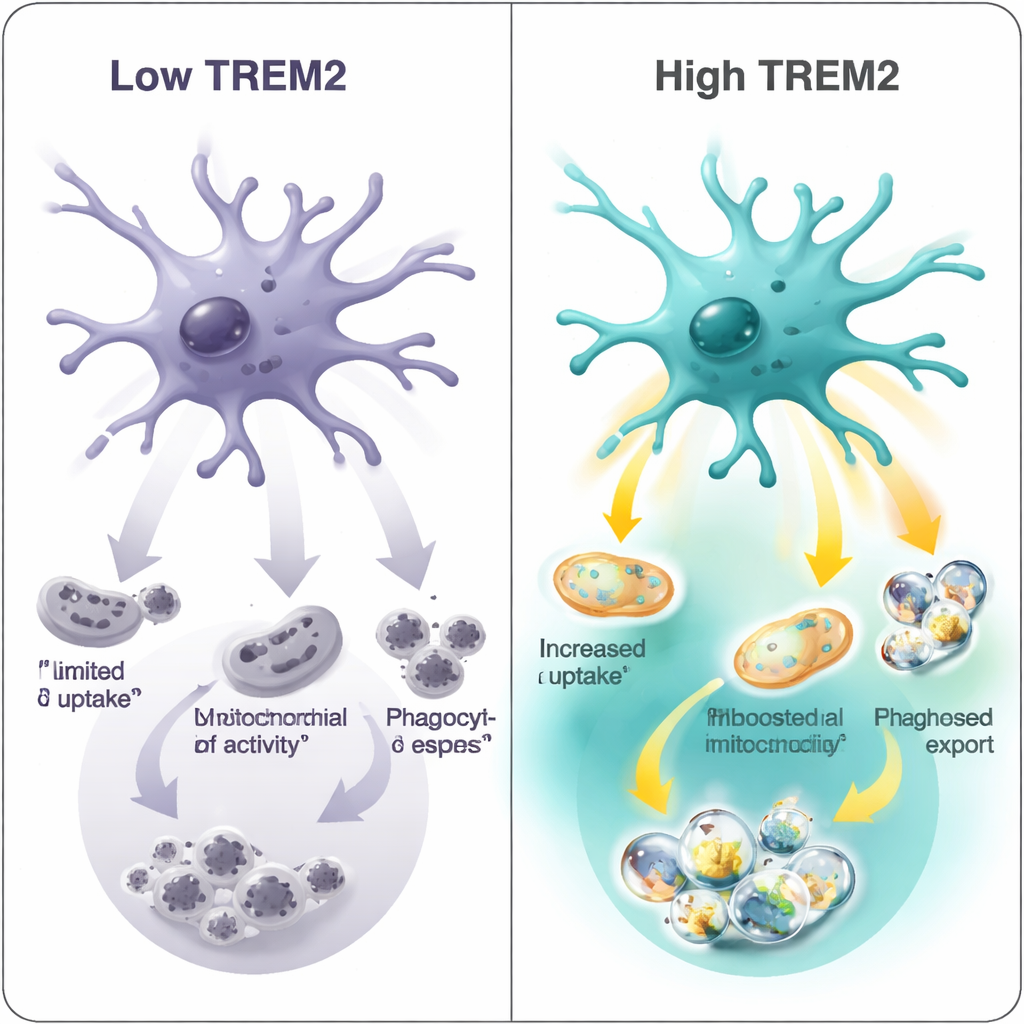
Wanneer het versterken van TREM2 helpt — en wanneer het kan overschrijden
Aangezien farmaceutische bedrijven antistoffen testen die TREM2 activeren, onderzochten de auteurs hoe zo’n middel microglia met verschillende basale TREM2-niveaus beïnvloedt. Ze behandelden reporter-muizen met amyloïde pathologie met een TREM2-activerende antistof die de bloed-hersenbarrière kan passeren, en sorteerden vervolgens opnieuw microglia op TREM2-expressie. Opvallend reageerden de cellen met middelmatig TREM2 het sterkst: hun metabolische markers lieten verhoogde glycolyse zien, verbeterde lysosomale en peroxisomale activiteit, en hogere niveaus van bepaalde beschermende membraanlipiden. Microglia met weinig TREM2 veranderden nauwelijks, waarschijnlijk omdat ze niet genoeg doelwit voor het middel boden. Bij microglia met veel TREM2 leek dezelfde behandeling het metabolisme echter terug te duwen naar een meer gematigde toestand, wat wijst op een “plafondeffect” waarbij excessieve activatie wordt afgeremd in plaats van versterkt.
Wat dit betekent voor toekomstige Alzheimerbehandelingen
De kernboodschap voor een lezer zonder wetenschappelijke achtergrond is dat microglia met de juiste hoeveelheid TREM2 beter van brandstof worden voorzien, beter cholesterol beheren en beter schadelijk materiaal rondom amyloïde plaques opruimen. Maar het evenwicht is fragiel. Middelen die TREM2 stimuleren werken waarschijnlijk het beste binnen een specifiek venster van receptorlevels — te weinig TREM2 en er is niet genoeg om te activeren; te veel en het systeem zit al dicht bij of voorbij zijn optimale punt. Dit helpt verklaren waarom een vroege klinische studie met een TREM2-versterkende antistof mislukte en suggereert dat toekomstige onderzoeken mogelijk TREM2-activiteit en microgliale toestand in de tijd moeten meten, bijvoorbeeld met beeldvorming van de hersenen, om de juiste patiënten en timing van behandeling te kiezen. Kortom, dit werk herdefinieert TREM2 als een fijn afstelbare “dimmer” voor microgliaal metabolisme en opruimwerk, in plaats van een eenvoudige aan/uit-schakelaar, en biedt een routekaart voor slimmere, meer gerichte immunotherapieën bij de ziekte van Alzheimer.
Bronvermelding: Feiten, A.F., Dahm, K., Schlepckow, K. et al. TREM2 expression level is critical for microglial state, metabolic capacity and efficacy of TREM2 agonism. Nat Commun 17, 2002 (2026). https://doi.org/10.1038/s41467-026-68706-8
Trefwoorden: microglia, TREM2, Ziekte van Alzheimer, hersenenmetabolisme, immunotherapie