Clear Sky Science · nl
Cachexie bij STK11/LKB1-gemuteerde niet-kleincellige longkanker hangt af van tumor-secretie van GDF15
Waarom sommige longkankers gevaarlijk gewichtsverlies veroorzaken
Kanker groeit niet altijd stilletjes op één plek. Bij veel mensen berooft het de lichaams van vet, spierkracht en energie in een aandoening die verlies of cachexie wordt genoemd. Deze studie onderzoekt een urgente vraag voor patiënten met een veelvoorkomend type longkanker: waarom veroorzaken sommige tumoren dit ernstige gewichtsverlies terwijl andere dat niet doen? De onderzoekers traceren het probleem naar een stresssignaal dat door bepaalde tumoren wordt gemaakt en tonen aan dat het blokkeren van dit signaal bij proefdieren het gewichtsverlies grotendeels kan stoppen of zelfs kan terugdraaien.
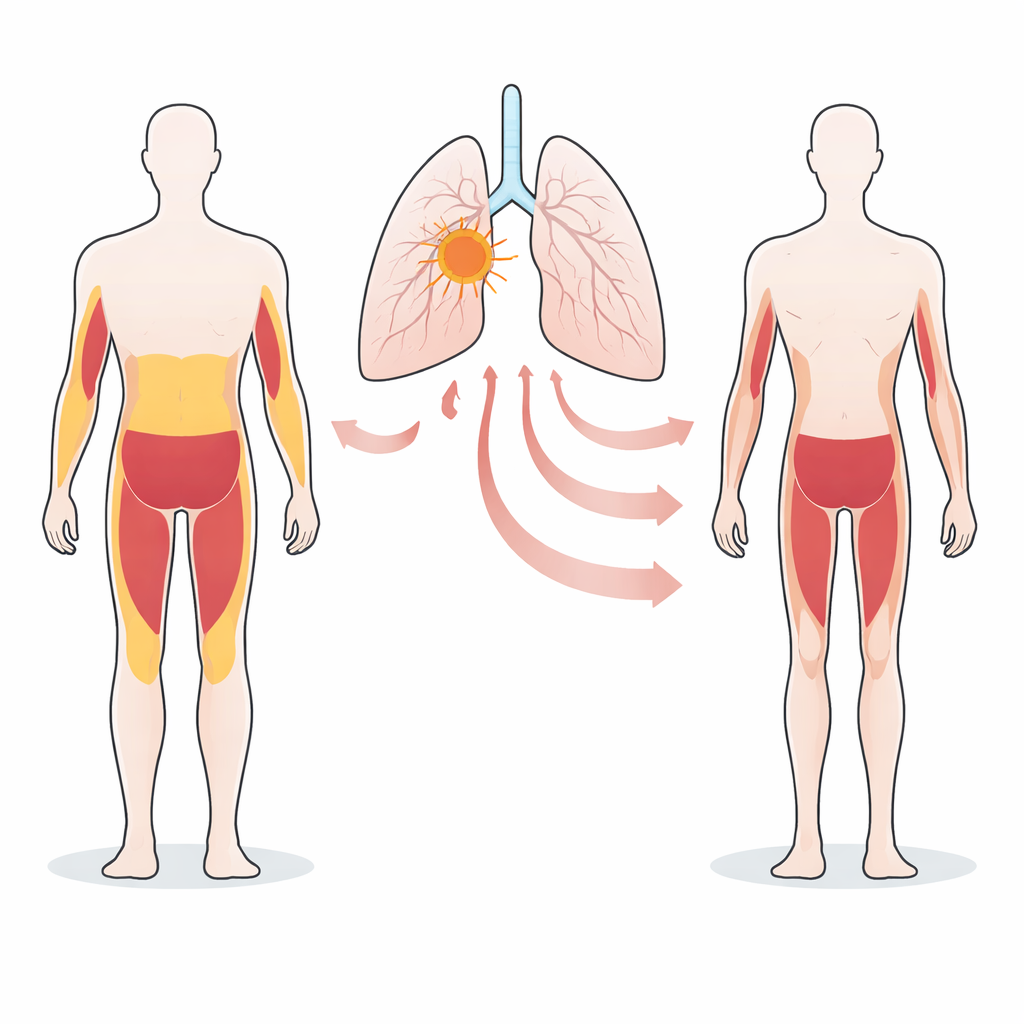
Een verborgen verband tussen tumorgenen en lichaamsverlies
Het team richtte zich op niet-kleincellige longkankers die foutieve versies van het gen STK11/LKB1 dragen. Eerder werk liet zien dat tumoren met dit defect vaak samengaan met sterk verlies van gewicht, vet en spieren bij zowel muizen als patiënten. Hier vergeleken de wetenschappers veel menselijke longtumorlijnen die bij het uitgroeien in muizen wél of géén cachexie veroorzaakten. Ze vonden dat de verwoestende tumoren met STK11/LKB1-defecten veel hogere hoeveelheden van een hormoonachtig stress-eiwit genaamd GDF15 produceerden, en dat dit eiwit in de bloedbaan terechtkwam. Cellen van de gastheer droegen daarentegen weinig bij aan de in het bloed gevonden GDF15, wat erop wijst dat de tumor zelf de belangrijkste bron is.
Aantonen dat het tumorsignaal gewichts-, vet- en spierverlies veroorzaakt
Om te testen of door tumoren geproduceerd GDF15 daadwerkelijk cachexie veroorzaakt, gebruikten de onderzoekers genetische middelen om GDF15 alleen in de kankercellen uit te schakelen, terwijl alle andere genen onaangetast bleven. In verschillende STK11/LKB1-gemuteerde longkankerlijnen remde het uitzetten van GDF15 de tumorgroei niet, maar het beschermde muizen krachtig tegen verlies van lichaamsgewicht, vetmassa, spiermassa en grijpkracht. Deze bescherming trad op bij zowel mannelijke als vrouwelijke dieren en in modellen waarbij tumoren onder de huid of direct in de long werden geplaatst, wat suggereert dat het effect voortkomt uit factoren die in het bloed worden afgegeven en niet uit de locatie van de tumor. Zelfs wanneer tumoren slechts matige hoeveelheden GDF15 produceerden, dempte het afsnijden van dit signaal nog steeds de cachexie, wat laat zien dat relatief lage niveaus biologisch belangrijk kunnen zijn.
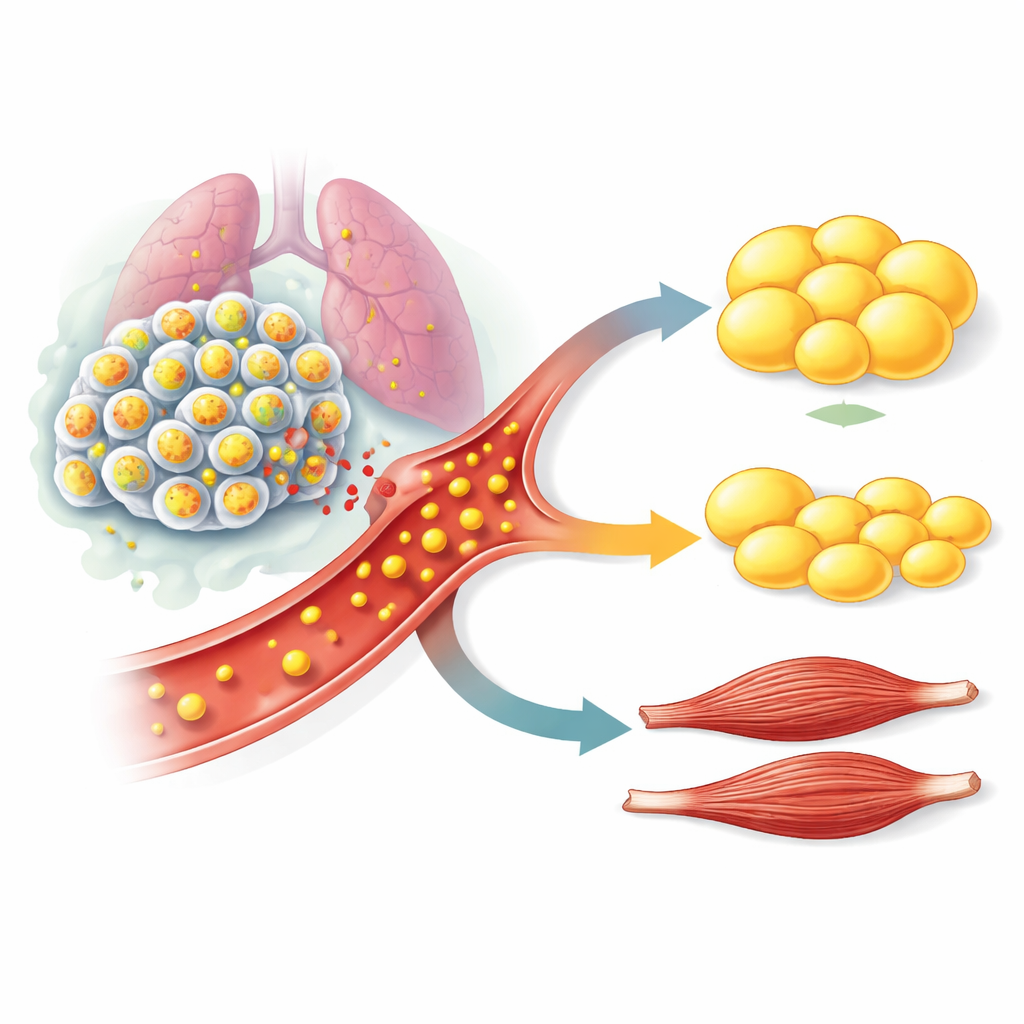
Antistoffen die het signaal blokkeren tonen therapeutische belofte
Aangezien farmaceutische bedrijven al antistoffen ontwikkelen die GDF15 neutraliseren, vroegen de onderzoekers of zo’n benadering in hun modellen behulpzaam zou zijn. Ze behandelden muizen met STK11/LKB1-gemuteerde tumoren met een GDF15-blokkerende antistof vergelijkbaar met een kandidaat die nu in klinische onderzoeken zit. Wanneer de antistof vroeg werd toegediend, voorkwam zij het gebruikelijke verlies van vet, spier en kracht zonder de tumorgroei te beïnvloeden. Wanneer de behandeling later plaatsvond—nadat de dieren al een groot deel van hun vetreserve hadden verloren—kon dezelfde antistof verdere achteruitgang stoppen en gedeeltelijk de lichaamsreserves en het spiergewicht herstellen. Vergelijkbare resultaten werden gezien in een muismodel van longkanker met een intact immuunsysteem, wat erop wijst dat de bevindingen niet beperkt zijn tot immuundeficiënte dieren.
Hoe een gestreste tumor de cachexie-schakelaar omzet
De studie onderzoekt ook waarom STK11/LKB1-gemuteerde tumoren zoveel GDF15 maken. Cellen gebruiken een intern alarmsysteem, de stressrespons, om om te gaan met lage voedingsstoffen en andere bedreigingen. In tumoren zonder werkend STK11/LKB1 is dit alarm chronisch actief, wat de productie en verwerking van GDF15 naar de volwassen, uitgescheiden vorm verhoogt. Toen de onderzoekers een werkend STK11/LKB1-gen herintroduceerden in een menselijke longkanker-lijn, kalmeerde de stressrespons. De GDF15-niveaus in de tumor en in het bloed daalden sterk, de voedselopname verbeterde en de dieren ontwikkelden geen cachexie meer, hoewel de tumoren nog steeds aanwezig waren.
Wat dit betekent voor patiënten met longkanker
Voor mensen met niet-kleincellige longkankers die STK11/LKB1-mutaties dragen, suggereert dit werk dat de tumor zelf kan fungeren als een endocrien orgaan dat GDF15 in de bloedbaan vrijgeeft en zo systemische cachexie veroorzaakt. Bij muizen verminderde het blokkeren van GDF15—hetzij door het uit de tumor te verwijderen, hetzij door een antistof in de circulatie te gebruiken—sterk het verlies van vet en spier zonder de tumor direct te laten krimpen. Dat wekt de mogelijkheid dat, bij de ongeveer 15 procent van longkankerpatiënten met STK11/LKB1-defecten, anti-GDF15-therapieën kunnen helpen om kracht en lichaamsgewicht te behouden over een breed scala aan bloed-GDF15-niveaus. Met andere woorden: het dempen van dit ene tumorgeproduceerde signaal zou op termijn een praktische manier kunnen bieden om een van de meest slopende complicaties van kanker te verlichten.
Bronvermelding: Yu, J., Guo, T., Gupta, A. et al. Cancer cachexia in STK11/LKB1-mutated non-small cell lung cancer is dependent on tumor-secreted GDF15. Nat Commun 17, 2182 (2026). https://doi.org/10.1038/s41467-026-68702-y
Trefwoorden: kanker-cachexie, niet-kleincellige longkanker, GDF15, STK11 LKB1-mutatie, verlies van spier en vet