Clear Sky Science · nl
Functionele en structurele inzichten in interacties tussen β-Arrestine 1 en Gαs of Gαi1
Waarom dit belangrijk is voor gezondheid en geneeskunde
Veel van de geneesmiddelen die we vandaag gebruiken — van allergiepillen tot hartmedicijnen en psychiatrische behandelingen — werken door een grote familie van eiwitten op de celoppervlakte te richten: G-eiwit–gekoppelde receptoren, of GPCR’s. Deze receptoren geven berichten door aan de cel met behulp van twee hoofdhelpers: G-eiwitten en eiwitten genaamd beta-arrestines. Deze studie onderzoekt hoe één beta-arrestine (beta-arrestine 1) rechtstreeks communiceert met twee typen G-eiwitten binnen de cel. Begrijpen hoe dit verborgen gesprek verloopt kan wetenschappers helpen preciezere geneesmiddelen te ontwerpen met minder bijwerkingen door te sturen hoe signalen binnen onze cellen vloeien.
Twee belangrijke boodschappers in onze cellen
Wanneer een hormoon of medicijn aan een GPCR op het celoppervlak bindt, activeert dat twee brede communicatieroutes. De ene route gebruikt G-eiwitten, die als moleculaire timers aan- en uitgezet worden door één klein molecuul (GDP) te verwisselen voor een ander (GTP). De andere route gebruikt beta-arrestines, die zowel de G-eiwitsignalering kunnen afsluiten als zelf signaleringspaden kunnen opstarten. Lange tijd bestudeerden wetenschappers vooral hoe receptoren apart met G-eiwitten of met beta-arrestines communiceren. Recente studies suggereerden dat G-eiwitten en beta-arrestines ook aan elkaar kunnen binden of zelfs grote “mega-complexen” met de receptor kunnen vormen. Maar de details van hoe deze eiwitten zich verbinden en wat dat betekent voor signalering waren onduidelijk.
Meten wie met wie bindt
In dit onderzoek richtten de onderzoekers zich op beta-arrestine 1 en twee G-eiwit “alfa”-subunits: Gαs, dat meestal de celactiviteit stimuleert, en Gαi1, dat die gewoonlijk dempt. Met een gevoelige bindingsmethode testten ze hoe sterk gezuiverde beta-arrestine 1 en elk G-eiwit onder verschillende omstandigheden aan elkaar kleven. Ze vonden dat de sleutel niet is of het G-eiwit “aan” of “uit” staat, maar of beta-arrestine 1 zich in een meer actieve, flexibele vorm bevindt. Een variant van beta-arrestine 1 zonder zijn staart — die zich gedraagt als een losse, actieve verzameling conformaties — bond sterk aan zowel Gαs als Gαi1. Daarentegen bond de rustvorm van beta-arrestine 1, of een vorm vergrendeld door een receptor-staart–achtig peptide, zwak of helemaal niet. Dit suggereert dat G-eiwitten de voorkeur geven aan beta-arrestine 1 wanneer deze actieve-achtige vormen uitprobeert die kunnen bestaan na receptoractivatie. 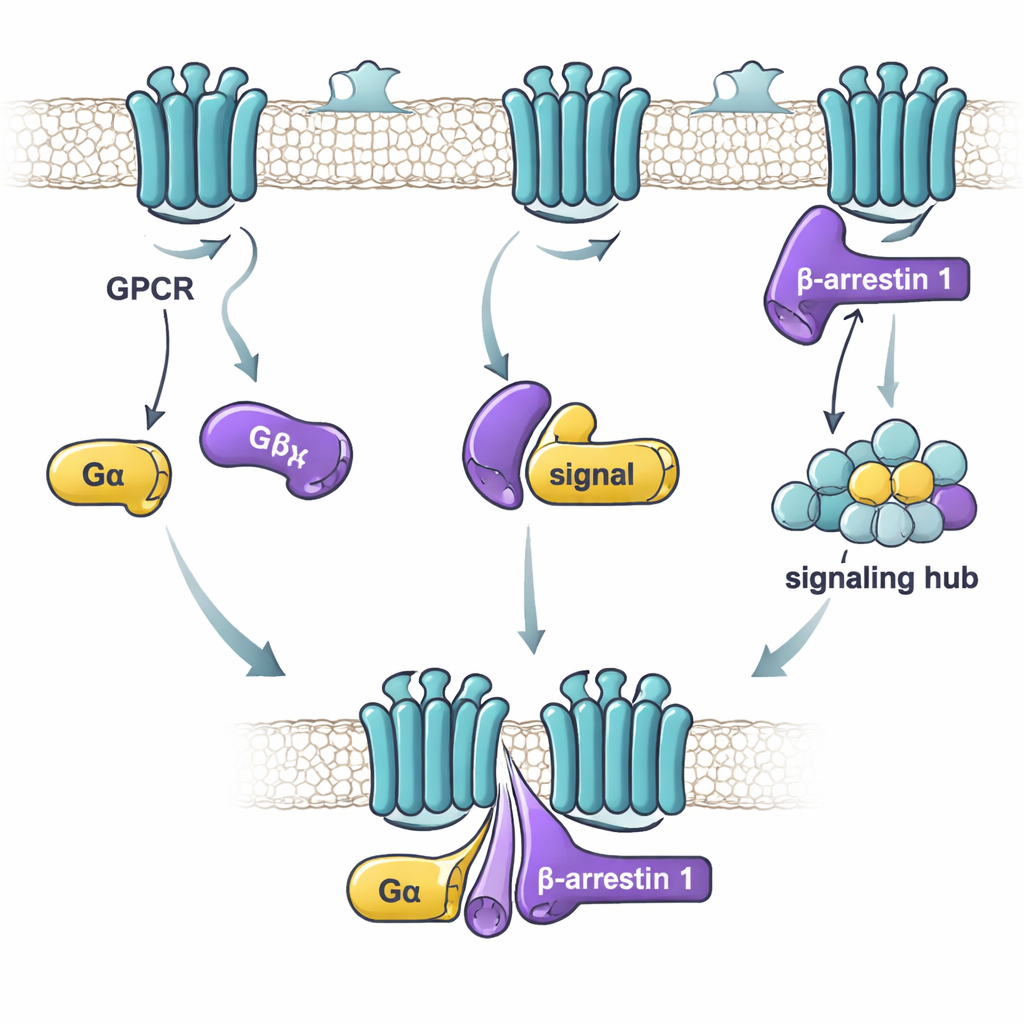
Fijne vormveranderingen volgen
Om te zien hoe binding de eiwitvorm beïnvloedt, gebruikte het team een methode die bijhoudt hoe snel waterstofatomen in de eiwitbackbone uitgewisseld worden met zwaar waterstof uit het oplosmiddel. Langzamere uitwisseling betekent meestal dat een regio meer beschermd of stijver is geworden; snellere uitwisseling wijst op meer flexibiliteit of blootstelling. Wanneer het actieve-achtige beta-arrestine 1-fragment aan Gαs of Gαi1 bond, lieten beide G-eiwitten duidelijke patroonveranderingen zien in meerdere regio’s, wat aangeeft dat ze zich rond het complex hervormen. Beta-arrestine 1 zelf veranderde daarentegen slechts licht, voornamelijk in flexibele lussen. Door te werken met geïsoleerde domeinen van de G-eiwitten lieten de onderzoekers ook zien dat zowel het belangrijkste katalytische ‘Ras-achtige’ deel als het omringende alfa-helical deel bijdragen aan de binding. Bij Gαs speelt het helical deel een bijzonder sterke rol; bij Gαi1 zijn beide delen ongeveer even belangrijk.
Functie zonder de hoofdschakel om te zetten
De volgende vraag was of dit directe contact verandert hoe G-eiwitten inschakelen. Het team gebruikte een fluorescente GTP-nabootsende probe die oplicht wanneer een G-eiwit van GDP naar GTP wisselt — een standaardmaat voor activatie. Verrassend genoeg veranderde het toevoegen van beta-arrestine 1 noch de snelheid noch de mate van deze nucleotidewisseling voor Gαs of Gαi1. Met andere woorden: beta-arrestine 1 werkt niet als een klassieke ‘aan-schakelaar’ voor G-eiwitten. In plaats daarvan toont zijn invloed zich op zijn eigen structuur. Met een slim geconstrueerde beta-arrestine 1 waarvan de staartbeweging via fluorescentie gevolgd kon worden, vonden ze dat actief Gαs, maar niet Gαi1, de loslating van de C-terminus van beta-arrestine bevordert wanneer een receptorafgeleid peptide aanwezig is. In levende cellen bevestigden aanvullende beeldvorming en energie-overdrachtsensoren dat Gαs en beta-arrestine 1 bij hormoonstimulatie dicht bij elkaar komen en dat Gαs helpt beta-arrestine 1 naar een meer actieve conformatie te duwen. 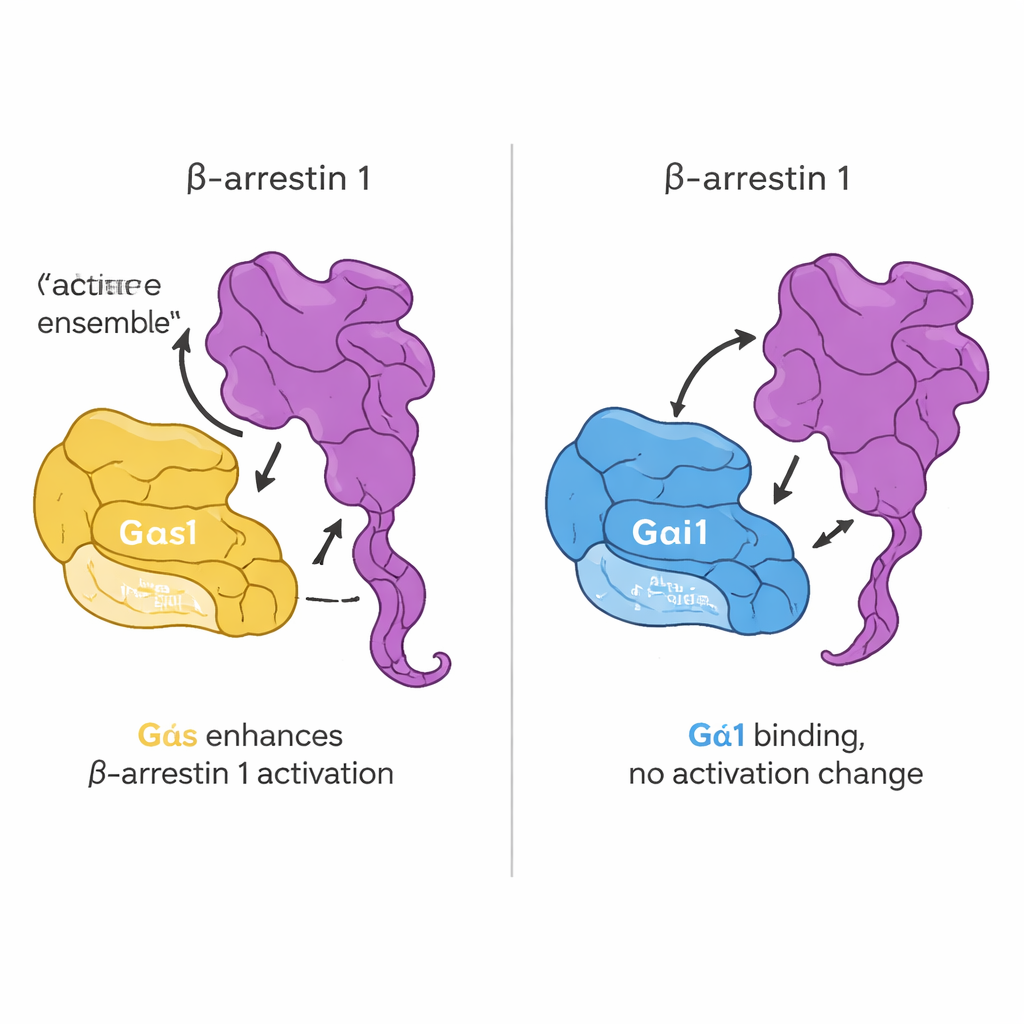
Een nieuwe laag van controle in celsignalering
Samengevoegd stellen de resultaten voor dat Gαs en Gαi1 allebei rechtstreeks aan beta-arrestine 1 binden, maar op enigszins verschillende manieren en met uiteenlopende gevolgen. Geen van beide G-eiwitten verandert daardoor hun belangrijkste ‘aan/uit’-gedrag. In plaats daarvan werkt de interactie, vooral voor Gαs, meer als een fijnregelknop voor beta-arrestine 1; ze duwt of stabiliseert deze in een meer actieve, staart-weggezette vorm. Dit voegt een eerder ondergewaardeerde laag toe aan GPCR-signaleringsroutes: receptoren kunnen niet alleen G-eiwitten en beta-arrestines coördineren, maar G-eiwitten en beta-arrestines kunnen ook direct elkaars gedrag beïnvloeden. Op de lange termijn kan het in kaart brengen van deze subtiele interacties geneesmiddelontwerpers helpen signalering in gunstige banen te sturen — door nuttige paden te versterken en die te vermijden die bijwerkingen veroorzaken.
Bronvermelding: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Trefwoorden: G-eiwit-gekoppelde receptoren, beta-arrestine, G-eiwit signalering, celsignaleringsmechanismen, structurele biologie