Clear Sky Science · nl
Epigenoom-brede analyse identificeert DNA-methyleringsmediatoren van behandelgerelateerd cardiometabool risico bij overlevenden van kinderkanker
Waarom de nasleep van kanker in het lichaam blijft hangen
Dankzij betere behandelingen groeien de meeste kinderen met kanker tegenwoordig op. Maar veel van deze overlevenden krijgen decennia later nieuwe gezondheidsproblemen, waaronder obesitas, hoge bloeddruk en aandoeningen die op diabetes lijken. Deze studie stelt een prangende vraag: hoe laten behandelingen in de kinderjaren zulke langdurige sporen achter voor hart en stofwisseling? Door te kijken naar chemische labels op DNA in bloedcellen vinden de onderzoekers aanwijzingen dat vroegere chemotherapie en bestraling het lichaam kunnen “herprogrammeren” op manieren die het lange-termijn cardiometabole risico verhogen.
Verborgen risico’s volgen bij volwassenen die als kind kanker hadden
Het team bestudeerde bijna 3.000 volwassenen die kinderkanker overleefden en worden gevolgd in de langlopende St. Jude Lifetime Cohort. Deze overlevenden kregen als kinderen verschillende chemotherapieën en bestraling aan de hersenen of romp (borst, buik, bekken) en keerden jaren later terug voor uitgebreide gezondheidscontroles en bloedonderzoek. De wetenschappers richtten zich op vijf belangrijke cardiometabole problemen die bekend zijn als risicofactoren voor hartziekte en voortijdig overlijden: obesitas, abnormale bloedsuikers, hoge triglyceriden, hoog cholesterol en hoge bloeddruk. Door overlevenden met en zonder deze condities te vergelijken, doorzochten zij miljoenen locaties in het genoom op verschillen in DNA-methylering — kleine chemische schakelaars die helpen bepalen hoe genen aan- of uitgeschakeld worden.
Chemische labels op DNA als herinnering aan behandeling
In het hele genoom vonden de onderzoekers bijna 1.900 DNA-locaties waar methyleringsniveaus gekoppeld waren aan minstens één van de vijf cardiometabole aandoeningen. De meeste van deze locaties waren verbonden aan één enkel probleem, maar een kleine groep leek fungeren als “hubs” die met meerdere problemen geassocieerd waren. Vijf sleutelplaatsen, gelegen in de buurt van twee genen genaamd CPT1A en LMNA, waren in verband met alle vijf cardiometabole risico’s tegelijk. Van deze genen is bekend dat ze de vetstofwisseling en de structurele integriteit van cellen beïnvloeden, wat suggereert dat behandeling gedeelde metabole en cardiovasculaire paden kan verstoren. Veel van de methyleringsveranderingen overlappen met signalen die eerder in de algemene bevolking zijn gezien, vooral die gerelateerd aan ontsteking, maar andere leken uniek te zijn voor kankeroverlevenden — wat suggereert dat behandeling een eigen, herkenbare biologische afdruk achterlaat.
Behandelingsverbanden, DNA-veranderingen en ziekte met elkaar verbinden
De volgende stap was onderzoeken of deze methyleringsveranderingen daadwerkelijk helpen verklaren hoe behandeling later tot ziekte leidt, in plaats van alleen maar mee te hangen. De onderzoekers concentreerden zich op nieuwe of verslechterende cardiometabole problemen die pas ontstonden nadat het bloedmonster was afgenomen, zodat de tijdlijn van behandeling naar DNA-verandering naar ziekte gewaarborgd bleef. Met statistische mediatieanalyses identificeerden zij 24 methyleringsplaatsen die samen tot ongeveer een kwart van het verband tussen specifieke behandelingen en latere cardiometabole problemen verklaarden. Bestraling van de hersenen en de romp toonde vooral sterke patronen: groepen methyleringsplaatsen verklaarden ruwweg 10–20% van de impact van deze radiotherapieën op abnormale bloedsuikers. Eén opvallende plaats, nabij een gen genaamd ANTXR2, leek ongeveer 20% van het effect van rompbestraling op latere glucoseproblemen te mediëren.
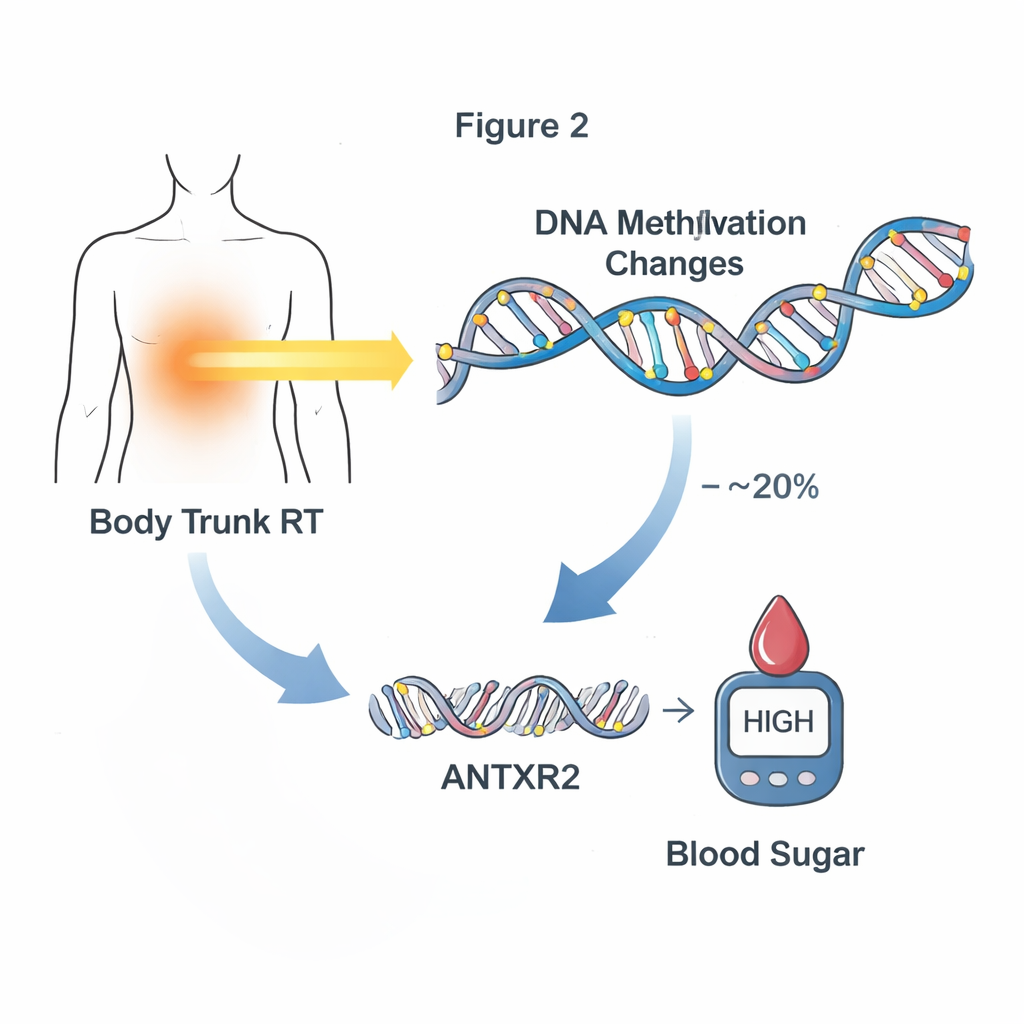
Van DNA-markeringen naar genactiviteit
Om te begrijpen hoe deze methyleringsmarkeringen de biologie zouden kunnen veranderen, bekeek het team genexpressie in een subset van overlevenden met zowel DNA- als RNA-gegevens uit hun bloed. Ze vonden tientallen methyleringsplaatsen waar hogere of lagere methylering gekoppeld was aan veranderingen in de expressie van nabijgelegen genen. Onder hen bevond zich de sleutelmediatorplaats nabij ANTXR2, waar methyleringsniveaus sterk samenhingen met de hoeveelheid expressie van dit gen, vooral bij overlevenden die rompbestraling hadden ontvangen. ANTXR2 helpt bij de regulatie van bloedvaten en het omliggende weefselraamwerk — systemen die beïnvloeden hoe glucose en insuline door het lichaam bewegen. Dit patroon suggereert een keten van gebeurtenissen waarbij bestraling methylering verandert, wat genactiviteit verschuift, en dat op zijn beurt het lichaam richting abnormale bloedsuikers kan duwen.
Wat dit betekent voor overlevenden en toekomstige zorg
Voor niet-specialisten is de kernboodschap dat behandelingen voor kinderkanker niet alleen op het moment weefsels beschadigen; ze kunnen ook blijvende “notities” op het DNA achterlaten die de gezondheid decennialang vormen. In deze studie helpen sommige van die notities — veranderingen in DNA-methylering — verklaren waarom bepaalde overlevenden een grotere kans hebben op obesitas, verhoogde vetwaarden in het bloed of glucoseproblemen die verband houden met diabetes en hartziekte. Hoewel deze chemische labels slechts een deel van het verhaal zijn, zouden ze uiteindelijk kunnen dienen als bloedgebaseerde biomarkers om overlevenden met het hoogste risico te identificeren en om te testen of leefstijlaanpassingen of nieuwe therapieën sommige van deze epigenetische sporen veilig kunnen herschrijven. Het werk brengt nazorg voor overlevenden een stap dichter bij precisiegeneeskunde: het gebruik van moleculaire voetafdrukken van eerdere behandeling om vroegere, meer gerichte preventie van hart- en metabole ziekten te sturen.
Bronvermelding: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Trefwoorden: overlevenden van kinderkanker, DNA-methylering, cardiometabool risico, radiotherapie, epigenetica