Clear Sky Science · nl
Co-translationale bepaling van quaternaire structuren in chaperone-fabrieken
Hoe cellulaire “assemblagelijnen” grote machines in vorm houden
In elke cel moeten duizenden eiwitonderdelen in elkaar passen tot complexe moleculaire machines, van de motoren die DNA kopiëren tot de fabrieken die andere RNA-moleculen bouwen. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: hoe beslissen cellen, in real time, welke hulp-eiwitten elk nieuw onderdeel begeleiden terwijl het wordt gemaakt, en hoe houden ze dit proces georganiseerd in het chaotische cytoplasma van de cel?
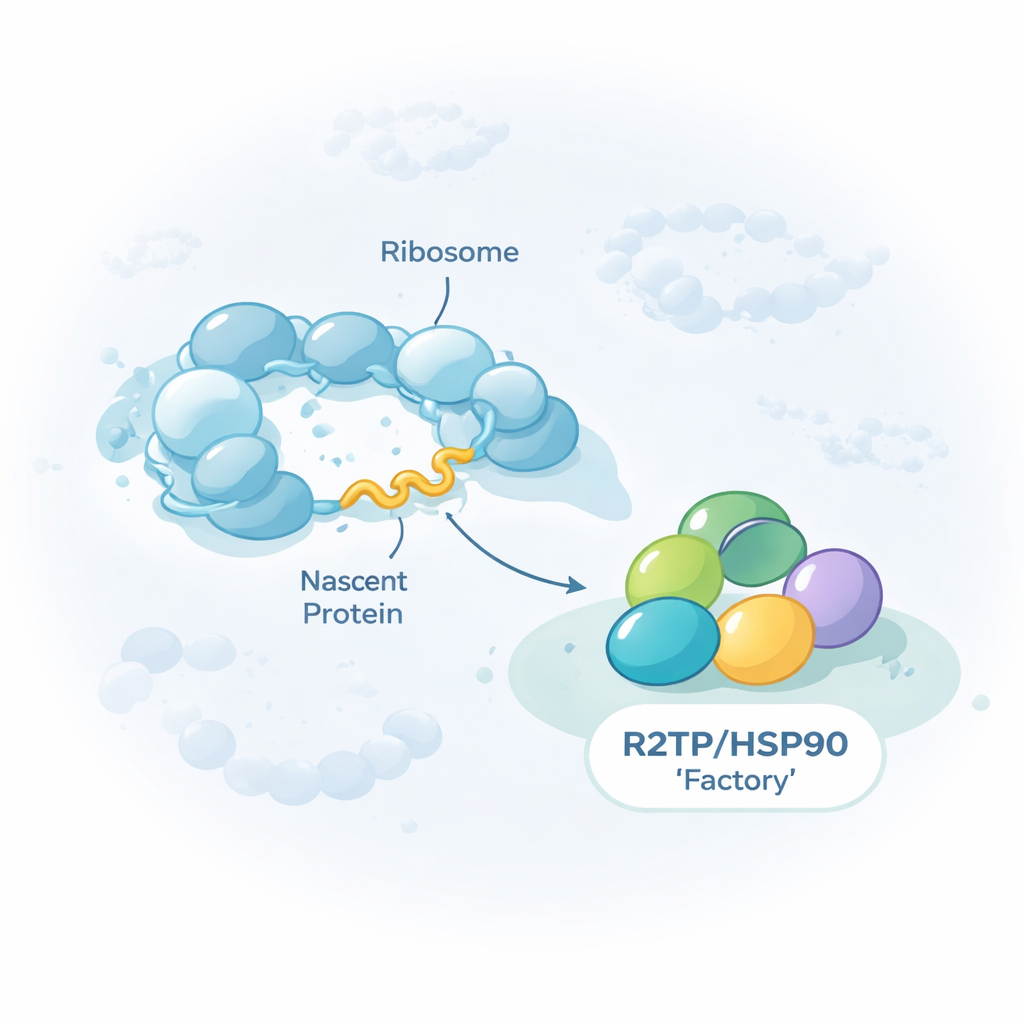
Een alleskunner voor cellulaire mega-machines
Het onderzoek concentreert zich op een groep hulp-eiwitten, of chaperonnes, bekend als HSP90/R2TP. In plaats van individuele eiwitten te laten vouwen, is deze chaperonne gespecialiseerd in het assembleren van reusachtige meeronderdeelcomplexen, waaronder de drie nucleaire RNA-polymerases die DNA in RNA transcriberen, bepaalde RNA–eiwitdeeltjes en grote remodelleringsmachines die de DNA-verpakking hervormen. De auteurs tonen aan dat R2TP deze cliënt-eiwitten niet alleen ontmoet nadat ze klaar zijn. Vaak hecht het zich terwijl elk cliënt-eiwit nog wordt aangemaakt op ribosomen, de eiwitfabrieken van de cel. Door R2TP uit menselijke cellen te trekken en de bijbehorende RNA’s te sequencen, vonden ze ongeveer 150 boodschapper-RNA’s waarvan de gecodeerde eiwitten tijdens hun eigen translatie door R2TP worden aangeraakt.
Hulp die meereist op groeiende eiwitketens
Om te testen of deze binding daadwerkelijk tijdens eiwitsynthese plaatsvindt, gebruikte het team medicijnen die translatie bevriezen of ontregelen. Wanneer ze verbindingen gebruikten die groeiende eiwitketens van ribosomen verwijderen, verdwenen de meeste boodschapper-RNA’s uit R2TP’s greep. Maar wanneer ze een middel gebruikten dat ribosomen eenvoudigweg pauzeert en de ontluikende ketens bevestigd laat, nam R2TP-binding juist toe. Gericht geconstrueerde rapporter-RNA’s bevestigden dit: als translatie kunstmatig vroeg werd gestopt, bond de chaperonne niet langer aan het bericht. Samen wijzen deze resultaten op een duidelijke engagementregel: R2TP herkent zijn cliënten voornamelijk via de voortkomende eiwitketen die uit het ribosoom komt, eerder dan via de RNA-sequentie zelf.
Chaperone-gebouwde “fabrieken” die specifieke boodschappen clusteren
Met geavanceerde single-molecule imaging deden de auteurs vervolgens een verrassende ontdekking. In plaats van veel verschillende cliënt-berichten willekeurig verspreid te zien, observeerden ze dat sommige sleutelberichten — vooral die voor de grote subunits van RNA-polymerase II en een groot splicingfactorcomplex-lid genaamd PRPF8 — vaak samenkwamen in heldere focuspunten in het cytoplasma. Deze foci waren verrijkt aan R2TP en zijn partner HSP90, evenals aan ribosomale componenten en de eiwitten die werden gemaakt, wat aantoont dat het actieve translatieplaatsen zijn. Wanneer translatie of de energieverslindende ATPase-activiteit van R2TP of HSP90 werd geblokkeerd, losten deze foci op. De auteurs noemen deze structuren “R2TP-fabrieken”: gespecialiseerde condensaten waar geselecteerde boodschapper-RNA’s en chaperonnes geconcentreerd zijn om tijdige, beschermende contacten tussen ontluikende eiwitketens en hun assemblagehelpers te bevorderen.
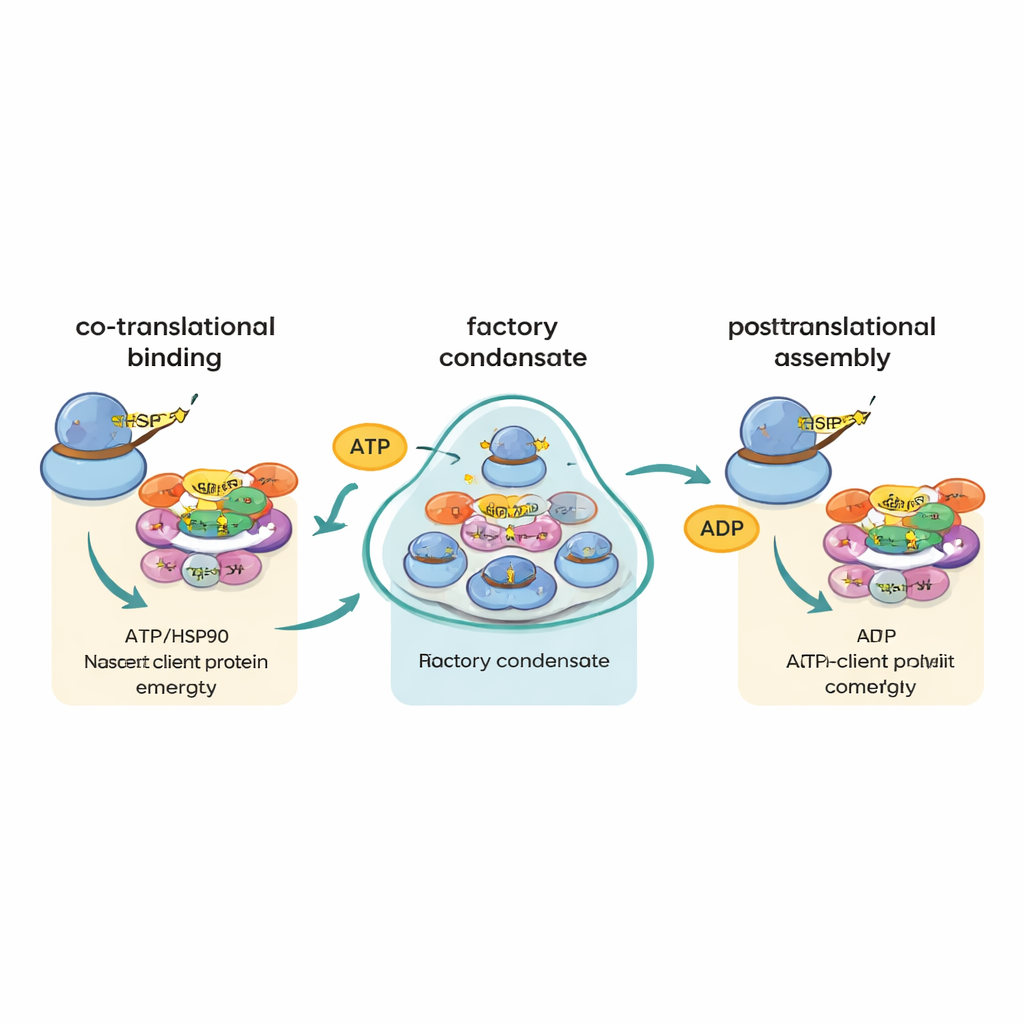
Onderdelen routeren zonder de blauwdrukken te matchen
Een eerder idee was dat berichten die verschillende onderdelen van hetzelfde complex coderen, elkaar zouden vinden en naast elkaar vertaald worden, zodat hun eiwitproducten onmiddellijk kunnen assembleren. Het nieuwe werk sluit dit “gecolokaliseerde blauwdruk”-model grotendeels uit. Zelfs voor eiwitparen die bekend staan om samen te voegen in hetzelfde complex, verschenen hun boodschapper-RNA’s zelden samen. In plaats daarvan ondersteunen de gegevens een andere strategie die de auteurs “co-translational chaperone channeling”, of “cha-cha”, noemen. In dit model, zodra elk groot of assemblage-gevoelig eiwit begint tevoorschijn te komen uit het ribosoom, grijpen R2TP en HSP90 in en bepalen ze het lot van dat eiwit en gidsen het door verdere assemblagestappen. De fabrieken zelf brengen dus niet hoofdzakelijk overeenkomende berichten bij elkaar; ze verhogen eerder de kans dat kwetsbare nieuwe eiwitten snel de juiste chaperonne ontmoeten.
Waarom deze verborgen organisatie van belang is voor gezondheid en ziekte
Door te onthullen dat R2TP en HSP90 niet alleen fragiele eiwitdelen beschermen maar ook vormgeven waar en hoe ze worden vertaald, legt deze studie een onverwachte laag van intracellulaire organisatie bloot. Het cha-cha-mechanisme helpt verklaren hoe cellen betrouwbaar enorme moleculaire complexen opbouwen, ook al delen de boodschappen voor hun onderdelen zelden hetzelfde adres. Het verklaart ook waarom defecten in chaperonnes of hun energiestromen vitale machines zoals RNA-polymerase en splicingfactoren kunnen destabiliseren, met gevolgen variërend van ontwikkelingsstoornissen tot kanker. In wezen laat het werk zien dat cellen vertrouwen op dynamische chaperonne-“fabrieken” om vers gemaakte onderdelen naar de juiste assemblages te leiden, waarmee hun interne machines efficiënt en ordelijk blijven.
Bronvermelding: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Trefwoorden: eiwit-chaperonnes, co-translatie-assemblage, moleculaire machines, RNA-polymerase, cellulaire kwaliteitscontrole