Clear Sky Science · nl
ProteoAutoNet: hoogdoorvoerende co-geëluëerde proteïneanalyse met robotica en machine learning
Waarom het begrijpen van samenwerkingen tussen eiwitten belangrijk is
In elke cel werken eiwitten zelden alleen. Ze vormen wisselende samenwerkingen om structuren te bouwen, DNA te kopiëren, beschadigde onderdelen te verwijderen en groei te ondersteunen. Veel vormen van kanker kapen deze partnerschappen, maar ze gedetailleerd in kaart brengen is traag en arbeidsintensief geweest. Deze studie introduceert ProteoAutoNet, een door robotica en machine learning aangedreven systeem dat sterk versnelt hoe wetenschappers eiwitpartnerschappen in cellen ontdekken, en laat zien hoe deze aanpak verborgen zwakke plekken in schildklierkankers kan onthullen.
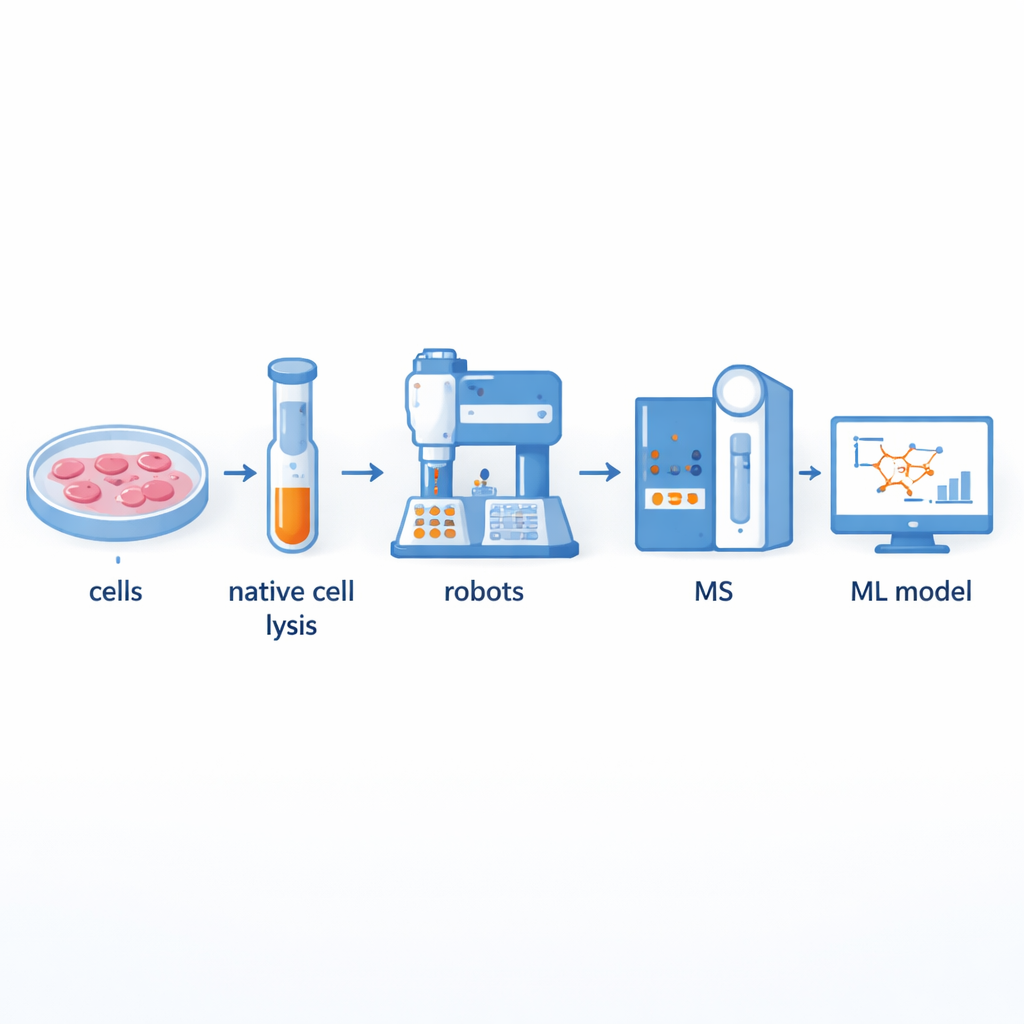
Het bouwen van een snellere fabriek voor eiwitpartnerschappen
Traditioneel gebruiken onderzoekers een methode die co-fractionatie massaspectrometrie heet om grote eiwitcomplexen te scheiden en vervolgens hun componenten te identificeren. Hoewel krachtig is deze aanpak arbeidsintensief en laagdoorvoer: honderden fracties met de hand voorbereiden kan dagen duren. De auteurs bouwden een door robotica ondersteund platform dat het grootste deel van deze workflow automatiseert. Celinhoud wordt eerst zachtjes geopend zodat natuurlijke eiwitcomplexen intact blijven, daarna door kolommen gescheiden op grootte om tientallen fracties te verkrijgen. Vloeistofhanteringsrobots en robotarmen nemen het daarna over: ze voegen reagentia toe, verteren eiwitten tot kleinere stukken, reinigen monsters en leveren ze aan een massaspectrometer voor meting. Deze opzet kan tot 540 fracties van meerdere schildkliercellijnen in slechts twee tot drie dagen verwerken, wat de doorvoer ongeveer verdubbelt ten opzichte van eerdere semi-geautomatiseerde systemen.
Robots die niet alleen sneller zijn, maar ook betrouwbaarder
Snelheid alleen is niet genoeg als de resultaten luidruchtig of inconsistent zijn. Het team controleerde zorgvuldig of de robotpipeline de kwaliteit van traditionele handmatige verwerking evenaart of overtreft. Met kwaliteitscontrolesmonsters lieten ze zien dat het geautomatiseerde systeem herhaaldelijk bijna 3.000 eiwitten per schildkliercellijn identificeerde met zeer grote overlap tussen replicaten en sterke overeenstemming in gemeten eiwithoeveelheden. Bij een directe vergelijking van robot- en handmatige verwerking van dezelfde monsters detecteerden beide benaderingen soortgelijke aantallen eiwitten, maar de robotmethode liet iets minder variatie in tellingen en stabielere eiwitabundantiemetingen zien. Dit betekent dat het nieuwe platform niet alleen tijd en arbeid bespaart, maar ook meer reproduceerbare experimenten ondersteunt — een cruciale eis voor grootschalige studies en klinische toepassingen.
Computers leren betekenisvolle verbanden herkennen
Zelfs met snelle instrumenten blijft een centrale uitdaging: besluiten welke eiwitten echt met elkaar interacteren en welke slechts toevallig samen voorkomen. Om dit aan te pakken combineerden de auteurs gecureerde eiwitcomplexdatabanken met een machine-learningmodel gebaseerd op het XGBoost-algoritme. Eerst schonken en voegden ze drie grote eiwitcomplexbronnen samen, resulterend in 96.635 bekende eiwit–eiwitinteracties. Ze gebruikten vervolgens profielen van hoe eiwitten over de fracties verschenen als invoerkenmerken en labelden paren als waarschijnlijke partners of niet-partners op basis van de databanken. Omdat echte, hoog-confidente partnerschappen relatief zeldzaam zijn, gebruikten ze een gerichte data-augmentatiestrategie: ze maakten veel licht gewijzigde versies van bekende positieve voorbeelden om het model te leren robuuste patronen te herkennen in plaats van specifieke sporen te memoriseren. Getraind op tientallen miljoenen van dergelijke voorbeelden uit drie schildkliercellijnen, behaalde het model sterke prestaties en rangschikte echte interacties duidelijk boven willekeur in zowel interne tests als in een onafhankelijke validatiecellijn.
Nieuwe inzichten in het celmachinerie van kanker
Met deze workflow brachten de onderzoekers netwerken van interacties in kaart in een normale schildkliercellijn en twee kankercellijnen: een papillaire schildkliercarcinoomlijn en een folliculaire carcinoomlijn die naar de longen kan uitzaaien. In deze cellen identificeerden ze meer dan 25.000 waarschijnlijke eiwitinteracties en vonden sterke signalen van bekende cellulaire machines zoals ribosomen (die eiwitten bouwen) en proteasomen (die eiwitten afbreken), wat bevestigt dat de methode gevestigde biologie teruggeeft. Door kankercellen met de normale lijn te vergelijken, ontdekten ze netwerken die in de ziekte versterkt waren. In de metastatische folliculaire carcinoomcellen waren zowel proteasoomcomponenten als een chaperoncomplex genaamd prefoldine veel meer verbonden en overvloedig. Verschillende prefoldinesubunits waren eerder aan andere kankers gekoppeld, maar grootschalige eiwitanalyses hadden hun gecoördineerde gedrag in schildklierkanker gemist, mogelijk omdat deze eiwitten strikt worden gereguleerd via afbraak. De co-fractionatiemethode bracht hun gecoördineerde veranderingen op complexniveau aan het licht.
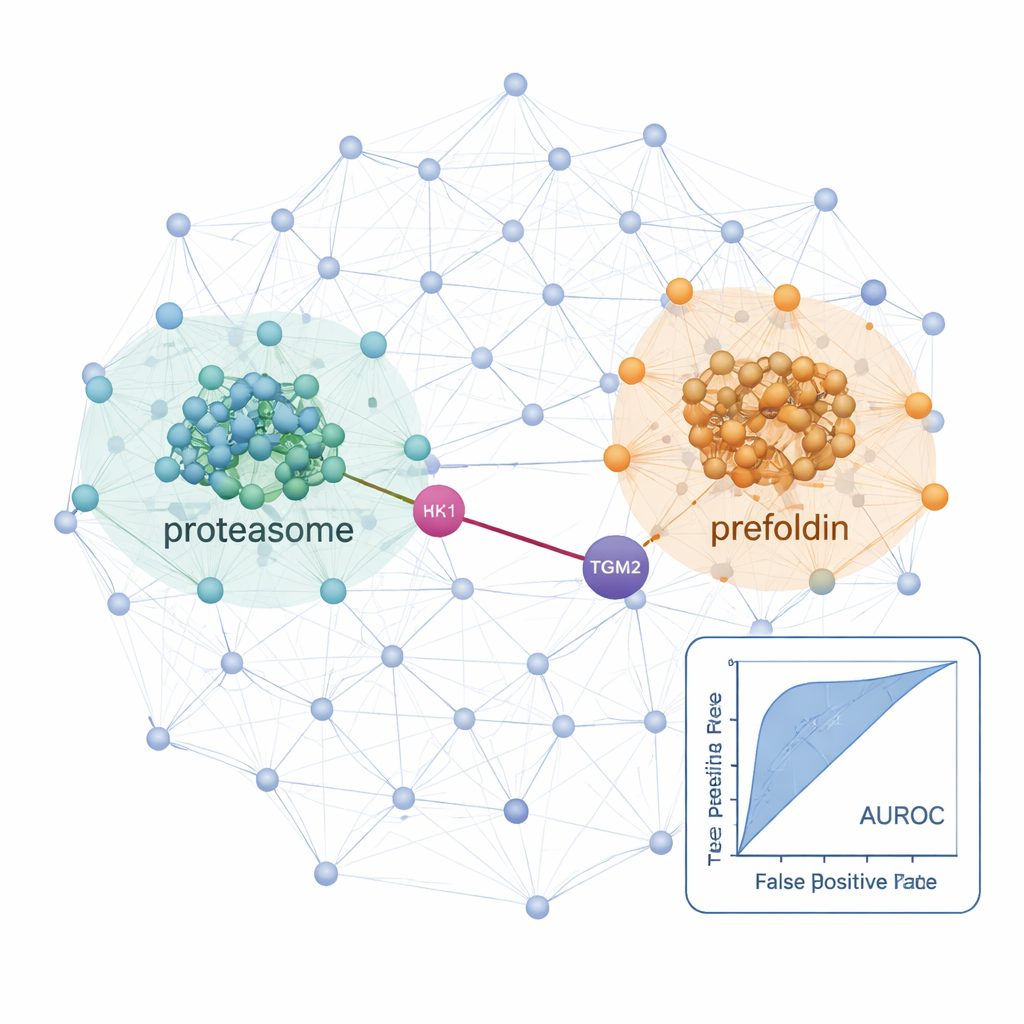
Verborgen verbindingen die toekomstige behandelingen kunnen sturen
De studie zette ook specifieke interacties in de schijnwerpers die van belang kunnen zijn voor hoe schildklierkankers groeien en uitzaaien. Een voorbeeld is een voorspelde partnerschap tussen HK1, een enzym dat de belangrijkste suikerverbrandingsroute van de cel start, en TGM2, een eiwit dat bekendstaat om invasie en metastase in schildkliertumoren te bevorderen. Deze HK1–TGM2-verbinding, afwezig in bestaande interactiedatabanken, werd ondersteund door structurele modellering en leek bijzonder actief in de papillaire carcinoomlijn, wat suggereert dat metabole herprogrammering en invasief gedrag fysiek verbonden kunnen zijn. Samengenomen laat ProteoAutoNet zien hoe het combineren van robotica en machine learning langzaam, door experts uitgevoerde kaartwerk van eiwitnetwerken kan opschalen. Voor niet-specialisten is de kernboodschap dat deze technologie zowel brede verschuivingen in cellulaire machinerie als onverwachte eiwitpartnerschappen kan onthullen die mogelijk op termijn artsen helpen beter te voorspellen welke schildklierkankers agressief zullen zijn en nieuwe therapeutische doelen kunnen aandragen.
Bronvermelding: Lyu, M., Hu, P., Zhang, G. et al. ProteoAutoNet: high-throughput co-eluted protein analysis with robotics and machine learning. Nat Commun 17, 1949 (2026). https://doi.org/10.1038/s41467-026-68686-9
Trefwoorden: proteïne-interacties, massaspectrometrie, machine learning in de biologie, schildklierkanker, proteasoom en prefoldine