Clear Sky Science · nl
Differentiële verstoring van membraanlipiden door lipopeptide-antibiotica, colistine en turnercyclamycines
Waarom dit ertoe doet voor toekomstige antibiotica
Men verwacht dat tegen het midden van deze eeuw drugresistente infecties jaarlijks tientallen miljoenen mensen zullen doden; enkele van de dodelijkste veroorzakers zijn Gram-negatieve bacteriën die al vele antibiotica negeren. Colistine is een van de weinige resterende geneesmiddelen die deze infecties nog kan behandelen, maar het is zwaar voor patiënten en bacteriën leren er in toenemende mate aan te ontsnappen. Deze studie ontleedt hoe colistine werkt in vergelijking met een nieuwe familie van natuurlijke antibiotica, de turnercyclamycines, en laat zien dat kleine chemische aanpassingen tot zeer uiteenlopende manieren van bacteriedoding kunnen leiden — en mogelijk tot veiliger geneesmiddelen.
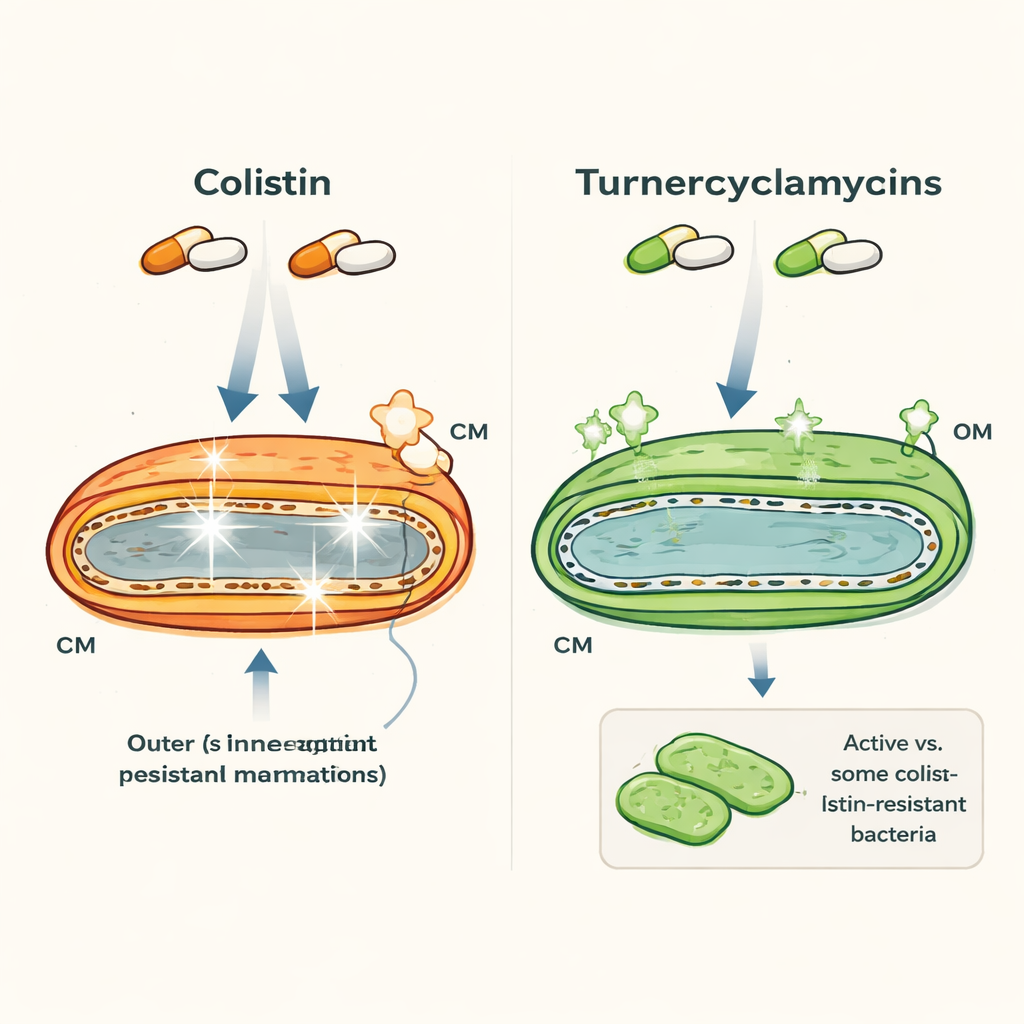
Twee uiterlijk vergelijkbare medicijnen met heel verschillend gedrag
Colistine en turnercyclamycines zijn beide lipopeptiden — moleculen die een vetstaart combineren met een peptidenring — en beide zijn gericht tegen Gram-negatieve bacteriën zoals Escherichia coli en Acinetobacter. Op het eerste gezicht lijken ze op elkaar, maar hun eigenschappen lopen sterk uiteen. Colistine is een laatste redmiddel dat snel werkt maar de menselijke nieren en zenuwen kan beschadigen, en bacteriën dragen steeds vaker resistentiegenen zoals mcr-1. Turnercyclamycines, ontdekt bij bacteriën die met schelpdieren geassocieerd zijn, kunnen veel van dezelfde ziekteverwekkers doden, waaronder sommige colistine-resistente stammen, maar vertonen veel minder toxiciteit in laboratoriumtests. Intrigerend is dat twee versies die alleen van elkaar verschillen door een kleine verlenging van de vetstaart al verschillende resistentiepatronen laten zien, wat suggereert dat zeer subtiele structurele kenmerken van belang zijn.
Hoe colistine gaten slaat en turnercyclamycines geduldig te werk gaan
De auteurs gebruikten fluorescerende kleurstoffen, time-kill-experimenten en elektronenmicroscopie om te volgen hoe deze middelen de bacteriële membranen in de tijd beïnvloeden. Colistine maakt zowel het buitenste membraan als het binnenste, cytoplasmatische membraan snel lekkend, wat binnen enkele uren tot snelle celdoding leidt. Turnercyclamycines doden daarentegen langzamer — het duurt 6 tot 10 uur voordat culturen volledig geruimd zijn — en verstoren vooral het buitenste membraan. Kleurstoffen die oplichten wanneer het binnenmembraan wordt doorbroken lieten sterke signalen zien bij colistine maar slechts bescheiden, vertraagde signalen bij turnercyclamycines, en hoogresolutiebeelden bevestigden weinig zichtbaar letsel aan het binnenmembraan, zelfs wanneer cellen stierven. Dit wijst erop dat turnercyclamycines niet doden via de klassieke ’pore-forming’-route die door veel membraantargeting-antibiotica wordt gebruikt.
Lipide bouwstenen als verborgen regelknoppen
Beide familietypen medicijnen zijn uiteindelijk afhankelijk van een bacterieel bestanddeel dat lipopolysaccharide (LPS) wordt genoemd, dat in het binnenmembraan wordt opgebouwd en meestal naar het buitenoppervlak wordt geëxporteerd. Wanneer de onderzoekers vroege stappen van de LPS-biosynthese uitschakelden, verloren zowel colistine als turnercyclamycines hun werkzaamheid; maar wanneer ze de transportmachinerie waarmee LPS naar buiten wordt verplaatst blokkeerden, bleven de middelen werken. Dit betekent dat het bestaan van LPS-bouwstenen essentieel is, maar hun uiteindelijke bestemming niet. Een belangrijk verschil kwam naar voren bij directe bindingsmetingen: colistine kleeft aan gezuiverd LPS met micromolaire affiniteit, terwijl turnercyclamycines geen meetbare binding lieten zien. In plaats daarvan werden turnercyclamycines sterk beïnvloed door andere membraanlipiden. Bepaalde fosfolipiden, vooral fosfatidylglycerol, konden hun activiteit dempen of moduleren, en de middelen werden gemakkelijk gevangen door outer membrane vesicles — kleine lipidebellen die door bacteriën worden afgescheiden.
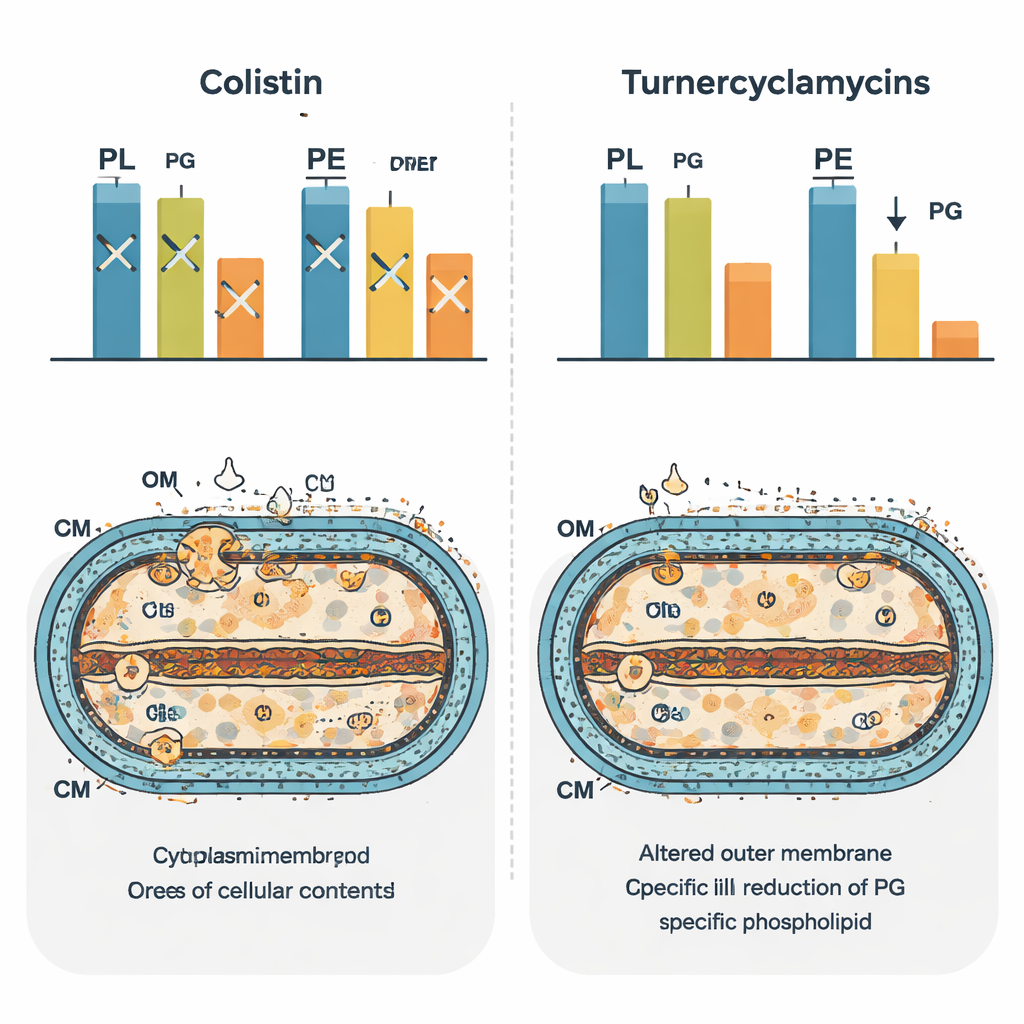
Het herschakelen van het bacteriële lipidenlandschap
Om het bredere effect op de cel te zien, gebruikte het team massa-spectrometrie-gebaseerde ‘fosfolipidomics’ om honderden lipidesoorten te catalogiseren na behandeling. Colistine produceerde een karakteristiek patroon van veranderingen, wat zijn brede verstoring van membraanhomöostase weerspiegelt. Turnercyclamycines gaven een ander handtekening die sterk leek op bacteriën die een lipide-transporterproteïne genaamd MlaA misten. In deze cellen waren bepaalde diacyllipiden uitgeput en namen monoacylvormen toe, wat suggereert dat de normale circulatie en remodellering van fosfolipiden tussen membranen uit balans was geraakt. Opmerkelijk was dat de niveaus van fosfatidylglycerol daalden in turnercyclamycin-behandelde cellen, wat het idee versterkt dat dit lipide direct verbonden is met hun potentie. De auteurs stellen voor dat turnercyclamycines kunnen fungeren als moleculaire mimics die de routes die vetzuur-, LPS- en fosfatidylglycerolsynthese of -transport koppelen, blokkeren.
Wat dit betekent voor het ontwerpen van betere geneesmiddelen
In eenvoudige bewoordingen toont de studie aan dat colistine doodt door snel beide beschermlagen van een Gram-negatieve bacterie open te scheuren, geholpen door sterke binding aan LPS, terwijl turnercyclamycines meer werken als saboteurs van de lipidenvoorraden van de cel. Ze glijden het buitenmembraan in, verstoren geleidelijk hoe specifieke lipiden worden gemaakt en gerecycled, en veroorzaken uiteindelijk het falen van de celomhulling — zonder het binnenmembraan zwaar te beschadigen. Omdat dit zachtere, meer gerichte mechanisme gekoppeld is aan lagere toxiciteit en een ander resistentieprofiel, biedt begrip ervan een routekaart voor het ontwerpen van volgende-generatie lipopeptide-antibiotica. Door kenmerken zoals de lengte en verzadiging van de vetstaart nauwkeurig af te stemmen, kunnen chemici mogelijk middelen bouwen die menselijk weefsel sparen, werkzaam blijven tegen colistine-resistente stammen en een stap voor blijven in de voortdurende wapenwedloop met antibioticaresistente bacteriën.
Bronvermelding: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Trefwoorden: antibioticaresistentie, Gram-negatieve bacteriën, colistine, lipopeptide-antibiotica, membraanlipiden