Clear Sky Science · nl
Structurele basis voor de dynamische conformaties van AP-4 en de associatie met ARF1
Hoe cellen hun lading sorteren en verzenden
Elke cel is een druk magazijn dat voortdurend duizenden eiwit-"pakketjes" sorteert en naar de juiste bestemmingen verzendt. Als dit bezorgsysteem bij zenuwcellen ontspoort, kan dat ernstige hersen- en bewegingsstoornissen veroorzaken. Deze studie onthult hoe één belangrijk transportsysteem, genaamd AP-4, van vorm verandert en samenwerkt met een regulatorisch eiwit, ARF1, om lading in kleine transportblaasjes te laden en waarom die flexibiliteit zo belangrijk is voor gezonde neuronen.
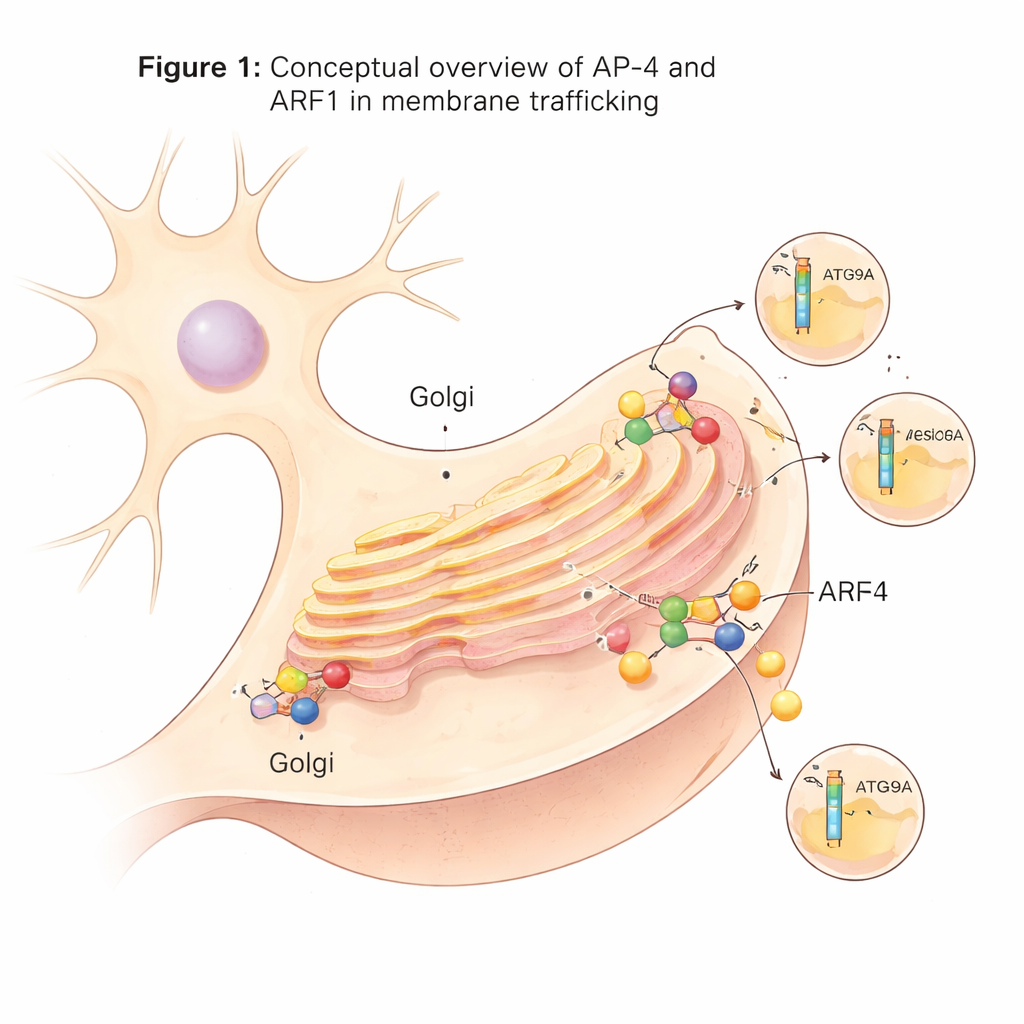
Een gespecialiseerd transportsysteem in zenuwcellen
In cellen ontstaan veel transportvesikels vanaf een centraal sorteerstation dat bekendstaat als het trans-Golgi-netwerk. Deze vesikels zijn afhankelijk van adaptor-eiwitcomplexen, of AP-complexen, die fungeren als laadperrons: ze herkennen cargoeiwitten en helpen bij het vormen van gecoate vesikels daaromheen. AP-4 is een van deze adaptoren en is bijzonder omdat het, in tegenstelling tot veel andere, niet het gebruikelijke skeleteiwit clathrine inzet. Hoewel AP-4 in veel weefsels voorkomt, speelt het een bijzonder belangrijke rol in neuronen. Als AP-4 bij mensen ontbreekt of defect is, slagen cruciale ladingen zoals het autophagie-gerelateerde eiwit ATG9A en bepaalde glutamaatreceptoren er niet in goed te verplaatsen, wat leidt tot een ernstige neuroontwikkelingsaandoening die bekendstaat als AP-4-deficiëntiesyndroom.
Een van vorm wisselend complex in rust
De auteurs gebruikten cryo-elektronenmicroscopie, een krachtige beeldvormingstechniek die grote eiwitassemblages in kaart kan brengen, om de driedimensionale structuur van het AP-4-"core"-complex in oplossing te bepalen. AP-4 bestaat uit vier subeenheden die samen een komachtige structuur vormen. Ze ontdekten dat AP-4 niet in één starre vorm zit. In plaats daarvan schakelt het van nature tussen een "gesloten" vorm, waarin een subeenheid (de C-terminale domein van de medium-subeenheid) in het midden van de kom is weggeborgen, en een "open" vorm, waarin dat deel naar buiten zwaait en zeer flexibel wordt. Aanvullende single-molecule fluorescentie-experimenten toonden aan dat deze subeenheid minstens drie posities inneemt—gesloten, gedeeltelijk open en volledig open—wat laat zien dat AP-4 van nature dynamisch is, zelfs vóórdat het aan membranen bindt.
De rol van ARF1: werver, geen hoofdschakelaar
Veel verwante adaptorcomplexen worden door binding van kleine regulatorische eiwitten, de ARF's, van een inactieve naar een actieve conformatie geschakeld. Om te onderzoeken hoe dit voor AP-4 werkt, losten de onderzoekers structuren op van AP-4 gebonden aan ARF1, een kleine GTP-bindende eiwit die zich aan membranen verankert. Ze vonden dat ARF1 zich voornamelijk hecht aan één van de grote AP-4-subeenheden nabij het N-terminus, op een manier die lijkt op andere AP-complexen. Verrassend genoeg veroorzaakt ARF1-binding geen ingrijpende structurele herschikking in AP-4. De gesloten en open vormen blijven naast elkaar bestaan en de algemene architectuur van het complex blijft grotendeels ongewijzigd. Biochemische testen bevestigden dat specifieke contactpunten tussen ARF1 en AP-4 essentieel zijn voor membraanrekrutering, maar ARF1 alleen vergrendelt AP-4 niet in één enkele actieve staat.
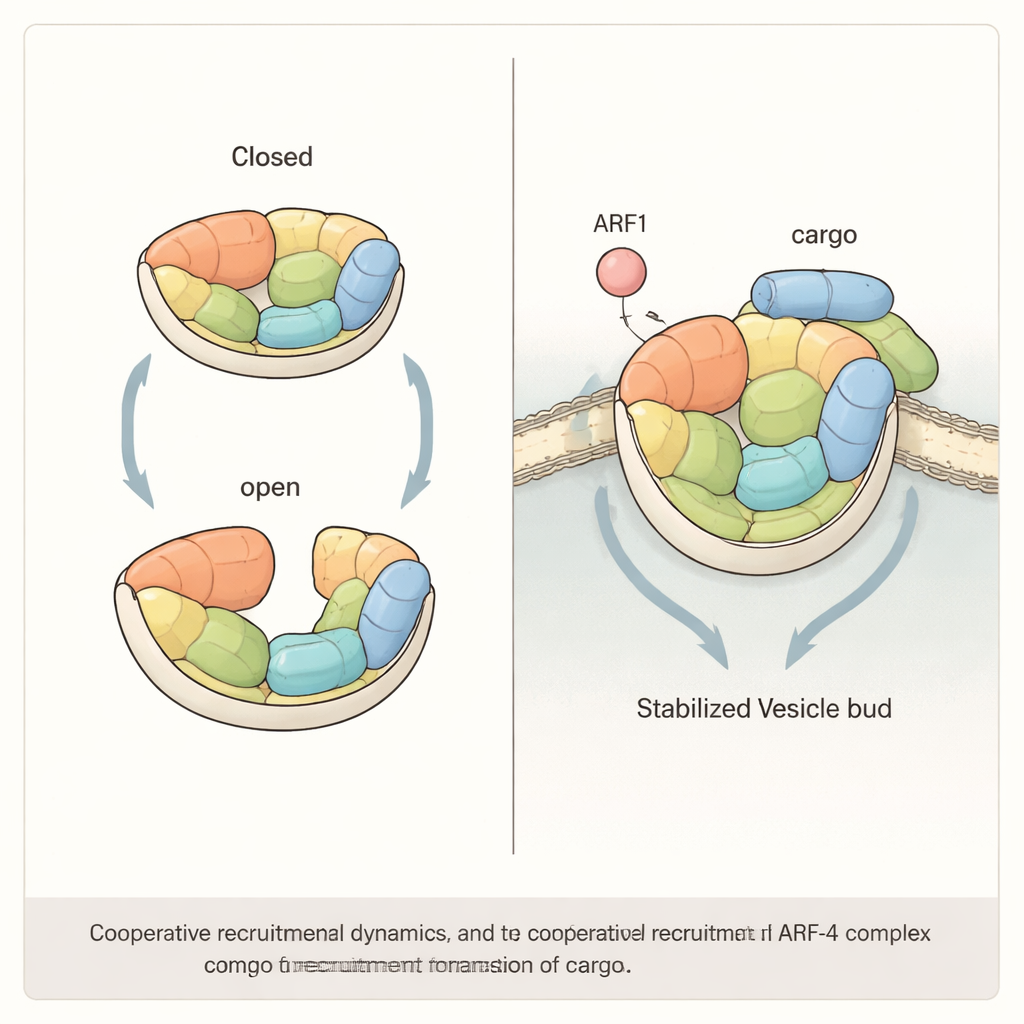
Samenwerking tussen regulator en lading
De studie laat verder zien dat efficiënte rekrutering van AP-4 naar membranen waarschijnlijk samenwerking vereist tussen ARF1 en de cargoeiwitten zelf. Door het systeem te reconstrueren op kunstmatige bolletjes en liposomen, vonden de auteurs dat óf ARF1 óf een korte staart van het cargo-eiwit ATG9A AP-4 kan aantrekken, maar wanneer beide samen aanwezig zijn, halen ze aanzienlijk meer AP-4 binnen dan je zou verwachten op basis van hun individuele effecten. Toen de onderzoekers mutaties inbrachten die AP-4 stijf maakten—waardoor het minder goed tussen open en gesloten toestanden kan schakelen—verdween dit synergetische effect. In menselijke cellen die een sleutel-subeenheid van AP-4 misten, faalde het herstel door alleen zulke "starre" gemuteerde versies van het complex om het normale verkeer van ATG9A vanaf het Golgi te herstellen, wat benadrukt dat de flexibiliteit van AP-4 geen curiositeit is maar een functionele vereiste.
Waarom flexibiliteit belangrijk is voor de gezondheid van de hersenen
Samengevat portretteert het werk AP-4 als een van vorm wisselende adaptor die meerdere conformaties in oplossing en op membranen uitprobeert. In plaats van als een aan/uit-schakelaar te fungeren, werkt ARF1 als een membraangebonden werver die samen met cargoeiwitten AP-4 helpt stabiliseren in productieve configuraties voor vesikelvorming. Het verstoren van dit evenwicht—door ARF1- of cargobinding te verzwakken of door AP-4 in één vorm te bevriezen—belemmert de export van lading uit het Golgi en kan bijdragen aan neuroontwikkelingsziekten. Door de structurele basis van AP-4’s dynamisch gedrag te onthullen, biedt deze studie een kader voor het begrijpen van AP-4-gerelateerde aandoeningen en wijst het op mogelijke strategieën om het juiste verkeer in aangetaste neuronen te herstellen.
Bronvermelding: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Trefwoorden: membraanvervoer, AP-4 adaptorcomplex, ARF1, vesikelvorming, neuroontwikkelingsstoornis