Clear Sky Science · nl
ZNF683+ NK-cellen bepalen chemotherapiegevoeligheid bij gevorderde HPSCC door het immuummicro-omgeving te hervormen
Waarom chemotherapie bij bepaalde keelkankers beter werkt
Mensen met gevorderde hypofaryngeale kanker — een tumor diep in de keel — ondergaan vaak zware chemotherapie met onzekere uitkomsten. Sommige tumoren slinken sterk, terwijl andere nauwelijks reageren. Deze studie stelt een eenvoudige maar cruciale vraag: wat is er anders in de tumoren die goed reageren? Door individuele immuuncellen één voor één te bestuderen, ontdekken de onderzoekers een bepaald type ‘beschermende’ cel die het verschil kan maken tussen slagen en falen van de standaardchemotherapie.
De uitdaging van een verborgen, moeilijk te behandelen kanker
Hypofaryngeaal plaveiselcelcarcinoom is een van de dodelijkste hoofd-halskankers, mede omdat het groeit in een krappe, lastig te onderzoeken regio en vroeg weinig klachten geeft. Veel patiënten worden laat gediagnosticeerd, wanneer de opties beperkt zijn en de vijfjaarsoverleving laag is. Een combinatiedosis bekend als TPF-chemotherapie wordt veel gebruikt omdat het de ziekte kan beheersen terwijl het strottenhoofd zoveel mogelijk behouden blijft. Toch tonen 10–20 procent van de patiënten weinig of geen respons, waardoor kostbare tijd verloren gaat. Traditionele genetische tests, die signalen over miljoenen cellen middelen, hebben moeite gehad dit verschil te verklaren, waardoor de auteurs zich richtten op het levende ecosysteem van immuuncellen in de tumor.
Het immuunlandschap van de tumor cel voor cel lezen
De onderzoekers volgden 12 patiënten in de tijd, verzamelden tumormonsters vóór en na twee cycli TPF-chemotherapie en profilen meer dan 150.000 immuuncellen op single-cell resolutie. Ze onderzochten ook nog eens 41 extra patiënten om belangrijke bevindingen te bevestigen met beeldvorming en flowcytometrie. Door de genactiviteit en het celtype van elke cel in kaart te brengen, bouwden ze een gedetailleerde atlas van het tumormicro-omgeving: T-cellen, B-cellen, macrofagen, dendritische cellen, mestcellen, neutrofielen en natural killer (NK)-cellen. Onder al deze spelers viel één patroon op. Voor de behandeling hadden tumoren die later afnamen veel meer NK-cellen dan die resistent waren tegen therapie, en hoe groter het aandeel NK-cellen, hoe meer de tumor uiteindelijk slonk.
Een speciale NK-celsubset bereidt T-cellen voor op succes
Dieper gravend verdeelde het team NK-cellen in drie groepen op basis van hun moleculaire kenmerken. Slechts één van deze groepen, gekenmerkt door de transcriptiefactor ZNF683 en grotendeels aanwezig in het weefsel rondom tumorclusters, correleerde sterk met een goede chemotherapie-respons. Patiënten waarvan de tumoren bij baseline meer van deze ZNF683+ NK-cellen bevatten, profiteerden veel waarschijnlijker van TPF. In muisexperimenten maakte het verwijderen van NK-cellen bijna volledig een einde aan het voordeel van chemotherapie, wat bevestigt dat NK-activiteit niet alleen een merker is maar een vereiste voor effectieve behandeling. Intrigerend genoeg fungeerden deze NK-cellen niet louter als directe kankerdoders; hun genprogramma’s waren verrijkt voor het begeleiden en activeren van T-cellen.
Hoe NK-cellen krachtige tumordodende T-cellen vrijspelen
Om te begrijpen welke T-cellen het meest van belang waren, volgden de wetenschappers individuele T-celreceptorclonen vóór en na behandeling. Ze vonden dat bij responders een specifieke groep CD8 “effector memory”-T-cellen, verrijkt voor een molecule genaamd GZMK, dramatisch uitgroeide na chemotherapie. Deze T-cellen produceerden hoge niveaus van de toxische cytokinen TNF en interferon-gamma zonder tekenen van diepe uitputting, waardoor ze krachtige, duurzame moordenaars waren. Ruimtelijke beeldvorming liet zien dat deze GZMK+ CD8 T-cellen na de behandeling sterk clusteren in tumoren van responders maar niet in die van non-responders. In kweektests met menselijke cellen dreef direct contact met ZNF683+ NK-cellen de expansie van deze GZMK+ CD8 T-celsubset aan, een effect dat verdween wanneer de cellen door een barrière gescheiden werden.
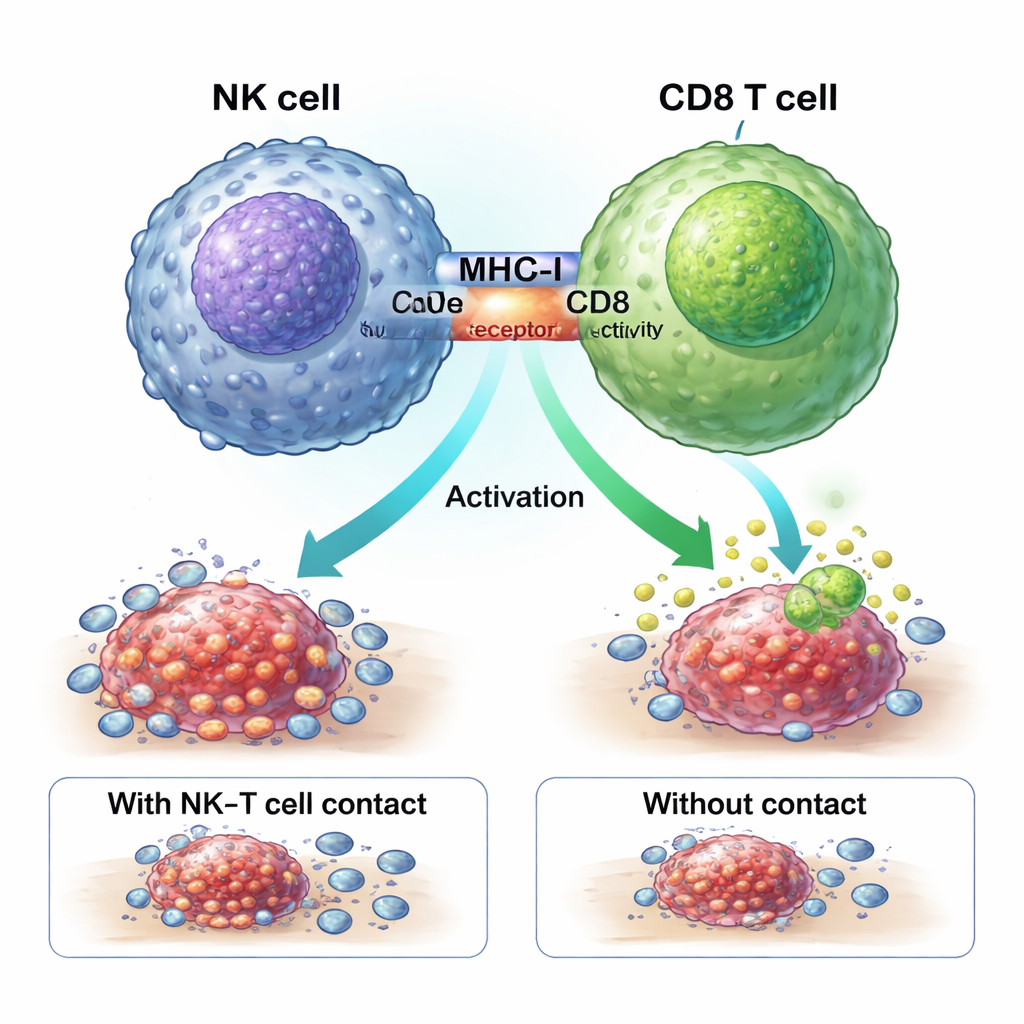
Een fysieke handdruk die tumorvechters activeert
De studie toont aan dat ZNF683+ NK-cellen de chemotherapie-respons versterken via een fysieke “handdruk” met CD8 T-cellen. Moleculen genaamd MHC-I op het NK-celoppervlak binden CD8-receptoren op T-cellen in een zone van nauwe interactie, een immuunsynaps. Het blokkeren van MHC-I verhinderde dat NK-cellen de krachtige GZMK+ CD8 T-cellen genereerden. In speciaal gemaakte muismodellen die ZNF683 alleen in NK-cellen misten, uitten deze NK-cellen minder MHC-I en waren ze veel minder effectief in het activeren van CD8 T-cellen, wat het idee versterkt dat ZNF683 NK-cellen programmeert tot effectieve coaches voor T-celstrijders in plaats van simpele uitvoerders.
Wat dit betekent voor patiënten
Voor niet-specialisten is de kernboodschap dat niet alle immuuncellen in een tumor gelijk zijn. Dit werk identificeert een specifieke NK-celsubset als verkenner die het slagveld voorbereidt voordat de chemotherapie begint. Tumoren rijk aan deze cellen zijn klaar om golven van sterke CD8 T-cellen los te laten zodra de medicijnen ingrijpen, wat leidt tot veel grotere terugval. Het meten van de hoeveelheid van deze NK–T-celasas voor de behandeling zou artsen kunnen helpen voorspellen wie baat heeft bij TPF-chemotherapie en wie mogelijk alternatieve of aanvullende therapieën nodig heeft. In de toekomst zouden behandelingen die deze ZNF683+ NK-cellen versterken of nabootsen resistente hypofaryngeale kankers omvormen tot tumoren die veel gevoeliger zijn voor standaardchemotherapie.
Bronvermelding: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Trefwoorden: hypofaryngeale kanker, chemotherapie resistentie, natural killer-cellen, tumor immuunmicro-omgeving, CD8 T-cellen