Clear Sky Science · nl
Foto-geïnduceerde selectieve N–N-bindingconstructie via het benutten van nitreenafgifte en -overdracht
Een nieuwe manier om stikstofatomen met licht te verbinden
Stikstofatomen vormen de kern van veel geneesmiddelen, gewasbeschermingsmiddelen en geavanceerde materialen. Chemici zijn erg bedreven in het binden van stikstof aan koolstof, maar het direct verbinden van twee stikstofatomen is veel lastiger. Deze studie introduceert een lichtgedreven, metaalvrije methode om stikstofatomen gecontroleerd aan elkaar te koppelen, wat een eenvoudiger route opent naar een breed scala nuttige moleculen.
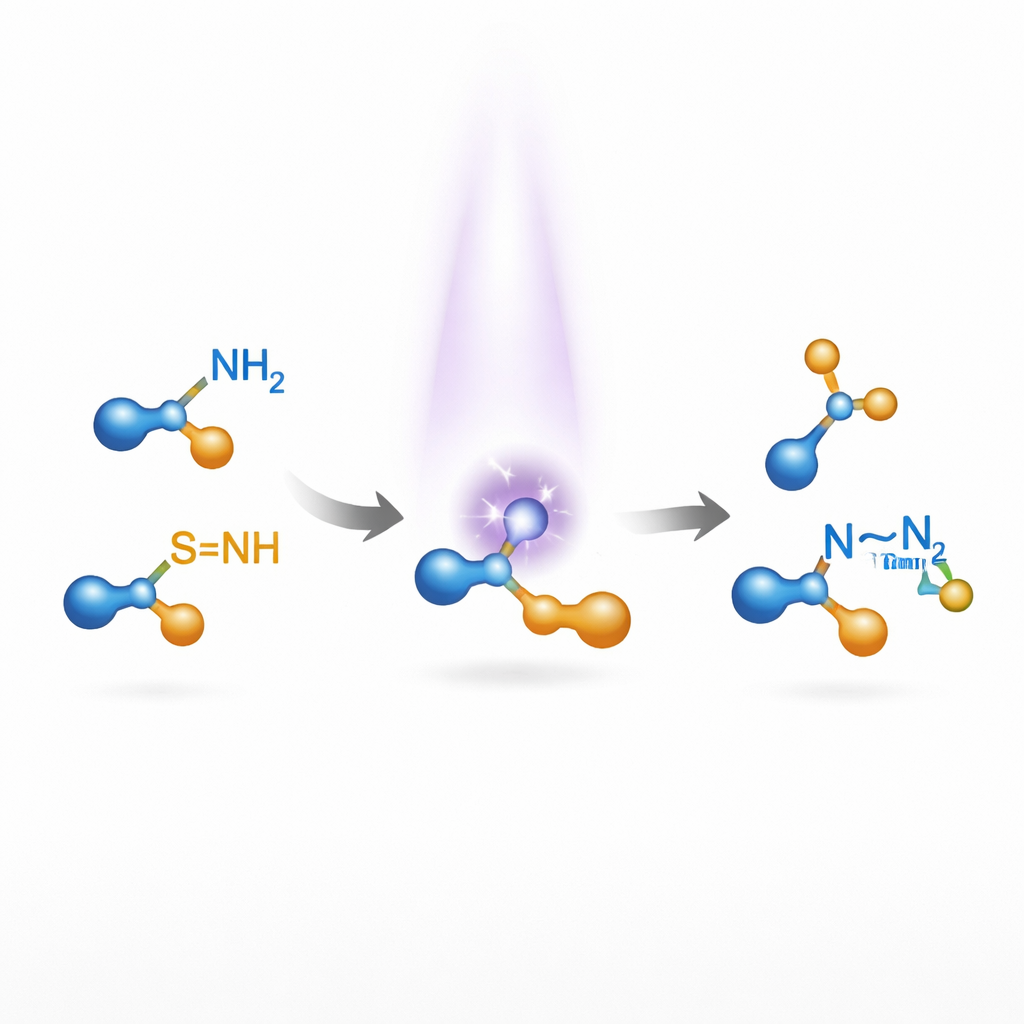
Waarom het verbinden van stikstof met stikstof moeilijk is
Veel natuurlijke producten en geneesmiddelen bevatten paren van aan elkaar gebonden stikstofatomen, een motief dat het gedrag van een molecuul in het lichaam of in materialen kan afstemmen. Bestaande manieren om deze N–N-eenheden te bouwen beginnen meestal met kant-en-klare stikstof–stikstoffragmenten, zoals hydrazines of diazoverbindingen, en worden stap voor stap aangepast. Het direct smeden van de N–N-binding uit eenvoudige aminen is aantrekkelijk maar moeilijk: stikstof is vrij elektronegatief, waardoor twee stikstofatomen niet vanzelf een stabiele, niet-polaire binding vormen. Eerdere successen leunden sterk op overgansmetaal-katalysatoren en werken vaak alleen voor smalle families van moleculen, wat hun bruikbaarheid in ontdekkingschemie beperkt.
Licht gebruiken om een reactieve tussenpersoon te temmen
De auteurs richtten zich op nitreen—zeer reactieve, kortlevende stikstofsoorten die in principe in andere bindingen kunnen inserteren. Traditionele nitreenchemie vereist doorgaans metaal-katalysatoren en kan lijden onder nevenreacties omdat nitreenen zo energiek zijn. Het team vroeg zich af of ze nitreenen op een zachtere, beter controleerbare manier konden genereren met licht, zonder metalen, en deze vervolgens konden gebruiken om eenvoudige aminen tot N–N–bevattende producten te koppelen. Hun sleutelidee was het gebruik van sulfilimines, een familie moleculen die gemakkelijk aan te passen is en ultraviolet en nabij-zichtbaar licht absorbeert. Onder belichting kunnen deze sulfilimines splitsen op een manier die een nitreenfragment vrijmaakt terwijl een onschadelijk zwavelhoudend bijproduct wordt teruggevormd.
Een brede, metaalvrije receptuur voor stikstofparen
Na systematisch testen identificeerden de onderzoekers een specifiek sulfilimine dat onder 365-nanometer licht in chloroform efficiënt reageert met veel aminen om hydrazideproducten te geven—moleculen met een pasgevormde N–N-binding naast een carbonylgroep. Ze optimaliseerden factoren zoals de structuur van het sulfilimine, het oplosmiddel en de lichtintensiteit om het gewenste product te bevorderen boven gebruikelijke bijproducten zoals ureumverbindingen. Onder deze milde omstandigheden koppelden veel verschillende aminen, waaronder aromatische en alifatische types en cyclische varianten, succesvol. Ze toonden ook aan dat vele verschillende sulfilimines, met zowel aromatische als alifatische acylgroepen en sulfonylgroepen, goed meewerken en tientallen uiteenlopende N–N-bevattende producten opleveren. Belangrijk is dat de methode laat in een synthese kan worden toegepast om complexe, biologisch actieve moleculen zoals veelgebruikte ontstekingsremmers en chiraal bouwstenen te modificeren, wat de praktische waarde voor geneesmiddelen- en materialensynthese aantoont.
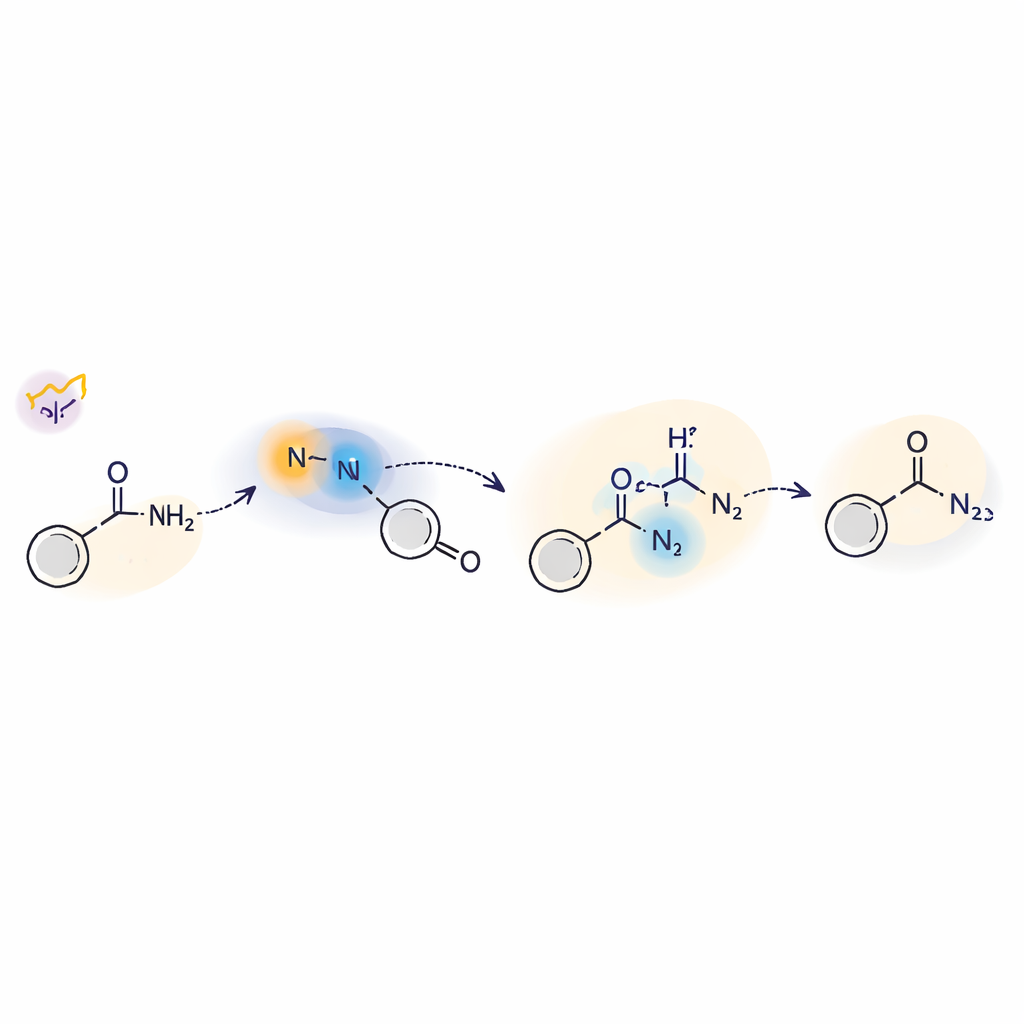
Een blik onder de motorkap van de lichtgestuurde stap
Om te begrijpen hoe deze lichtgestuurde chemie werkt, combineerde het team experimenten en theorie. Ze gebruikten radicaalvangers, isotopenlabeling en elektronparamagnetische resonantie om aan te tonen dat vrije nitreenintermediairen en stikstofgecentreerde radicalen tijdens de reactie optreden. Tijdsgelimiteerde laserspectroscopie toonde twee belangrijke vormen van het nitreen: een kortlevende triplettoestand en een langerlevende singlettoestand. De singletvorm reageert direct met aminen via een soort nucleofiele aanval, terwijl de triplet kan deelnemen aan waterstofatoomoverdrachtstappen. Computationale berekeningen ondersteunden een mechanisme waarbij licht het sulfilimine exciteert, de zwavel–stikstofbinding splijt, en het resulterende nitreen vervolgens het amine via zowel singlet- als tripletroutes betrekt voordat het zich vestigt in de uiteindelijke hydrazidestructuur.
Wat dit betekent voor toekomstige moleculen
Dit werk toont dat zorgvuldig ontworpen sulfilimines kunnen fungeren als “nitreenreservoirs” die reactieve stikstofeenheden op verzoek vrijgeven onder licht, zonder hulp van metalen. Door zowel de singlet- als tripleteigenschappen van nitreenen te benutten terwijl hun concentratie laag wordt gehouden, bereikt de methode selectieve vorming van N–N-bindingen over een breed scala bouwstenen. Voor niet-specialisten is de kernboodschap dat chemici nu een eenvoudiger, schoner en flexibeler manier hebben om stikstofatomen aan elkaar te rijgen, wat de ontwikkeling van nieuwe geneesmiddelen, agrochemicaliën en stikstofrijke materialen kan versnellen.
Bronvermelding: Yu, M., Feng, J., Wang, X. et al. Photo-induced selective N-N bond construction via harnessing nitrene release and transfer. Nat Commun 17, 2084 (2026). https://doi.org/10.1038/s41467-026-68674-z
Trefwoorden: nitreenchemie, foto-geïnduceerde reacties, N–N-bindingsvorming, sulfilimines, hydraziden