Clear Sky Science · nl
Regulatie van AP1-adaptorassemblage door de tweehandige chaperonne MEA1
Waarom deze verborgen celhulp belangrijk is
In elke menselijke cel vervoeren duizenden kleine pakketjes eiwitten naar de plek waar ze nodig zijn of naar het cellulaire “recyclingcentrum” voor afbraak. Dit verkeer houdt onze cellen gezond en onze immuunverdediging in evenwicht. Het hier samengevatte artikel onthult een voorheen mysterieuze eiwit, MEA1 genoemd, dat essentieel blijkt voor de opbouw van een van de sleutelmachines die deze pakketjes inladen. Begrijpen hoe MEA1 werkt helpt verklaren hoe cellen belangrijke ladingen reguleren, waaronder moleculen die antivirale immuunreacties aan- en uitzetten.
Verkeersleiding in het celverzendpunt
Een groot deel van het celverkeer loopt via een structuur die het Golgi-apparaat heet, een stapel afgeplatte sacculi die fungeert als een centraal postkantoor. Vanuit het Golgi kan lading naar het celoppervlak worden gestuurd of worden omgeleid naar interne compartimenten voor afbraak. Een eiwitcomplex dat AP1 heet, staat centraal in deze route. AP1 herkent labels op ladingseiwitten, helpt het membraan te buigen en werft een buitenlaag van clathrine aan om kleine transportvesikels te vormen. Zonder correct geassembleerd AP1 hopen cruciale ladingen zich op de verkeerde plekken op en kunnen normale signaalroutes, waaronder die gekoppeld aan immuniteit, verstoord raken. 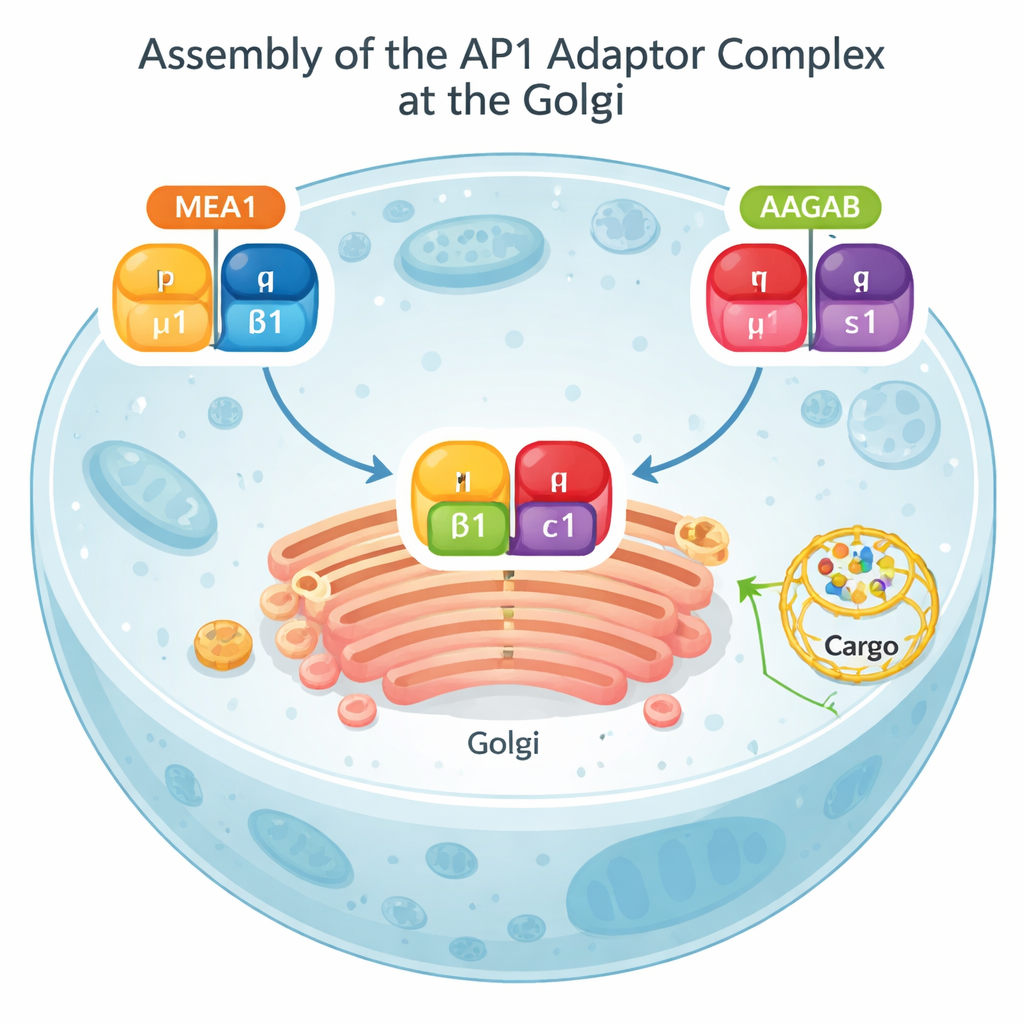
Een ontbrekende assemblagewerker vinden
De auteurs wilden eiwitten identificeren die fysiek met AP1 geassocieerd zijn en mogelijk helpen bij de assemblage. Ze doorzochten een grote eiwit–interactie-database, filterden kandidaten weg die onwaarschijnlijk met AP1 zouden samenwerken, en gebruikten vervolgens een kunstmatig-intelligentiehulpmiddel, AlphaFold, om te voorspellen hoe de overgebleven eiwitten contact zouden maken met individuele delen van AP1. Deze zoektocht bracht MEA1 naar voren, een klein en eerder onbeschreven eiwit dat in veel weefsels voorkomt. Vervolgexperimenten in menselijke cellijnen bevestigden dat MEA1 bindt aan twee specifieke AP1-subunits, bekend als μ1 en β1, zowel wanneer ze afzonderlijk getest werden als in hun natuurlijke, onveranderde vormen.
MEA1 houdt AP1 intact en houdt het celverkeer gaande
Om te onderzoeken wat MEA1 precies doet, verwijderden de onderzoekers het MEA1-gen in menselijke cellijnen. Wanneer MEA1 ontbrak, waren alle vier onderdelen van AP1 sterk verminderd en verdwenen de karakteristieke AP1-plekjes nabij het Golgi vrijwel. Dit verlies had duidelijke functionele gevolgen. Eén AP1-lading, de folaatreceptor FOLR1, stapelde zich op aan het celoppervlak in plaats van naar binnen te worden gestuurd, een teken van defect AP1-sorteren. Een andere lading, het immuunsignalerende eiwit STING, werd niet langer efficiënt ingepakt in vesikels die naar lysosomen, de recyclingcentra van de cel, gingen. Daardoor bleven geactiveerde STING en de bijbehorende kinase TBK1 langdurig op hoge niveaus aanwezig, wat aangeeft dat de ‘uitknop’ voor dit antivirale pad niet goed functioneerde. Herintroductie van MEA1 herstelde de AP1-niveaus en corrigeerde deze transportdefecten.
Een tweehandige chaperonne en een botsingsgebaseerd bouwproces
Biochemische testen en AlphaFold-modellen toonden aan dat MEA1 zich gedraagt als een “tweehandige” assemblagechaperonne: het voorste deel pakt de μ1-subunit vast, terwijl het achterste deel β1 vastgrijpt. Op zichzelf zijn μ1 en β1 onstabiel en hebben ze de neiging te klonteren of afgebroken te worden; wanneer ze aan MEA1 gebonden zijn, worden ze oplosbaar en klaar om te assembleren. Een andere bekende chaperonne, AAGAB, vervult een parallelle rol voor de overige twee AP1-subunits, γ en σ1. Wanneer MEA1–μ1–β1 en AAGAB–γ–σ1-complexen elkaar ontmoeten, combineren hun subunits tot een compleet, vierdelig AP1-adaptor. Op dat moment laten beide chaperonnes los en keren terug naar het celvocht, terwijl het nieuwgevormde AP1 naar membranen gaat om zijn sorteertaak uit te voeren. Dit “dual-chaperone collision”-mechanisme toont aan dat de AP1-assemblage zorgvuldig wordt georkestreerd in plaats van aan toevallige ontmoetingen te worden overgelaten.
Breder inzicht in cellulaire kwaliteitscontrole
Buiten AP1 suggereert de studie een algemenere strategie die cellen mogelijk gebruiken om veel grote eiwitmachines te bouwen. MEA1 kan ook zwak assisteren bij een ander adaptorcomplex, AP2, en samen met AAGAB en een derde chaperonne genaamd CCDC32 illustreert het een breder pad dat de auteurs “Chaperone-assisted Adaptor Protein Assembly” noemen. In dit schema stabiliseren gespecialiseerde chaperonnes kwetsbare subunits, brengen ze de juiste paren samen en blokkeren ze tijdelijk de cargo-bindingsplaatsen totdat het complex volledig gevormd en veilig inzetbaar is. 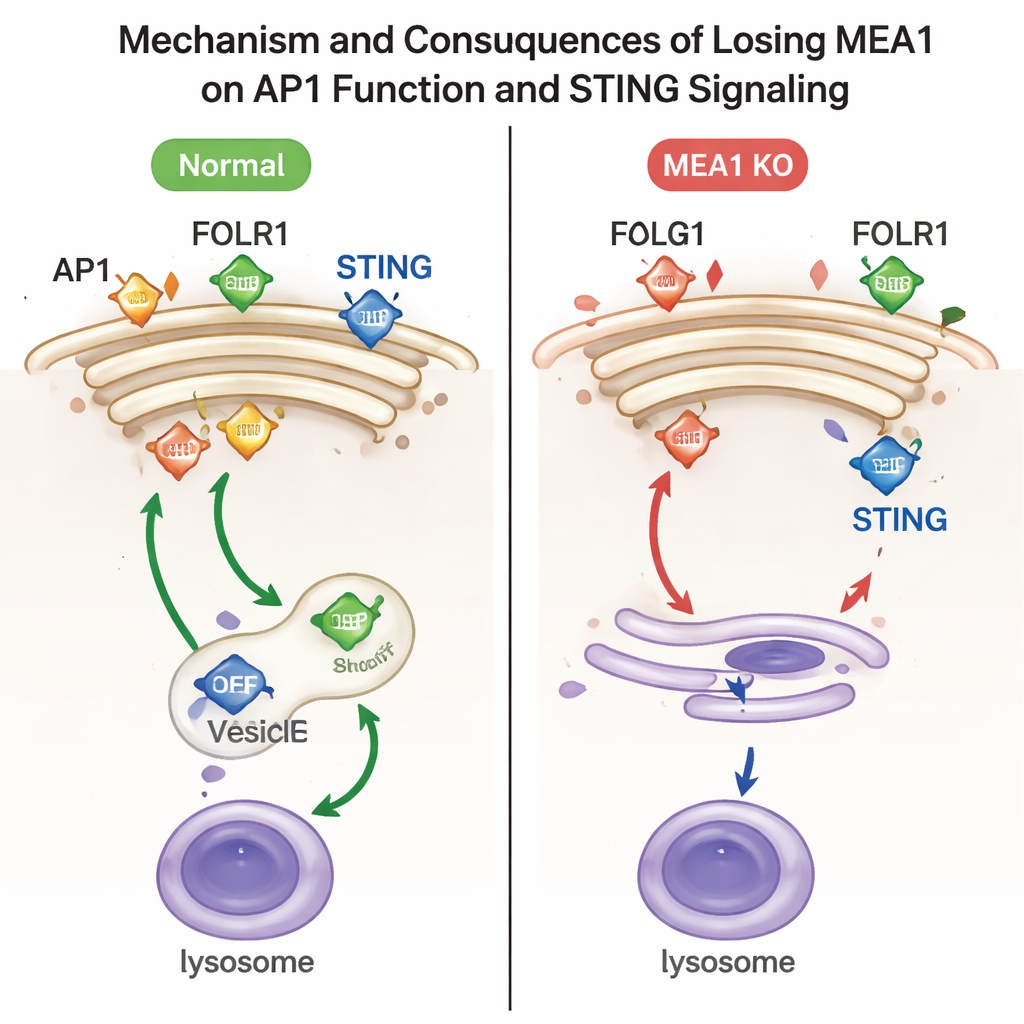
Wat dit betekent voor gezondheid en ziekte
Voor niet-specialisten is de belangrijkste conclusie dat MEA1 een cruciale achter-de-schermenwerker is die helpt bij de assemblage van AP1, een kernsorteringsmachine in onze cellen. Wanneer MEA1 ontbreekt, valt AP1 uit elkaar, ontstaan er verkeersopstoppingen en worden belangrijke regelaars zoals STING niet adequaat uitgeschakeld. Deze nieuwe kennis kan uiteindelijk helpen sommige immuunstoornissen of andere ziekten die samenhangen met foutief eiwitverkeer te verklaren, en het onthult een algemeen principe voor hoe cellen veilig complexe moleculaire machines bouwen uit onstabiele onderdelen.
Bronvermelding: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Trefwoorden: eiwittransport, adaptor-eiwit AP1, moleculaire chaperonnes, STING-signaleringspad, celbiologie