Clear Sky Science · nl
Moleculaire herkenning van thyreoglobuline door sortiline
Hoe schildkliercellen beslissen wanneer ze hormoon vrijgeven
Schildklierhormonen stellen als het ware onze metabole “thermostaat” af en beïnvloeden alles van hartslag tot lichaamstemperatuur. Deze hormonen worden opgebouwd en opgeslagen in een enorm eiwit genaamd thyreoglobuline. Deze studie onthult hoe een ander eiwit, sortiline, helpt bepalen welke vorm van thyreoglobuline schildkliercellen terug naar binnen halen zodat het hormoon in de bloedbaan kan worden vrijgegeven — een besluit dat uiteindelijk bepaalt hoeveel schildklierhormoon het lichaam te zien krijgt.
Een opslageiwit dat wacht om verwerkt te worden
Thyreoglobuline is een massief, Y‑vormig eiwit dat door schildkliercellen wordt geproduceerd en uitgescheiden in een gelachtige ruimte genaamd het colloïd. Daar fungeert het zowel als grondstof als opslagplaats voor schildklierhormoon: specifieke bouwstenen (aminozuren) binnen thyreoglobuline worden chemisch gejodeerd om schildklierhormonen te vormen, terwijl ze nog in het grotere eiwit ingebed zijn. Om deze hormonen daadwerkelijk vrij te maken, moet thyreoglobuline opnieuw in de cel worden opgenomen, binnen lysosomale afbraakcompartimenten worden gekapt, en moeten de hormoonfragmenten naar het bloed worden getransporteerd.
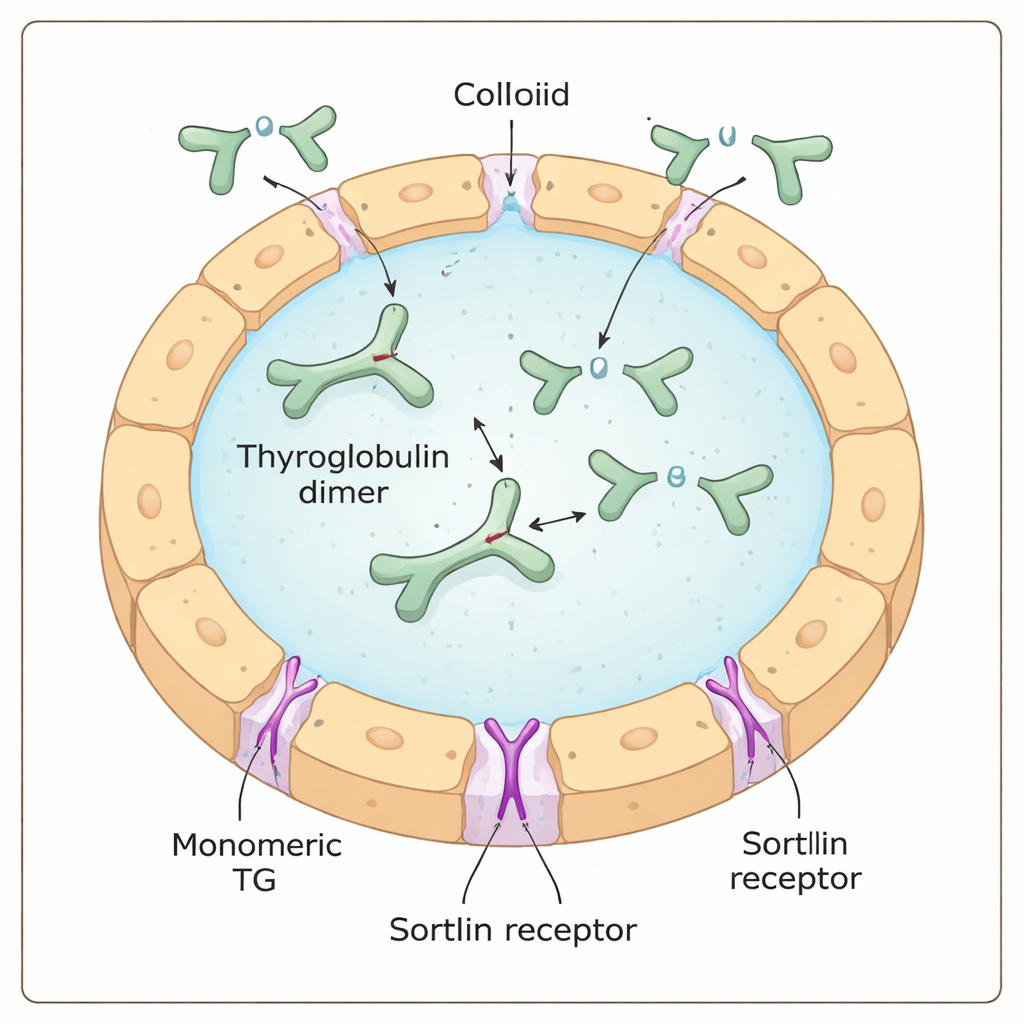
Een cellulaire poortwachter met een verborgen voorkeur
De receptor sortiline is voorgesteld als een van de “poortwachters” die thyreoglobuline aan het celoppervlak binden en naar binnen leiden. Eerder werk suggereerde dat sortiline de voorkeur geeft aan sterk gejodeerd thyreoglobuline, wat impliceerde dat de receptor het jodiumgehalte rechtstreeks zou kunnen waarnemen. Met een combinatie van biochemische tests, enkelmolecuulmassabelmetingen en celgebaseerde opnameremonstraties vonden de auteurs echter dat sortiline sterk de voorkeur geeft aan de eenheid, of monomere, vorm van thyreoglobuline boven de meer voorkomende gekoppelde, dimerische vorm. Hoe meer monomeer aanwezig in een monster, hoe efficiënter het complexe vormde met sortiline en door schildkliercellen werd geïntroduceerd, onafhankelijk van de hoeveelheid jodium die het droeg.
Inzoomen op het contactpunt
Om deze voorkeur op atomaire schaal te begrijpen, gebruikte het team hoogresolutie cryo-elektronenmicroscopie en crosslinking-massaspectrometrie. Deze methoden toonden aan dat sortiline een korte, flexibele staart herkent aan het C‑terminus (één uiteinde) van monomere thyreoglobuline. Deze staart schuift in een centrale holte van sortiline die lijkt op een tienbladige propeller en dockt aan twee kleine “hotspots” binnenin. Opmerkelijk is dat in de dimerische vorm van thyreoglobuline een deel van het gebied rond deze staart begraven ligt en voor sortiline onbereikbaar is, wat verklaart waarom het dimer een slechte partner is. De gegevens suggereren dat extracellulair trimmen of het losser worden van thyreoglobuline — door natuurlijke eiwitafbraak — helpt dimeren omzetten in monomeren die sortiline kan grijpen.
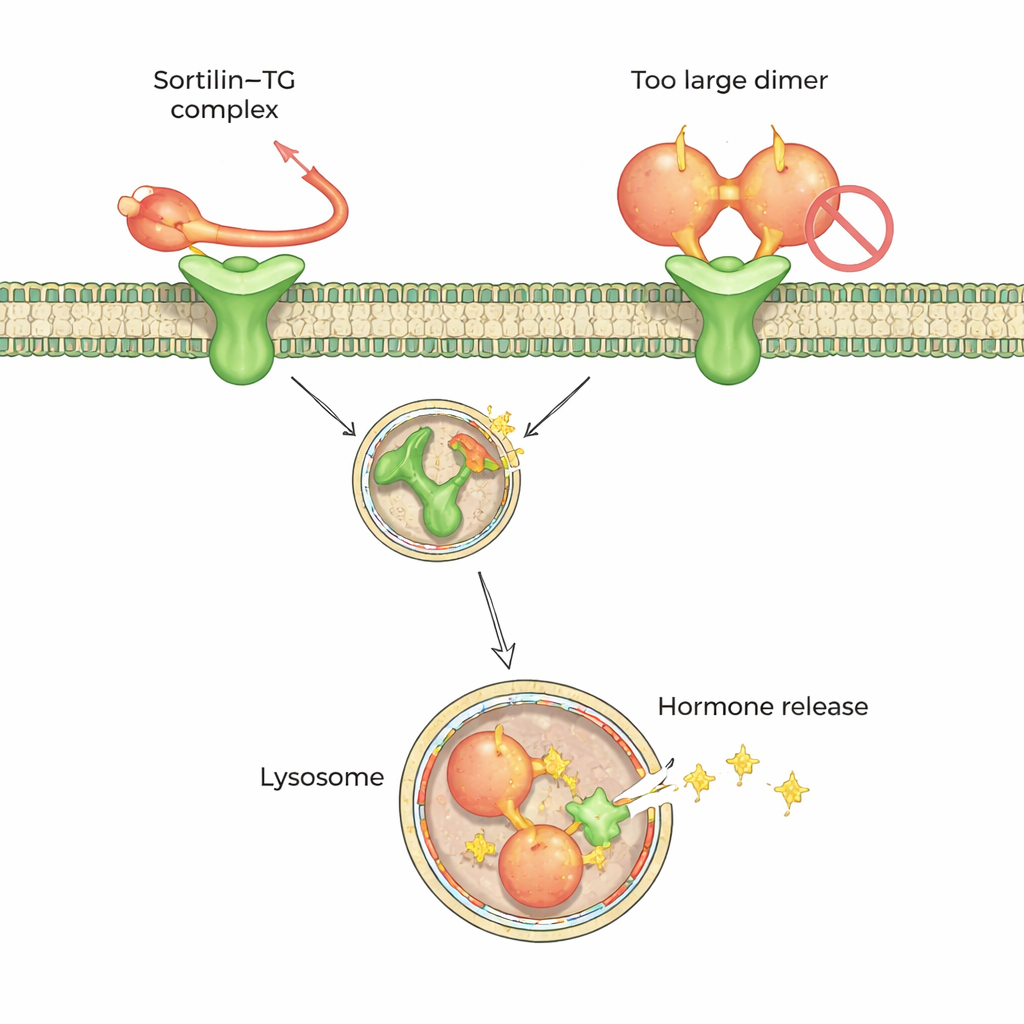
Een gedeelde dockcode voor veel laad-eiwitten
Sortiline is niet alleen een schildklier-eiwit; het helpt bij het vervoeren van veel verschillende moleculen door het lichaam, waaronder factoren die verbonden zijn met hart‑ en hersenziekten. Door hun structurele werk te combineren met geavanceerde predictietools zoals AlphaFold en AlphaPulldown, vergeleken de onderzoekers hoe tientallen bekende sortilinepartners mogelijk in de propellerholte binden. Ze vonden een terugkerend patroon: veel ladingseiwitten presenteren een ongestructureerde peptidensequentie van ongeveer twintig aminozuren die in dezelfde pocket past als de staart van thyreoglobuline, soms in dezelfde richting als een bekend hersenpeptide genaamd neurotensine, en soms in de tegengestelde richting. Ondanks de omgekeerde oriëntatie delen deze peptiden vergelijkbare kenmerken — een zure of negatief geladen groep aan het ene uiteinde, een volumineus aromatisch residu aan het andere, en een flexibele, vaak prolinerijke stretch ertussen.
Waarom jodium minder belangrijk is dan vorm
Aangezien het sleutelcontact tussen sortiline en thyreoglobuline deze flexibele staart is, onderzochten de auteurs of het extra joderen van een hormoonvormende tyrosine in die staart de binding zou veranderen. Dat bleek niet zo te zijn: een synthetisch peptide dat een volledig gevormd schildklierhormoon droeg gedroeg zich vrijwel identiek aan de ongemodificeerde versie. Modellering toonde aan dat de gejodeerde ring in de oplossing uitsteekt zonder nieuwe strakke contacten te maken. Samen met de opnameresultaten ondersteunt dit een herziene zienswijze: sortiline “telt” de jodiumatomen op thyreoglobuline niet. In plaats daarvan signaleert het of het eiwit genoeg is ontspannen of deels afgebroken om de monomere vorm en de staart op de juiste manier bloot te leggen.
Wat dit betekent voor schildkliergezondheid
Voor niet‑specialisten is de kernboodschap dat de vrijgave van schildklierhormoon minder wordt gereguleerd door een ingebouwde jodiumsensor en meer door een mechanische controle van eiwitsvorm en flexibiliteit. Sortiline fungeert als een scanner aan het celoppervlak die zoekt naar thyreoglobulinemoleculen die zijn losgemaakt of getrimd tot monomeren, waarna ze naar binnen worden gehaald voor de definitieve hormoonvrijgave en jodiumrecycling. Dit werk verduidelijkt een belangrijke stap in de biologie van schildklierhormonen en suggereert dat geneesmiddelen die sortiline blokkeren — momenteel onderzocht voor andere ziekten — onbedoeld de behandeling van schildklierhormonen zouden kunnen verstoren door dit herkenningsproces te beïnvloeden.
Bronvermelding: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Trefwoorden: schildklierhormoon, thyreoglobuline, sortiline, eiwitverkeer, endocytose