Clear Sky Science · nl
De brughelix van Cas12a is een allosterische regulator van R-loopvorming en RuvC-activatie
Waarom dit belangrijk is voor genbewerking
Veel krachtige instrumenten voor genbewerking, waaronder die achter opkomende therapieën en snelle diagnostische tests, vertrouwen op CRISPR-eiwitten die DNA op gekozen plaatsen knippen. Als deze moleculaire scharen echter op de verkeerde plek snijden, kunnen ze schadelijke bijwerkingen veroorzaken. Deze studie ontleedt een klein bewegend onderdeel binnen de Cas12a-editor, de zogenaamde brughelix, en laat zien hoe veranderingen in zijn vorm functioneren als een interne veiligheidsschakelaar die juiste doelherkenning koppelt aan DNA-knippen. Inzicht in deze schakel biedt een routekaart om CRISPR-instrumenten te ontwerpen die zowel nauwkeurig als veiliger zijn voor medische en biotechnologische toepassingen.
Een moleculaire klem met bewegende delen
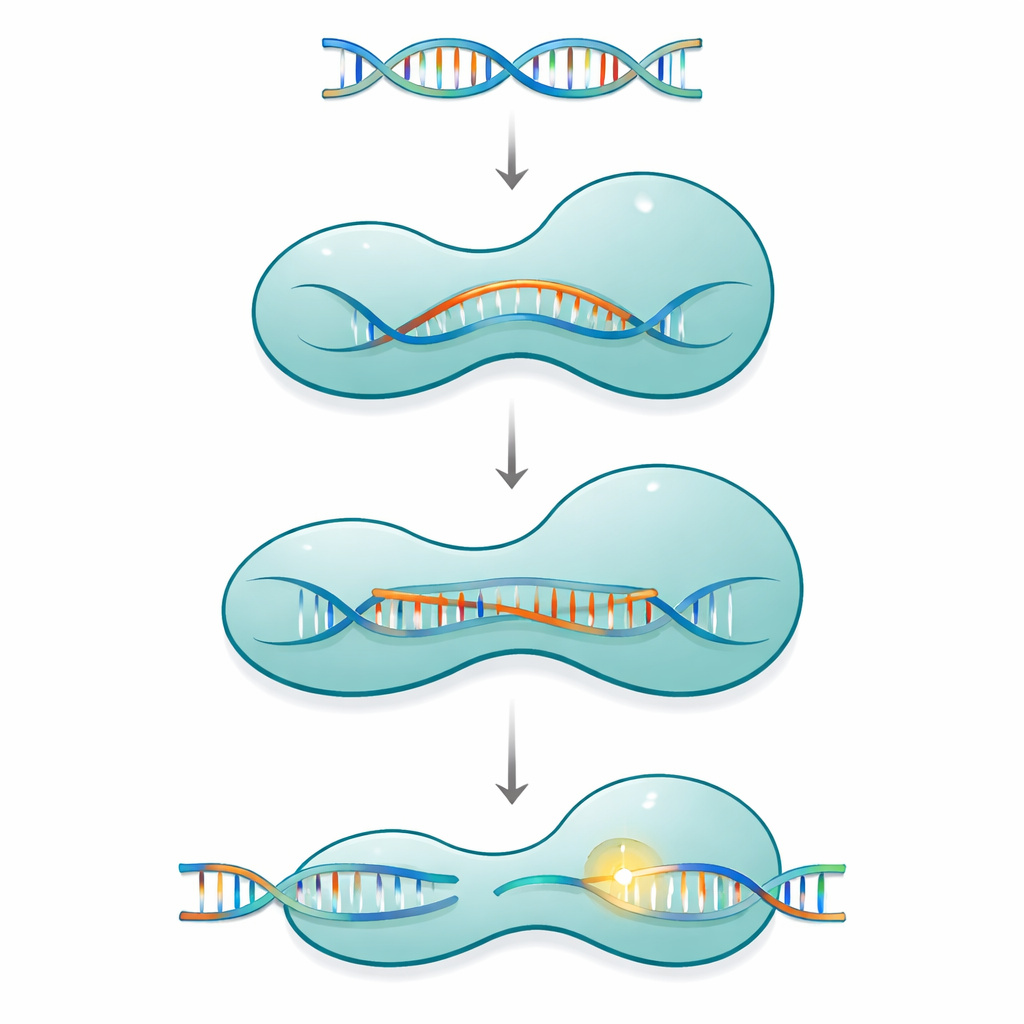
Cas12a behoort tot een familie van enkelvoudige eiwit-CRISPR-systemen die een korte gids-RNA gebruiken om overeenkomend DNA in virussen of in het genoom van een cel te vinden en te knippen. Het eiwit heeft de vorm van een tweearmige klem: een herkenningszijde die de sequentie controleert, en een knipzijde die de chemische machinerie herbergt. Deze twee helften zijn verbonden door een slanke, positief geladen segment dat de brughelix wordt genoemd. Wanneer Cas12a zijn gids-RNA en daarna zijn DNA-doel bindt, gedraagt het eiwit zich niet als een star instrument. In plaats daarvan beweegt het door een reeks van grote en kleine vormveranderingen die geleidelijk sluiten rond een groeiende RNA–DNA-hybride structuur, bekend als een R-loop, en activeert het knippunt pas volledig zodra een lang genoeg stuk juiste baseparing is gevormd.
Onderzoeken van de ingebouwde veiligheidsschakelaar
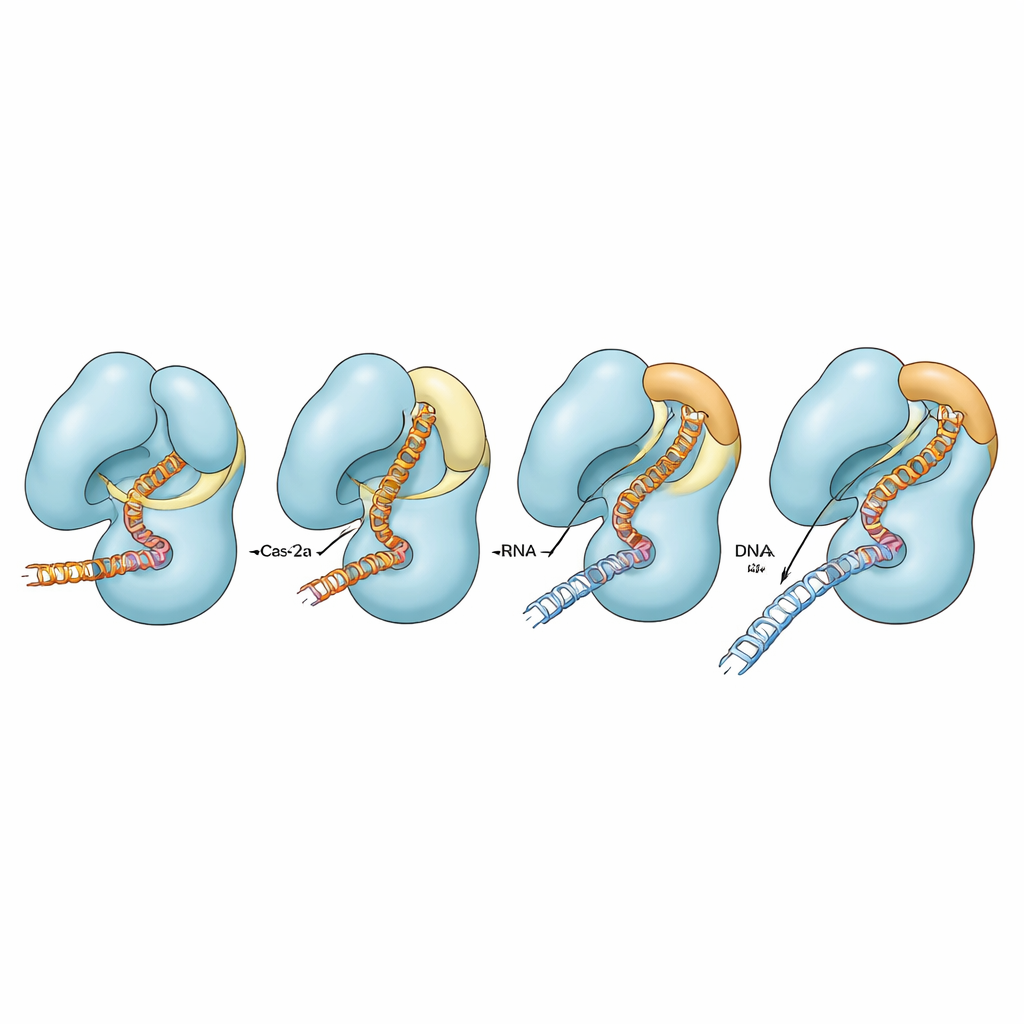
De onderzoekers richtten zich op een Cas12a uit de bacterie Francisella novicida en op een eerder ontworpen variant waarbij twee aminozuren in de brughelix waren vervangen door prolinen, een wijziging die bekendstaat omdat die helixen verstijft of verbreekt. Deze variant, genoemd FnoCas12aKD2P, knipt DNA selectiever maar langzamer dan het natuurlijke eiwit. Met cryo-elektronenmicroscopie legden ze vijf verschillende structurele momentopnamen vast van deze variant gebonden aan zijn gids-RNA en een stuk doel-DNA. Deze momentopnamen tonen het eiwit in verschillende stadia van zijn activatiepad, van vroege initiële DNA-herkenning tot latere toestanden waarin een deel van de RNA–DNA-hybride is gevormd maar volledige snijklaarheid nog niet is bereikt.
Hoe vormveranderingen nauwkeurig knippen aandrijven
Het vergelijken van de variant met eerder bepaalde structuren van normale Cas12a onthulde een duidelijk patroon. In het natuurlijke eiwit verandert een segment van de brughelix van een losse lus in een langere, rechte helix en buigt het naar de groeiende RNA–DNA-hybride, waarmee het nauw contact maakt. Tegelijkertijd versoepelt een aangrenzende helix in het knipdomein, en een klein gebied dat de "deksel" wordt genoemd, dat normaal gesproken het actieve centrum blokkeert, schakelt van lus naar helix en zwaait open. Gezamenlijk openen deze gecoördineerde bewegingen een ruimte die het mogelijk maakt dat één DNA-streng binnenkomt en wordt geknipt. In de proline-bevattende variant kan de brughelix deze lus-naar-helixtransitie of het juiste buigen niet volledig uitvoeren. Daardoor blijft de RNA–DNA-hybride vervormd en verder weg, blijft de deksel in een gesloten, lusachtige staat, en bereikt het complex zelden een volledig pre-katalytische conformatie. Deze mechanische flessenhals vertraagt knippen op het juiste doel en maakt het moeilijker voor niet-perfect passende DNA-moleculen om langs de interne controlepunten te glippen.
Fijnregelen van fideliteit door contacten aan te passen
Om te testen hoe verschillende contacten rond de deksel en de brughelix bijdragen aan activiteit, veranderden de auteurs specifieke geladen residuen die deze regio’s verbinden. In de normale Cas12a hadden het verbreken van deze contacten slechts bescheiden effecten op het knippen van perfect overeenkomend DNA, al beïnvloedden sommige omstandigheden hoe efficiënt de tweede DNA-streng werd gekliefd wanneer mismatches aanwezig waren. In de achtergrond met een aangetaste brughelix verminderden dezelfde substituties echter sterk of schaften ze bijna alle knipactiviteit van beide strengen af, vooral wanneer gids en DNA niet perfect overeenkwamen. Computersimulaties ondersteunden deze bevindingen en toonden aan dat alleen wanneer de brughelix volledig zijn helical vorm kan aannemen, de brug, de aangrenzende helix, de deksel en de nucleïnezuren in sterk gecoördineerde bewegingen bewegen. Wanneer de helix is aangetast, raken deze bewegingen gedeeltelijk of volledig ontkoppeld en worstelt het enzym om zijn katalytische cyclus te voltooien.
Een ontwerpgids voor CRISPR-instrumenten van de volgende generatie
Samengevat onthult het werk de brughelix als een intern controleniveau dat de lengte en kwaliteit van de RNA–DNA-hybride koppelt aan het openen van de knipruimte in Cas12a. Door het eiwit te dwingen een specifieke reeks vormveranderingen te voltooien voordat het DNA wordt gekliefd, handhaaft dit mechanisme van nature discriminatie tegen mismatches. De bevindingen helpen verklaren waarom gerichte wijzigingen in dit kleine gebied Cas12a-varianten kunnen opleveren met verminderd off-target knippen en verminderde "collateral" DNA-activiteit, eigenschappen die wenselijk zijn voor veiliger genbewerking en diagnostiek. Breder beschouwd benadrukt de studie hoe subtiele verschuivingen in korte helixen langafstandcommunicatie in grote moleculaire machines kunnen coördineren, en biedt het algemene principes voor het ontwerpen van nucleïnezuurverwerkende enzymen met hoge fideliteit.
Bronvermelding: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Trefwoorden: CRISPR-Cas12a, nauwkeurigheid van genbewerking, brughelix, R-loopvorming, allosterische regulatie