Clear Sky Science · nl
RoboA versterkt planaria-stamcelbestemming via FoxA en Anosmin1a
Hoe wormen hun organen teruggroeien
Sommige platwormen kunnen vrijwel elk ontbrekend lichaamsdeel opnieuw vormen, van hun voedingsbuis tot hun hersenen. Deze opmerkelijke eigenschap berust op volwassen stamcellen die naar behoefte in vele verschillende celtypen kunnen veranderen. Maar met zoveel vrijheid: hoe zorgen deze cellen ervoor dat ze niet per ongeluk het verkeerde weefsel op de verkeerde plaats bouwen—bijvoorbeeld maagcellen in het hoofd in plaats van neuronen? Deze studie gebruikt de planaria-platworm om te onthullen hoe een kleine set signalen uiterst flexibele stamcellen op het juiste spoor houdt tijdens regeneratie.
De regenererende worm en haar verborgen potentieel
De planaria Schmidtea mediterranea is een favoriete modelorganisme om regeneratie te bestuderen omdat een grote populatie stamcellen door het hele lichaam is verspreid. Een belangrijk orgaan is de pharynx, een spierachtige voedingsbuis die in het midden van de worm ligt en bij voedselopname naar buiten opent. Eerder onderzoek toonde aan dat een gen genaamd foxA cruciaal is voor het herbouwen van deze pharynx na beschadiging, en dat normaal gesproken alleen bepaalde stamcellen nabij de pharynx foxA activeren. De nieuwe studie stelt een ogenschijnlijk eenvoudige vraag: wat weerhoudt stamcellen in andere regio’s—vooral het hoofd en de hersenen—ervan ook een pharynx-identiteit te kiezen?
Wanneer de begeleiding ontbreekt
De onderzoekers richtten zich op een receptorproteïne genaamd RoboA, die op lage niveaus in veel celtypen voorkomt, ook in stamcellen. Toen ze RoboA-activiteit verminderden met RNA-interferentie, ontwikkelden dieren na amputatie vaak extra, verkeerd geplaatste pharynxen. Nauwkeuriger onderzoek toonde iets subtielers: zelfs in onbeschadigde wormen leidde het terugschakelen van RoboA tot het verschijnen van pharynxachtige neuronen en spieren in het hersengebied. Deze “ectopische pharynxneuronen” gedroegen zich qua genexpressie als normale pharynxcellen, maar zaten nu op de verkeerde plaats. Belangrijk is dat het algemene lichaamsplan en de hersenarchitectuur grotendeels intact bleven, wat suggereert dat RoboA het hele dier niet hertekende, maar veeleer fijn afstemde wat nabijgelegen stamcellen worden.
Een drieganger-schakelaar voor celbestemming
Om te begrijpen hoe RoboA werkt, zocht het team naar partners buiten de cel. Hoewel Robo-eiwitten vooral bekend staan om het binden van een ligand genaamd Slit, reproduceerde het uitschakelen van Slit de verkeerd geplaatste pharynxcellen niet. Een omvangrijke RNAi-screen van uitgescheiden en membraaneiwitten wees in plaats daarvan Anosmin1a (Anos1a) aan, een uitgescheiden eiwit verwant aan een humane factor die bij het Kallmann-syndroom betrokken is. Vermindering van Anos1a veroorzaakte vergelijkbare extra pharynxneuronen, en gecombineerde RoboA–Anos1a-knockdowns gedroegen zich alsof ze in dezelfde route samenwerken. Tegelijkertijd toonde moleculaire profilering dat de transcriptiefactor FoxA centraal staat in de beslissing: wanneer RoboA aanwezig is, houdt het FoxA uitgeschakeld in stamcellen van het hoofd; wanneer RoboA-signaal ontbreekt, schakelt FoxA aan en kunnen diezelfde stamcellen zelfs in de hersenen kiezen voor een pharynxneuron-bestemming.
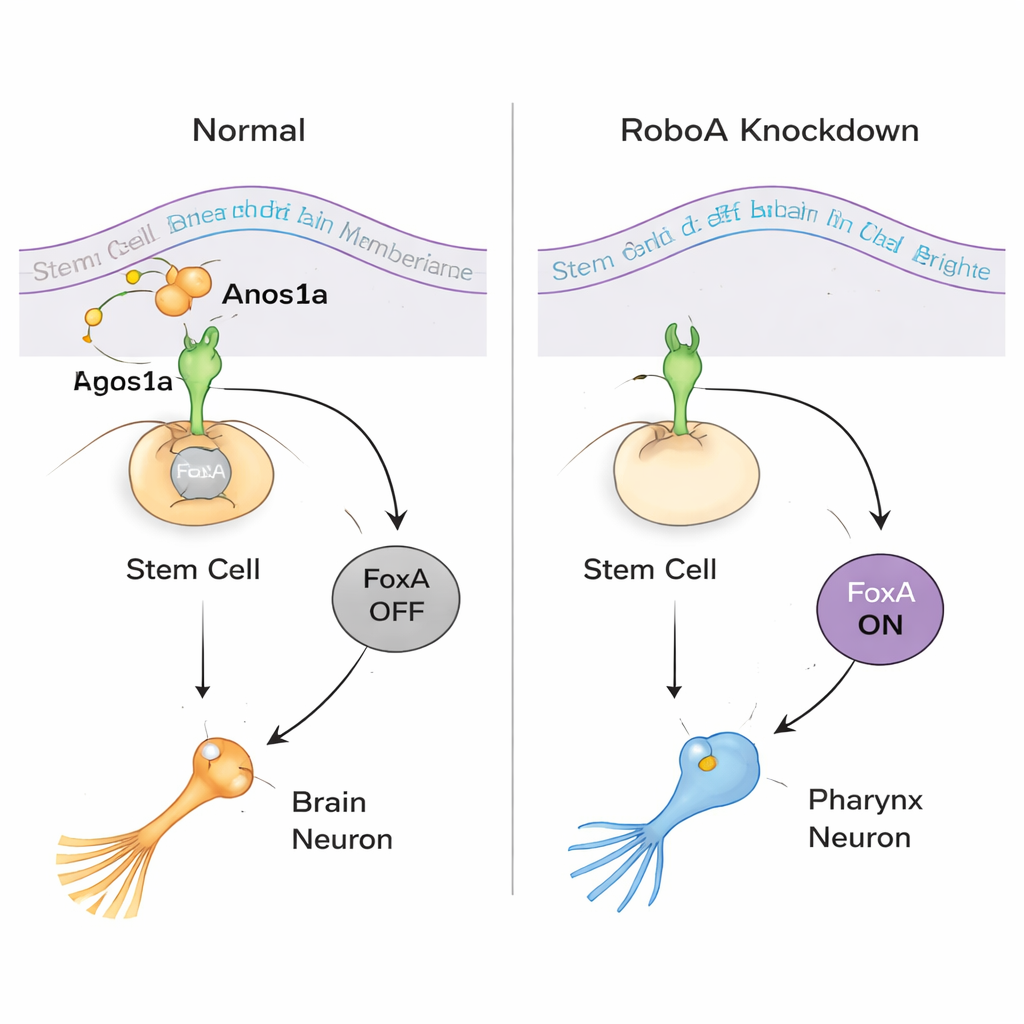
Het onthullen van een tweerichtingskeuze in stamcellen
Het team vroeg vervolgens of deze flexibiliteit beide richtingen op werkt. In normale dieren vertrouwen stamcellen rond de pharynx op FoxA om pharynxneuronen en epitheliale cellen te worden, terwijl pharynxspieren een andere route volgen. Wanneer FoxA voor langere periodes werd uitgeschakeld, verloren wormen hun pharynxen volledig en groeiden abnormale uitgroeisels in het midden van het lichaam. Enkelcel-RNA-sequencing en markeranalyse toonden aan dat deze uitgroeisels veel celtypen bevatten die normaal beperkt zijn tot het hoofd, waaronder oecellen en hersenspecifieke neuronen. Met andere woorden: wanneer FoxA ontbreekt waar de pharynx zou moeten vormen, neigen lokale stamcellen naar een hersenachtige identiteit. Deze bevinding toont dat dieselde stamcellen in de ene of de andere richting kunnen worden geduwd—“pharynx” of “hersenen”—afhankelijk van welke signalen ze ontvangen.
Fijnregelen van regeneratie, niet het herschilderen van de kaart
Als men alle bewijs samenbrengt, stellen de auteurs dat planaria-regeneratie door twee lagen wordt geleid. Brede “positie-controlesignalen”, zoals Wnt en andere patroonvormende moleculen, zetten de grove kaart uit van kop, romp en staart. Daarboven opereren lokale “bestemming-versterkende” genen zoals RoboA en Anos1a als veiligheidschecks die ongepaste opties blokkeren. In het hoofd houdt RoboA–Anos1a-signaal FoxA uitgeschakeld zodat stamcellen hersenneuronen produceren in plaats van pharynxcellen; nabij de pharynx mag FoxA aangaan en pharynx-specifieke bestemmingen aansturen. Deze gelaagde controle stelt planaria-stamcellen in staat buitengewoon plastisch te blijven en toch organen op de juiste plaats te herbouwen, en biedt een blauwdruk voor hoe robuuste regeneratie kan samengaan met strikte anatomische orde.
Bronvermelding: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Trefwoorden: planaria regeneratie, pluripotentie van stamcellen, orgaanpatronering, RoboA-signaaltransductie, transcriptiefactor FoxA