Clear Sky Science · nl
NeoPrecis: verbetering van de voorspelling van respons op immunotherapie door integratie van gekwalificeerde immunogeniciteit en clonality-bewuste neoantigeenlandschappen
Waarom sommige kankers op immunotherapie reageren en andere niet
Immunotherapie heeft de kankerzorg veranderd, maar veel patiënten profiteren er nog steeds niet van en sommigen krijgen ernstige bijwerkingen. Een grote vraag is waarom sommige tumoren door het immuunsysteem worden opgemerkt en vernietigd, terwijl andere ongemerkt blijven. Deze studie introduceert NeoPrecis, een computationele methode die nauwkeuriger kijkt naar de “vlaggen” die tumoren aan het immuunsysteem laten zien—genoemd neoantigenen—en die die informatie gebruikt om beter te voorspellen welke patiënten waarschijnlijk op moderne immunotherapieën zullen reageren.
Nieuwe vlaggen op kankercellen
Kankercellen hopen DNA-mutaties op die de eiwitten die ze produceren kunnen veranderen. Kleine fragmenten van deze gewijzigde eiwitten, bekend als neoantigenen, kunnen op het celoppervlak worden gepresenteerd en door T-cellen—de moordenaars van het immuunsysteem—als vreemd worden herkend. Jarenlang vertrouwden artsen en onderzoekers op grove maatstaven zoals tumor mutation burden—het totale aantal mutaties—om te schatten hoe waarschijnlijk het is dat een kanker op immuun checkpointremmers reageert. Maar dat is een botte maatstaf: niet elke mutatie creëert een zichtbaar of aantrekkelijk doelwit voor T-cellen, en tumoren kunnen samengesteld zijn uit veel verschillende celtypen. NeoPrecis is ontworpen om verder te gaan dan alleen het tellen van mutaties en in plaats daarvan te beoordelen hoeveel daarvan daadwerkelijk veelbelovende doelwitten zijn over de hele tumor.
Drie belangrijke ingrediënten tegelijk bekijken
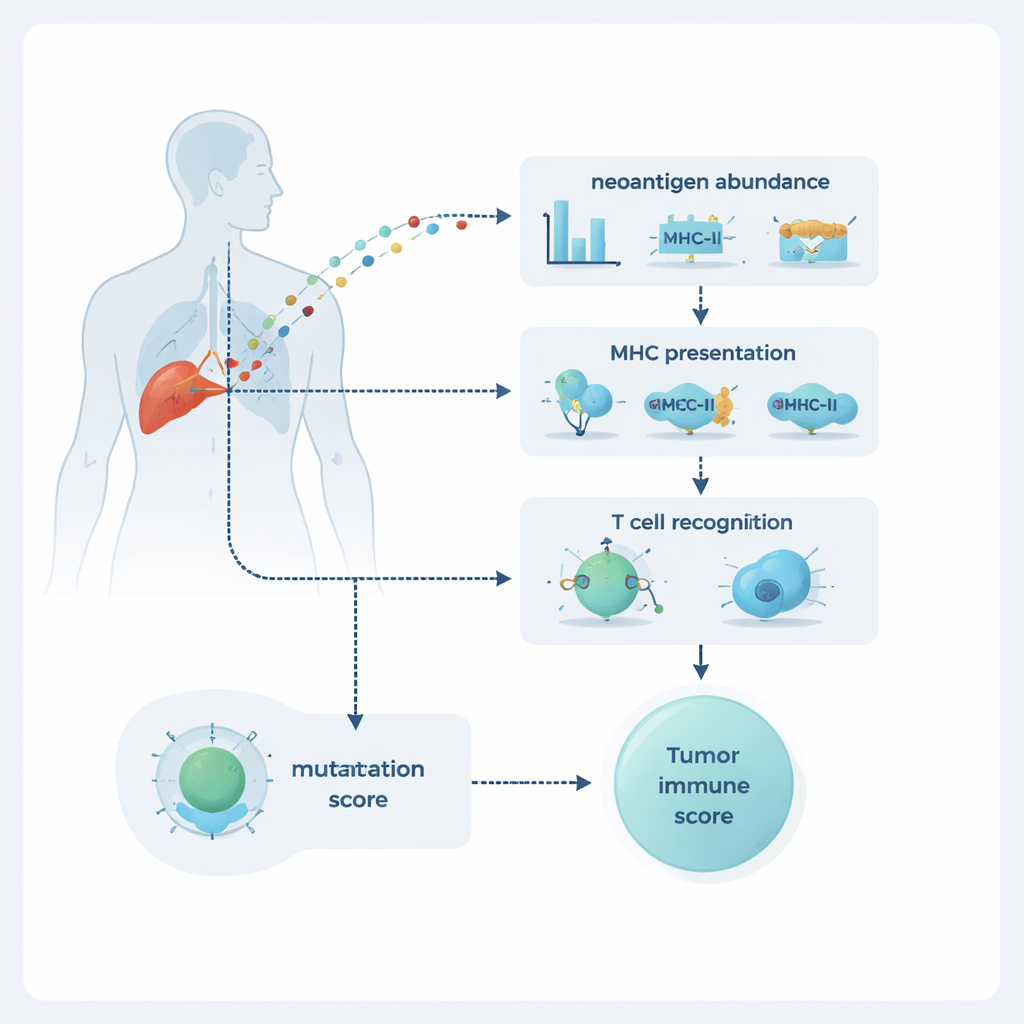
NeoPrecis evalueert elke mutatie langs drie dimensies: hoe overvloedig deze in de tumor is, of deze waarschijnlijk op het celoppervlak wordt gepresenteerd, en hoe waarschijnlijk het is dat T-cellen deze opmerken. Overvloed wordt geschat met DNA- en RNA-sequencing, die tonen hoe algemeen de mutatie is en hoe sterk ze wordt tot expressie gebracht. Presentatie wordt gemodelleerd via binding aan moleculen genaamd MHC klasse I en klasse II, die fungeren als billboards die eiwitfragmenten aan T-cellen tonen. Het meest vernieuwende onderdeel is de T-celherkenningscomponent, NeoPrecis-Immuno. Dit model leert van grote databanken met bekende T-cel–peptide-interacties om in te schatten hoe verschillend een gemuteerd fragment is van zijn normale tegenhanger op een manier die relevant is voor T-celherkenning, terwijl het ook rekening houdt met de specifieke MHC-varianten die een persoon draagt.
Een computer leren wat T-cellen “zien”
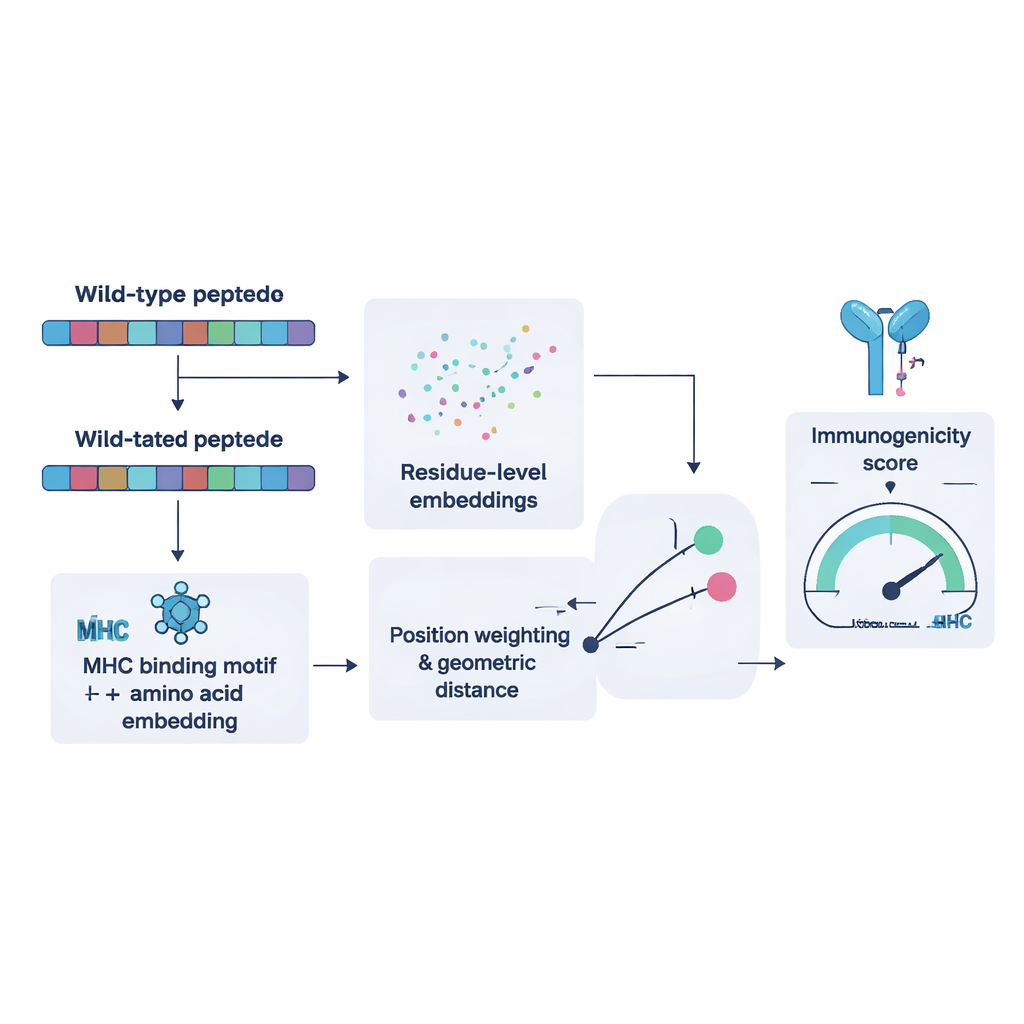
Om NeoPrecis-Immuno te trainen, stelden de onderzoekers eerst duizenden voorbeelden samen waarbij dezelfde T-cel meerdere soortgelijke peptiden herkent en voorbeelden waarbij dat niet het geval is. Ze gebruikten deze voorbeelden om het model te leren dat gemuteerde fragmenten die sterk op normale lijken minder snel een immuunrespons oproepen, omdat dergelijke zelfachtige doelwitten doorgaans tijdens de T-celontwikkeling worden gefilterd. Het model stelt elk peptide voor als een punt in een wiskundige ruimte die wordt gevormd door zowel de aminozuurvolgorde als de bindingsvoorkeuren van de MHC-moleculen van de persoon. Vervolgens meet het hoe ver het gemuteerde peptide van het origineel afligt. Grotere, motiefgeïnformeerde afstanden komen overeen met een hogere kans op immunogeniciteit. Getest tegen bestaande tools op onafhankelijke kankerdatasets, presteerde NeoPrecis-Immuno gelijk aan of beter dan deze tools, vooral bij MHC klasse II, die presenteert aan helper-T-cellen die antitumorresponses ondersteunen en in stand houden.
Van individuele mutaties naar de hele tumor
Individuele mutaties vertellen maar een deel van het verhaal; ook de verdeling binnen de tumor doet ertoe. Sommige mutaties zijn “clonaal”, aanwezig in bijna elke kankercel, terwijl andere “subclonaal” zijn, alleen in bepaalde regio’s voorkomen. NeoPrecis bouwt een “neoantigeenlandschap” door zijn immunogeniciteitsscores over mutaties op te tellen en daarbij informatie te leggen over bij welke subclonen ze horen en hoe vaak die subclonen voorkomen. Dit levert tumorniveau-scores op die kankers benadrukken die rijk zijn aan sterke, wijdverbreide neoantigenen—vooral die welke zowel door MHC klasse I als klasse II kunnen worden gepresenteerd en mogelijk gecoördineerde helper- en killer-T-celresponses kunnen opwekken. In patiëntengroepen met melanoom en niet-kleincellig longcarcinoom die behandeld werden met checkpointremmers, scheidden deze op NeoPrecis gebaseerde scores responsers beter van non-responders dan standaard mutatietellingen, en waren ze bijzonder behulpzaam bij complexe, heterogene longtumoren.
Wat dit voor patiënten betekent
Voor patiënten ligt de belofte van NeoPrecis in een preciezere afstemming van immunotherapieën op degenen die er het meest van zullen profiteren, en een helderder begrip waarom sommige tumoren resistent zijn tegen behandeling. Door te focussen op de kwaliteit en verdeling van neoantigenen—niet alleen op hun kwantiteit—helpt het kader te verklaren waarom tumoren met vergelijkbare mutatielasten zich heel verschillend kunnen gedragen. In de toekomst zouden zulke gedetailleerde kaarten van het immuun-zichtbare landschap van een tumor niet alleen het gebruik van checkpointremmers kunnen sturen, maar ook het ontwerp van gepersonaliseerde kankervaccins die prioriteit geven aan de meest krachtige en breed gedeelde doelwitten binnen de kanker van elke persoon.
Bronvermelding: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Trefwoorden: kankerimmunotherapie, neoantigenen, tumorheterogeniteit, checkpointremmers, computationale oncologie