Clear Sky Science · nl
Stenotrophomonas bevordert progressie van gastro-intestinale tumoren via STING-afbraak in tumorcellen en verzwakte immuunrespons
Verborgen bacteriën in tumoren
De meesten weten dat microben in onze darmen spijsvertering en zelfs stemming kunnen beïnvloeden, maar weinigen beseffen dat levende bacteriën zich daadwerkelijk binnen kankercellen kunnen vestigen. Deze studie onthult hoe een veelvoorkomende omgevingsbacterie, Stenotrophomonas, zich verbergt in gastro-intestinale tumoren en stilletjes hun groei bevordert, terwijl ze tegelijkertijd de afweer van het lichaam verzwakt en moderne kankerimmunotherapieën minder effectief maakt.
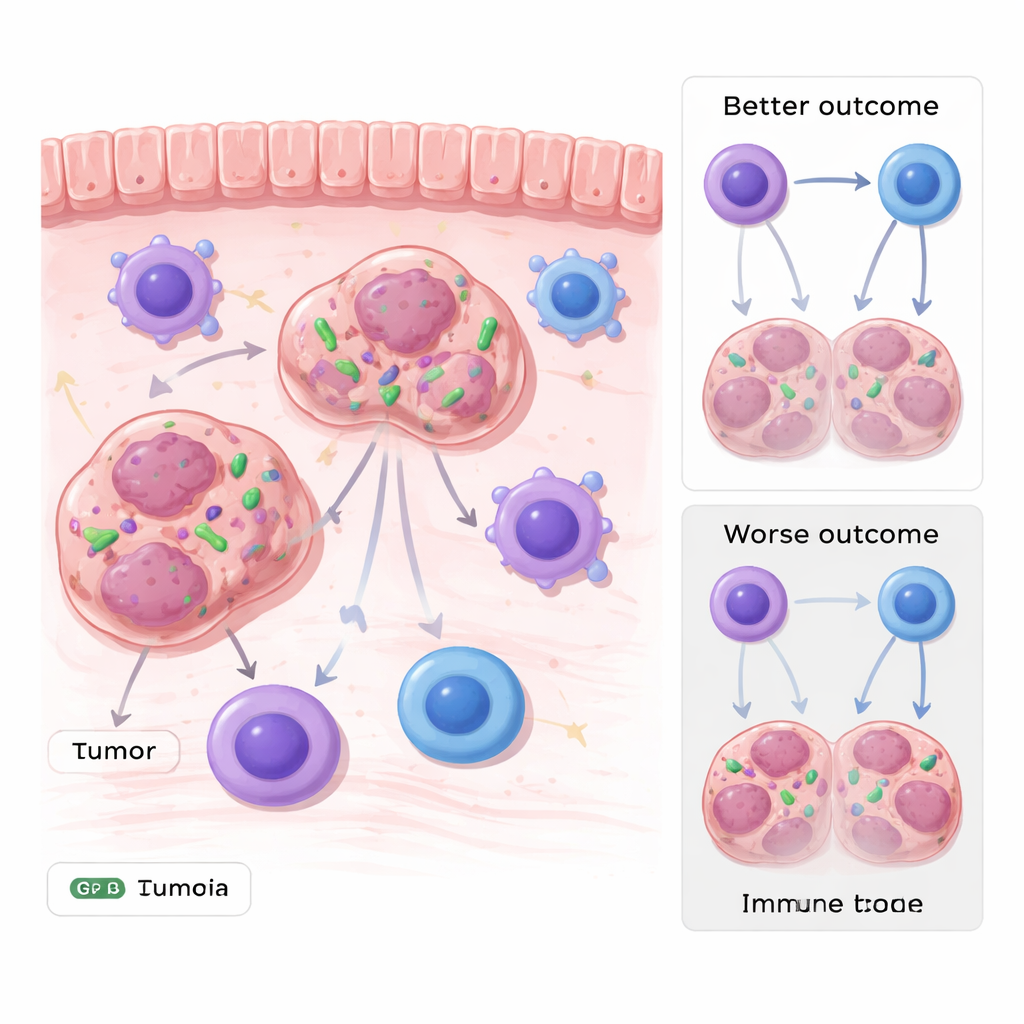
Bacteriën in kankercellen
Gastro-intestinale tumoren, zoals maag- en colorectale kankers, groeien in voortdurend contact met de rijke bacteriële gemeenschappen van het spijsverteringskanaal. Door meerdere genetische datasets van patiënten te analyseren en hun bevindingen vervolgens in tumormonsters te valideren, vonden de onderzoekers dat DNA van Stenotrophomonas buitengewoon vaak voorkwam in verschillende typen gastro-intestinale tumoren. Belangrijk is dat de vindplaats niet alleen oppervlaktecontaminatie leek te zijn: beeldvormende methoden, waaronder fluorescente probes en elektronenmicroscopie, toonden hele bacteriën aan in het cytoplasma van tumorcellen. Patiënten wier tumoren hogere niveaus van deze bacterie bevatten, hadden de neiging een slechtere prognose te hebben, wat de microbe koppelt aan een minder gunstige uitkomst.
Hoe een microbe het immuunevenwicht beïnvloedt
Het team vroeg zich vervolgens af of deze verborgen bacteriën slechts samenvielen met agressieve tumoren of daadwerkelijk de ziekte stimuleren. In muismodellen infecteerden ze tumorcellen met fluorescent gelabelde Stenotrophomonas voordat ze deze in dieren implanteren. Tumoren die de bacterie droegen, groeiden sneller en groter dan de bacterievrije tumoren, over meerdere kankerceltypes heen. Bij onderzoek van het omliggende immuunsysteem zagen de onderzoekers dat het totale aantal immuuncellen, inclusief T-cellen en macrofagen, vergelijkbaar was. Het cruciale verschil lag bij een gespecialiseerde subset macrofagen die het molecuul MHC-II tot expressie brengen, waarmee ze tumorfragmenten presenteren aan cytotoxische T-cellen. In tumoren met Stenotrophomonas waren deze MHC-II–positieve macrofagen sterk verminderd, en T-cellen vertoonden zwakkere kankerdodende activiteit.
Het kortsluiten van een cellulaire alarmsysteem
Om het mechanisme te begrijpen richtten de onderzoekers zich op een belangrijk alarmsignaal binnen cellen, bekend als STING, dat normaal vreemd DNA detecteert en de afgifte van antivirale 'gevaar'-signalen, type I interferonen, op gang brengt. In laboratoriumexperimenten produceerden tumorcellen die met Stenotrophomonas waren geïnfecteerd veel minder interferon-beta, en de genen die normaal door dit pad worden geactiveerd, waren onderdrukt. De studie toonde aan dat de bacterie stress veroorzaakt in het eiwitvouwhuis van de cel, het endoplasmatisch reticulum, en vervolgens een kwaliteitscontrole-route kapert die ER-geassocieerde degradatie heet. Via een hulp-eiwit genaamd SEL1L tagt deze route het STING-eiwit voor afbraak in het proteasoom, de 'versnipperaar' van de cel. Met uitgeputte STING-niveaus geeft de tumorcel een zwakker alarm af, wat leidt tot minder interferon en, daaruit volgend, verminderde activering van MHC-II–positieve macrofagen.
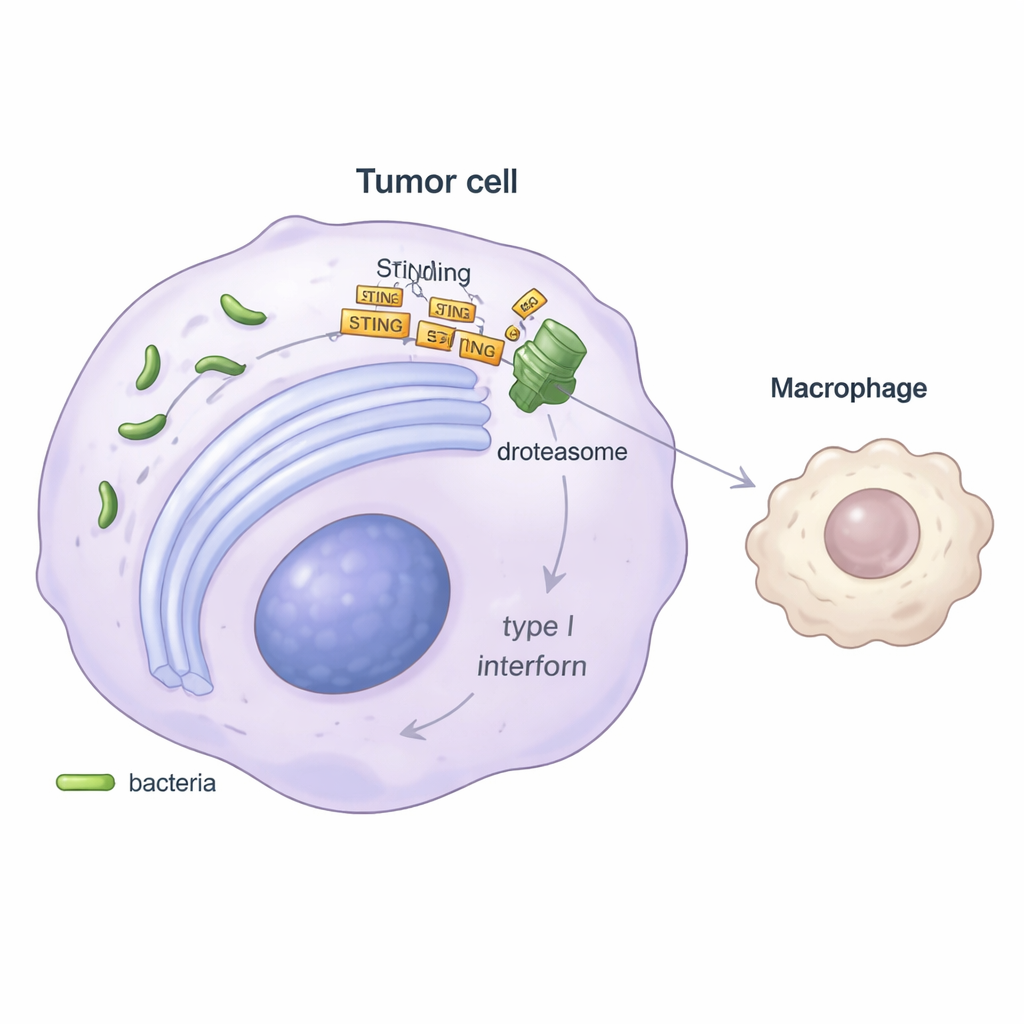
Ondergraven van immunotherapie — en een mogelijke oplossing
Aangezien moderne immunotherapieën zoals anti–PD-1 afhankelijk zijn van een krachtige T-celrespons, testte het team hoe intracellulaire Stenotrophomonas de behandeling beïnvloedt. Bij muizen reageerden tumoren met de bacterie slechter op anti–PD-1 vergeleken met bacterievrije tumoren, zelfs wanneer gecombineerd met chemotherapie. T-cellen in deze tumoren toonden verminderde activiteits- en delingsmarkers, consistent met onvoldoende immuunstimulatie. Opmerkelijk was dat behandeling van de dieren met het antibioticum levofloxacine, dat Stenotrophomonas effectief doodt, de tumorgroei vertraagde en de respons op anti–PD-1 verbeterde. Het herstel van interferon-signaalering met een klinisch interferonmiddel kon ook de populatie nuttige MHC-II–positieve macrofagen herstellen en in sommige situaties de T-cel-killing nieuw leven inblazen, wat de centrale rol van dit pad onderstreept.
Wat dit betekent voor patiënten
Voor de niet-specialist is de kernboodschap dat sommige gastro-intestinale kankers mogelijk een eigen intern microbioom hebben dat hen helpt immuunaanvallen te ontlopen. Stenotrophomonas verlaagt door afbraak van het STING-alarm in tumorcellen de immuunsignalen die normaal macrofagen en cytotoxische T-cellen zouden mobiliseren. Dit versnelt niet alleen de tumorgroei, maar kan ook helpen verklaren waarom bepaalde patiënten geen voordeel halen uit krachtige immunotherapieën. Hoewel aanvullend onderzoek nodig is voordat dit de klinische praktijk verandert, zorgen deze bevindingen voor de mogelijkheid dat het testen van tumoren op dergelijke bacteriën — en het selectief behandelen met gerichte antibiotica of middelen die STING stabiliseren — op termijn de uitkomsten voor mensen met maag- en colorectale kanker kan verbeteren.
Bronvermelding: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
Trefwoorden: tumormicrobioom, gastro-intestinale kanker, Stenotrophomonas, STING-route, kankerimmunotherapie