Clear Sky Science · nl
NR6A1 is essentieel voor de specificatie, vorming en overleving van neurale-kruin-cellen
Hoe vroege celdeliberingen het gezicht en lichaam vormen
Voordat we geboren worden, reizen een speciale groep cellen, neurale-kruin-cellen genoemd, door het embryo om mee te helpen aan de bouw van gezicht, hart, zenuwen en meer. Als deze cellen het niet goed doen, kunnen baby’s met ernstige aangeboren afwijkingen ter wereld komen. Deze studie onthult een eerder ondergewaardeerde moleculaire schakelaar, een eiwit genaamd NR6A1, die helpt bepalen wanneer en waar neurale-kruin-cellen in zoogdierembryo’s ontstaan, en wat er gebeurt wanneer die schakelaar faalt.
De zwervende bouwers van het embryo
Neurale-kruin-cellen ontstaan heel vroeg in de ontwikkeling langs de rand van het zich vormende brein en ruggenmerg. Nadat ze zich losmaken van dit weefsel, migreren ze lange afstanden om veel verschillende structuren te creëren, van aangezichtsbeenderen en kraakbeen tot onderdelen van het perifere zenuwstelsel en pigmentcellen in de huid. Omdat zij bijdragen aan zoveel organen, kunnen zelfs kleine verstoringen in hun vorming leiden tot brede aandoeningen die bekendstaan als neurocristopathieën, waaronder craniofaciaal syndromen zoals Treacher Collins. Begrijpen hoe deze cellen voor het eerst verschijnen is daarom essentieel om zowel normale ontwikkeling als aangeboren afwijkingen te verklaren.
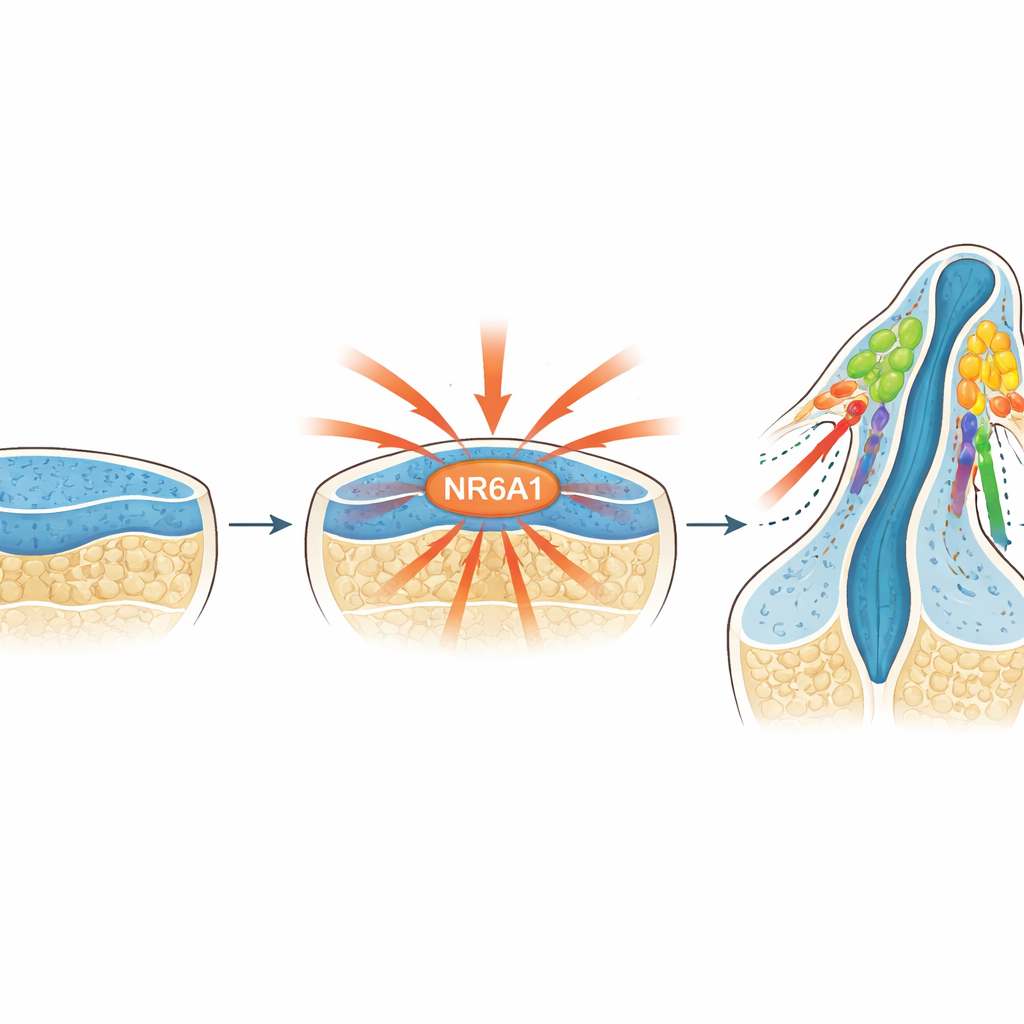
Een nieuw erkende hoofdschakelaar
De onderzoekers richtten zich op NR6A1, een lid van de familie van nucleaire receptoreiwitten die genactiviteit reguleren. Eerder werk suggereerde dat NR6A1 betrokken zou kunnen zijn bij hoofd- en gezichtsaandoeningen, maar de rol ervan in neurale-kruin-cellen was onbekend. Door NR6A1 te volgen in muisembryo’s vanaf net na implantatie, vonden ze dat de aanwezigheid sterk overeenkwam met waar en wanneer neurale-kruin-cellen normaal worden gevormd: het verschijnt in het vroege neurale weefsel, concentreert zich langs de dorsale (achter)zijde van het zich ontwikkelende brein en ruggenmerg, en is ook te zien in cellen op het moment dat ze dit weefsel verlaten om te gaan migreren.
Wat er gebeurt als de schakelaar ontbreekt
Muisjes die volledig NR6A1 missen overlijden vroeg in de ontwikkeling, dus het team onderzocht embryo’s net voor dat punt. Ze zagen een ernstig tekort aan neurale-kruin-cellen, met name achter de eerste boog die delen van kaak en nek zal vormen, waar migrerende neurale-kruin-cellen vrijwel geheel afwezig waren. Belangrijke genetische programma’s die normaal neurale-kruin-identiteit markeren en cellen in staat stellen los te komen en te bewegen, waren scherp verminderd. Tegelijkertijd bleven genen die cellen in een stamcelachtige, sterk proliferende staat houden aanstaan, en veel neurale-kruin-achtige cellen die zich wel vormden, stierven al snel. Deze bevindingen geven aan dat zonder NR6A1 neurale stamcellen niet goed overgaan naar migrerende neurale-kruin-cellen en niet kunnen overleven.
Stemheid uitzetten en migratie inschakelen
Om te begrijpen hoe NR6A1 deze controle uitoefent, koppelden de auteurs verschillende krachtige moleculaire technieken, waaronder enkelcellig RNA-sequencing, kaartlegging van chromatintoegankelijkheid en gerichte DNA–eiwitbindingsassays in zowel muis- als menselijk stamcel-afgeleide neurale-kruin-cellen. Ze ontdekten dat NR6A1 fysiek bindt aan specifieke DNA-motieven nabij genen die twee tegengestelde programma’s beheersen: één die pluripotentie in stand houdt (het vermogen om veel celtypen te worden) en een ander dat neurale-kruin-identiteit en celbeweging stimuleert. Wanneer NR6A1 aanwezig is, wordt chromatine rond stemheidsgenen zoals Oct4 en Nanog minder toegankelijk en deze genen worden omlaag gereguleerd, terwijl regio’s nabij neurale-kruin- en epitheliaal-naar-mesenchymale-transitie-genen opener en actiever worden. Overexpressie van Oct4 tijdens het cruciale venster van neurale-kruinvorming bootste het verlies van NR6A1 na, wat verder aantoont dat stemheid uitgeschakeld moet worden zodat neurale-kruin-cellen kunnen ontstaan.
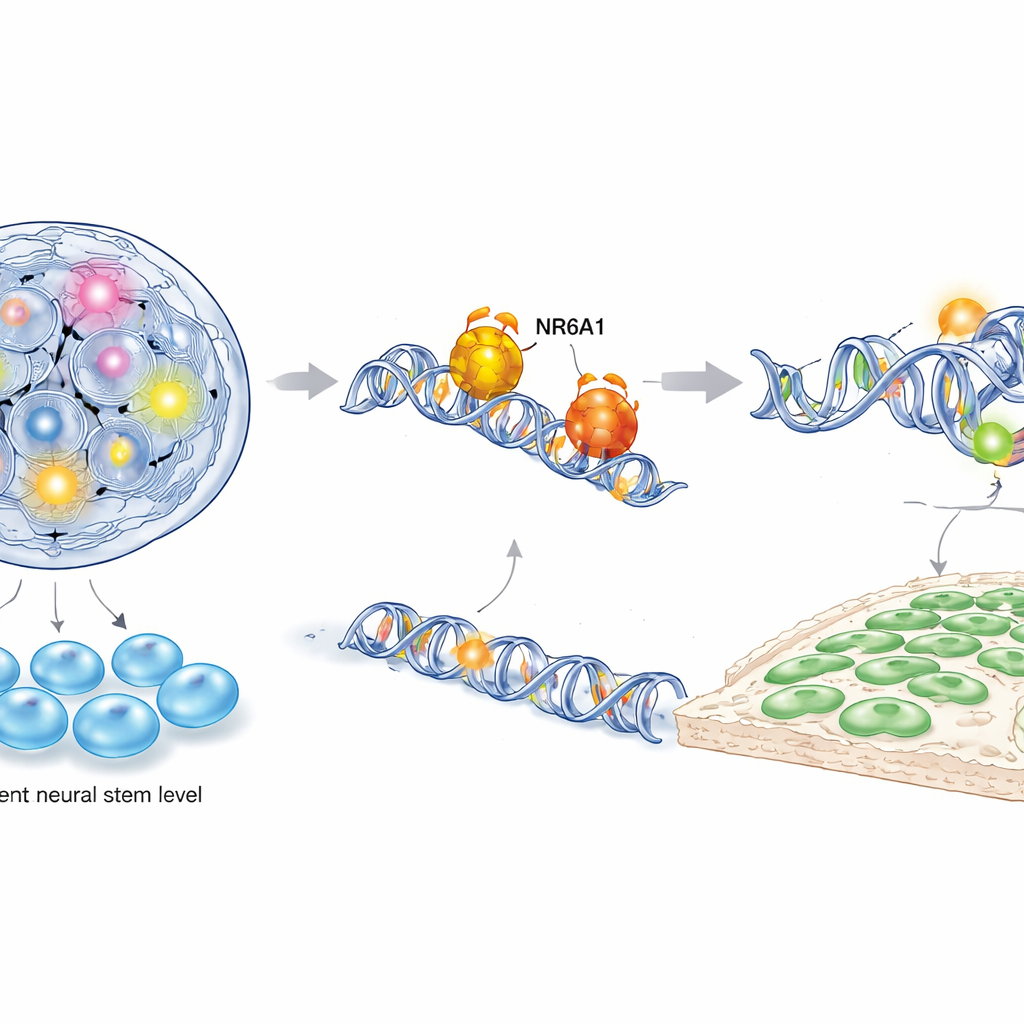
De tijdlijn van vroege ontwikkeling herschrijven
De studie herziet ook de kalender van wanneer neurale-kruin-cellen beginnen gespecificeerd te worden bij zoogdieren. Met een induceerbaar genetisch systeem om NR6A1 op verschillende tijdstippen te verwijderen, toonde het team aan dat het deleten ervan vóór of rond mid-gastrulatie—een stadium vroeger dan traditioneel werd aangenomen—al genoeg was om de activatie van neurale-kruin-genen te blokkeren. Ter vergelijking: het later verwijderen van NR6A1, ook met een veelgebruikte neurale-kruin-specifieke driverlijn, gaf geen duidelijke defecten. Dit betekent dat cruciale beslissingen over het neurale-kruinlot worden genomen voordat die standaardtools actief worden, wat verklaart waarom sommige eerdere muisstudies vroege vereisten mogelijk hebben gemist.
Waarom dit belangrijk is voor aangeboren afwijkingen en ziekte
Al met al onthult het werk NR6A1 als een centrale coördinator die neurale stamcellen helpt "op te groeien" tot neurale-kruin-cellen door gelijktijdig pluripotentieprogramma’s af te schakelen en migratie- en overlevingsprogramma’s in te stellen. Deze dubbele actie lijkt te beginnen tijdens mid-gastrulatie, eerder dan eerder erkend bij zoogdieren, en brengt de muisontwikkeling dichter bij die van andere gewervelden. Door te verduidelijken wanneer en hoe deze schakelaar werkt, biedt de studie een kader om eerdere genetische experimenten te herinterpreteren, betere hulpmiddelen te identificeren voor het bestuderen van neurale-kruin-biologie, en uiteindelijk neurocristopathieën te begrijpen en mogelijk te voorkomen die ontstaan wanneer deze vroege ontwikkelingsbeslissing misgaat.
Bronvermelding: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Trefwoorden: neurale-kruin-cellen, NR6A1, embryonale ontwikkeling, pluripotentie-schakelaar, neurocristopathie