Clear Sky Science · nl
Engineering the MmeFz2-ωRNA-systeem voor efficiënte genbewerking via een geïntegreerd computationeel-experimenteel kader
Kleinere genscharen voor grote medische problemen
Genbewerking heeft al veranderd hoe onderzoekers ziekten bestuderen, maar het omzetten van die technologie in veilige, praktische geneeskunde blijft een grote uitdaging. Een belangrijke hobbel is dat de krachtigste DNA-"scharen" van vandaag, zoals CRISPR-Cas9, fysiek groot zijn en moeilijk in de kleine afleveringsvoertuigen te verpakken die bij patiënten worden gebruikt. Deze studie introduceert een nieuw, compact gereedschap voor genbewerking gebaseerd op een weinig bekende enzymfamilie genaamd Fanzor2 en toont hoe kunstmatige intelligentie het snel kan herontwerpen tot een veelbelovende kandidaat voor toekomstige genetische therapieën.
Een nieuwe klasse compacte geneditors
De meeste huidige geneditors, zoals Cas9 en Cas12a, zijn omvangrijke eiwitten van meer dan duizend bouwstenen. Die grootte bemoeilijkt het inpakken in adeno-geassocieerde virussen (AAV's), het leidende afleveringssysteem voor gentherapieën. In tegenstelling hiermee zijn Fanzor2-eiwitten veel kleiner en komen ze van nature voor in eukaryoten, de levensgroep waartoe dieren en mensen behoren. De auteurs richtten zich op een lid van deze familie, MmeFz2, dat een kort RNA-molecuul gebruikt, ωRNA, om specifieke DNA-sequenties te vinden en door te snijden. Op papier leek MmeFz2 ideaal voor therapie: compact en programmeerbaar. In de praktijk was de activiteit in menselijke cellen echter teleurstellend, met minder dan één procent bewerkingsfrequentie op doelplaatsen. Het team zette zich in om dit onderpresterende enzym om te vormen tot een praktisch instrument.
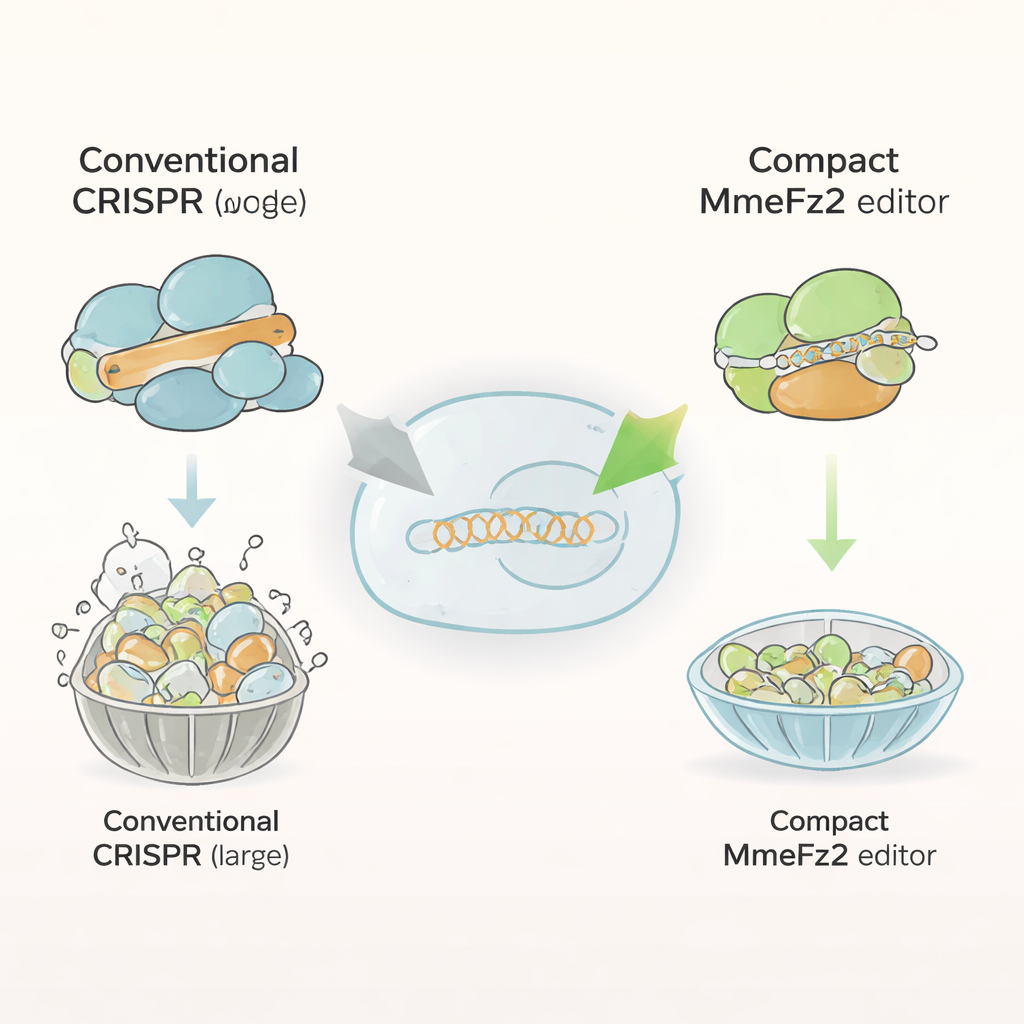
AI gebruiken om het gidsmolecuul te herontwerpen
Het eerste doelwit was het ωRNA, de gids die MmeFz2 vertelt waar te knippen. Met AlphaFold3, een geavanceerd programma dat 3D-structuren van eiwit–RNA–DNA-complexen voorspelt, bouwden de onderzoekers een model van MmeFz2 gebonden aan zijn ωRNA en een DNA-doel. Deze virtuele structuur toonde dat delen van het ωRNA slap waren, slecht gepaard en nauwelijks contact maakten met het eiwit. Geleid door deze informatie verving het team systematisch instabiele verbindingen in het RNA en verwijderde reeksen uridinebasen die de transcriptie kunnen verstoren. Vervolgens testten ze tientallen varianten in menselijke cellen. Door de beste wijzigingen te combineren en een overbodig stengeltje weg te knippen, creëerden ze een verkort ωRNA dat 30% kleiner was en toch bijna een 20-voudige verbetering in bewerkingsefficiëntie leverde over veel DNA-plaatsen.
Het eiwit fijnregelen met machine learning
Vervolgens verfijnte het team het eiwit zelf. Ze gebruikten opnieuw AlphaFold3 om in kaart te brengen waar MmeFz2 RNA en DNA aanraakte en ontwierpen meer dan honderd enkelvoudige aminozuurmutaties gericht op het versterken van die contacten of het verbeteren van flexibiliteit. Na screening van deze mutaties in cellen voerden ze de prestatiegegevens in EVOLVEpro, een machine-learningsysteem dat is gebouwd op eiwittaalmodellen getraind met miljoenen natuurlijke sequenties. Dit gereedschap leerde welke kenmerken doorgaans activiteit vergroten en stelde nieuwe combinaties van mutaties voor die naar verwachting nog beter zouden werken. Via een paar rondes van deze computationeel-experimentele cyclus kwamen de wetenschappers tot twee geoptimaliseerde enzymvarianten die, gecombineerd met het verbeterde ωRNA, de bewerkingsactiviteit meer dan 60-voudig verhoogden ten opzichte van het beginsysteem.
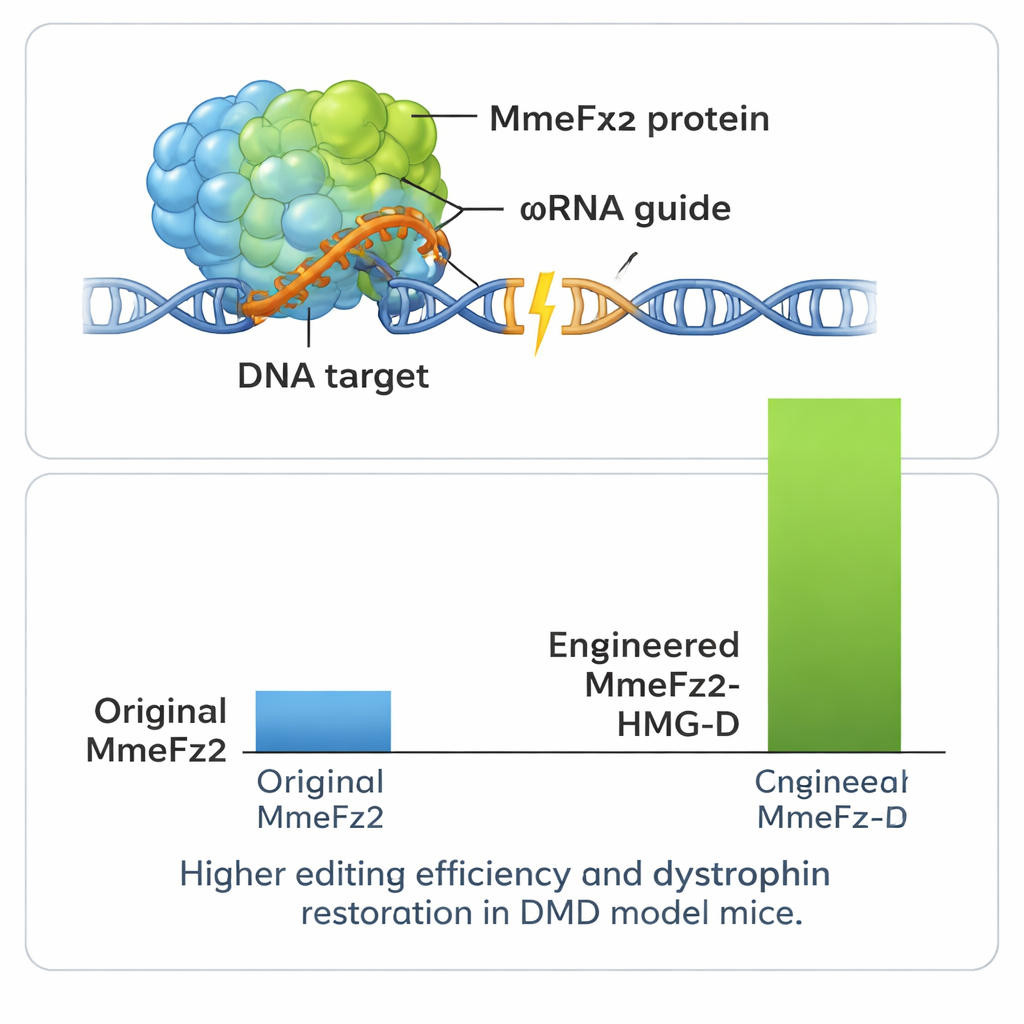
Meer vermogen en testen in een ziektemodel
Om nog meer prestaties uit het systeem te halen, fuseerden de auteurs MmeFz2 aan kleine DNA-bindende domeinen die eiwitten helpen zich aan genetisch materiaal vast te klampen. Een van deze, HMG-D genoemd, bleek bijzonder effectief wanneer het aan het uiteinde van het ontworpen enzym werd bevestigd en leverde bewerkingsniveaus boven 80% op sommige locaties. Belangrijk is dat testen op voorspelde off-target locaties in het genoom aangaven dat deze extra kracht niet gepaard ging met een groot verlies aan precisie. Omdat de hele geneditor — inclusief eiwit en gids-RNA — zo compact is, past hij comfortabel in een enkele AAV-vector, iets wat voor de meeste CRISPR-systemen niet mogelijk is. Het team zette dit voordeel in in een muismodel van Duchenne-spierdystrofie, een dodelijke, spierverslappende aandoening veroorzaakt door fouten in het dystrofine-gen. Een eenmalige injectie van de AAV-afgeleverde editor in de beenspier leidde tot detecteerbare correcties in het RNA van het gen en herstelde dystrofine-eiwit in een substantieel deel van de spiervezels.
Wat dit betekent voor toekomstige gentherapieën
Voor niet-specialisten is de kernboodschap dat de auteurs een zwak, obscure genknipenzym hebben getransformeerd tot een compact, hoogwaardig editor dat in één virale verpakking kan worden afgeleverd en een ernstige genetische ziekte in een realistisch diermodel kan herstellen. Even belangrijk is hoe ze daar kwamen: door AI-gebaseerde structuurvoorspelling en machine learning nauw te combineren met gerichte laboratoriumtests, verbeterden ze zowel het eiwit als het gids-RNA veel efficiënter dan met traditionele proef-en-foutbenaderingen. Deze geïntegreerde strategie kan de ontwikkeling van veel next-generation geneditors versnellen en preciezere en veiligere gentherapieën dichter bij patiënten met spierdystrofie en andere erfelijke aandoeningen brengen.
Bronvermelding: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Trefwoorden: genbewerking, alternatieven voor CRISPR, Duchenne-spierdystrofie, virale gentherapie, kunstmatige intelligentie in de biologie