Clear Sky Science · nl
Meerlandelijke genomische analyse benadrukt regionale choleraspreiding in Afrika
Waarom het volgen van ziekteverwekkers over grenzen heen belangrijk is
Cholera maakt nog steeds tienduizenden mensen per jaar ziek en veroorzaakt doden in Afrika, maar er blijven fundamentele vragen over hoe uitbraken beginnen, zich tussen landen verplaatsen en terugkeren. Deze studie brengt wetenschappers en volksgezondheidsteams uit zeven Afrikaanse landen samen om de bacterie die cholera veroorzaakt te volgen door zijn genetische code te lezen. Door honderden bacteriële genomen te vergelijken, laten de onderzoekers zien hoe recente choleragolven over grenzen heen zijn gevloeid, welke soorten stammen waar circuleren, en hoe deze kennis inspanningen kan verscherpen om toekomstige epidemieën te stoppen.
Een continentbrede blik op cholera
Om verder te gaan dan verspreide casusrapporten startte de Africa Centres for Disease Control and Prevention een samenwerkingsverband genaamd het Cholera Genomics Consortium in Africa (CholGEN). Laboratoria in Kameroen, de Democratische Republiek Congo, Malawi, Mozambique, Nigeria, Oeganda en Zambia sequentieerden 763 hoogwaardige genomen van de Vibrio cholerae O1-bacterie, voornamelijk uit 2019 tot 2024. Dit is de grootste reeks cholera-genomen ooit binnen Afrika zelf gegenereerd. Door deze nieuwe genomen te plaatsen naast bijna 1.800 eerder gesequenceerde monsters uit Afrika en Azië, kon het team reconstrueren hoe recente Afrikaanse uitbraken passen in de langlopende wereldwijde cholerapandemie.
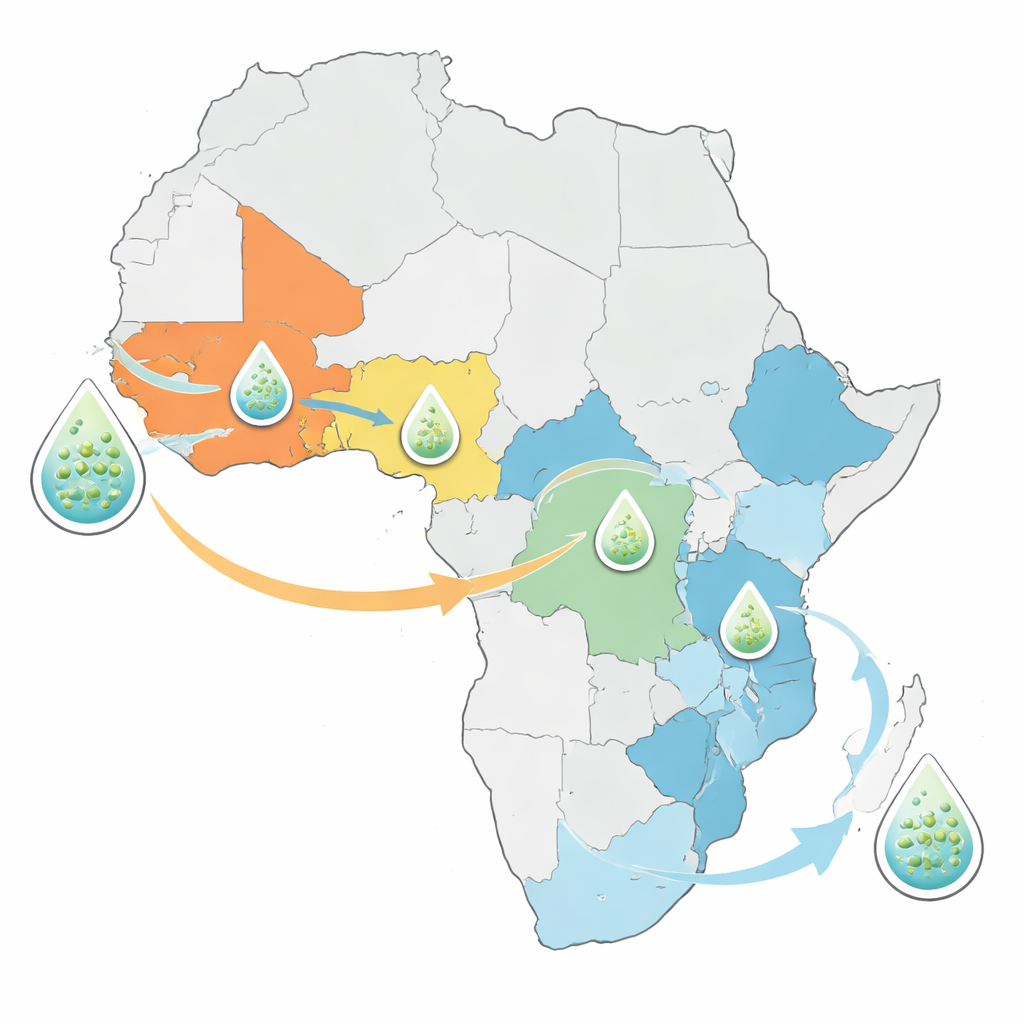
Oude stammen, nieuwe routes
De analyse toonde aan dat de cholerastammen die de huidige Afrikaanse uitbraken veroorzaken geen volledig nieuwe bedreiging vormen. In plaats daarvan stammen alle nieuw gesequenceerde bacteriën af van eerder bekende introducties van de zevende-pandemielijn van cholera die in 1970 voor het eerst vanuit Azië naar Afrika kwam. West- en Centraal-Afrikaanse landen zoals Nigeria, Kameroen en de Democratische Republiek Congo worden vaak gedomineerd door één of twee langdurige lijnen die al decennialang voortbestaan. Oost- en Zuid-Afrikaanse landen herbergen daarentegen een mix van meerdere lijnen tegelijk. Eén lijn in het bijzonder, aangeduid als AFR15, heeft zich de afgelopen jaren snel verspreid en is gekoppeld aan uitzonderlijk grote uitbraken in Malawi, Zambia en buurlanden, evenals aan epidemieën in delen van het Midden-Oosten en Zuid-Azië.
Grootte van uitbraken niet terug te voeren op genen alleen
Men zou kunnen vermoeden dat de explosieve verspreiding van AFR15 te wijten is aan grote genetische veranderingen die het gevaarlijker maken of beter in staat om behandeling te ontwijken. Echter, toen de onderzoekers de snelheid en het patroon van mutaties vergeleken in meerdere actieve lijnen, vonden ze geen opvallende verschillen. De bacteriën evolueerden met vergelijkbare snelheden, en het type mutaties en de betrokken genen zagen er over de lijnen heen grotendeels hetzelfde uit. Ook de algemene profielen van antibioticaresistentiegenen bleven grotendeels stabiel in de tijd en tussen landen. De belangrijkste uitzondering was Oeganda, waar bacteriën een groot mobiel DNA-element verworven—een plasmide—dat meerdere resistentiegenen draagt, waarschijnlijk geïmporteerd samen met stammen die gekoppeld zijn aan uitbraken in Jemen en Libanon. Zelfs dan vond de studie geen nieuwe genen die op zichzelf de ernst van recente Afrikaanse uitbraken zouden verklaren.
Verborgen reizen zichtbaar door beter bemonsteren
Aangezien de bacteriële genomen een spoor dragen van waar nauw verwante stammen zijn gevonden, kon het team afleiden hoe vaak cholera grenzen overschrijdt. Ze detecteerden veel voorbeelden van internationale verspreiding tussen buurlanden, inclusief herhaalde uitwisselingen tussen Zambia en de Democratische Republiek Congo. Maar bij nadere beschouwing zagen ze dat de statistische signalen van grensoverschrijdende sprongen het sterkst waren in jaren en regio’s met intensief bemonsteren. Dit suggereert dat de werkelijke bewegingen van cholera frequenter zijn dan de huidige gegevens laten zien; vele transmissiegebeurtenissen blijven waarschijnlijk onopgemerkt simpelweg omdat ergens geen bacteriën worden gesequenced. Om dit aan te pakken ontwikkelden de auteurs een kader om te schatten hoeveel nieuwe informatie een land wint door extra monsters te sequencen, waarbij genetische diversiteit, aantal introducties en bestaande data in balans worden gebracht.
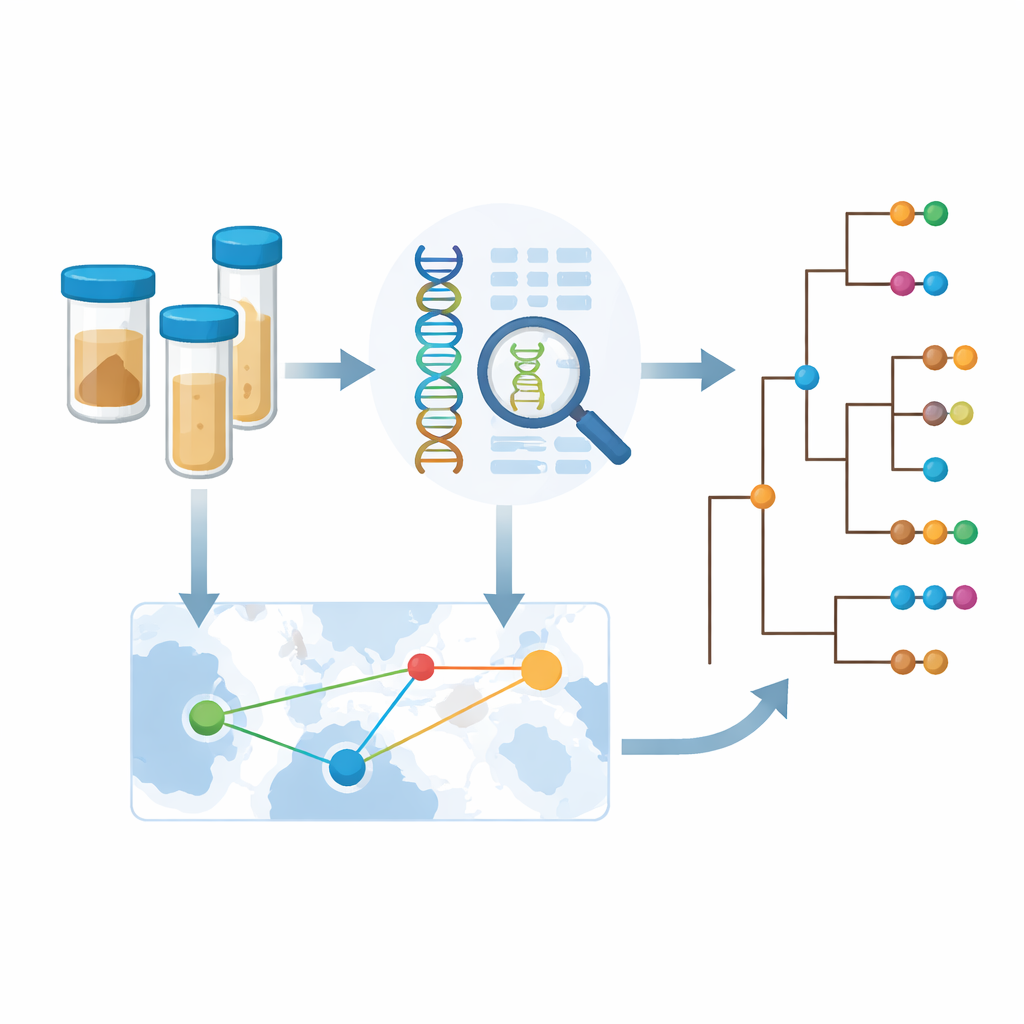
Genomics gebruiken om slimmer te bestrijden
De studie concludeert dat voor cholera in Afrika van vandaag de manier en plaats van verspreiding belangrijker zijn dan enige dramatische verandering in de bacterie zelf. De bevindingen pleiten voor routinegewijze, regionaal gecoördineerde genomische surveillance zodat buurlanden gezamenlijke uitbraken vroeg kunnen ontdekken, hun bronnen kunnen traceren en interventies zoals vaccinatiecampagnes, verbeteringen in water en sanitaire voorzieningen en reacties in grensgebieden efficiënter kunnen richten. Door sequentiecapaciteit op te bouwen binnen Afrikaanse volksgezondheidslaboratoria en data over grenzen heen te delen, bieden initiatieven zoals CholGEN een praktisch stappenplan om moderne genetica te gebruiken en dichter bij het ambitieuze doel te komen cholera als volksgezondheidsbedreiging tegen 2030 uit te bannen.
Bronvermelding: Mboowa, G., Matteson, N.L., Tanui, C.K. et al. Multicountry genomic analysis underscores regional cholera spread in Africa. Nat Commun 17, 2539 (2026). https://doi.org/10.1038/s41467-026-68642-7
Trefwoorden: cholera, genomische surveillance, Afrika, grensoverschrijdende transmissie, antimicrobiële resistentie