Clear Sky Science · nl
Metabole karakterisering van tumor‑immuuninteracties door multiplex immunofluorescentie onthult ruimtelijke mechanismen van immuuntherapie‑respons bij niet‑kleincellige longkanker (NSCLC)
Waarom dit onderzoek ertoe doet
Immuuntherapie heeft voor sommige mensen met gevorderde longkanker de behandeling veranderd, maar de meeste patiënten zien hun kanker nog steeds doorgroeien ondanks deze krachtige middelen. Deze studie stelt een eenvoudige maar cruciale vraag: kunnen we het kankergezwel zelf beter bestuderen — waar verschillende cellen zitten en hoeveel energie ze gebruiken — om te voorspellen wie echt baat heeft bij immuuntherapie? Door kleine biopsiemonsters om te zetten in gedetailleerde cellulaire kaarten, streven de onderzoekers ernaar de behandeling van longkanker dichter bij een werkelijk gepersonaliseerde aanpak te brengen.
Een longtumor bekijken als een stedenkaart
Het team onderzocht weefsel van 55 mensen met gevorderde niet‑kleincellige longcarcinomen (NSCLC) die behandeld werden met remmers van immuuncheckpoints, een belangrijke klasse immuuntherapiemiddelen. Voor de behandeling werden hun tumormonsters gekleurd met een paneel van 44 merkers via multiplex immunofluorescentie, waardoor veel eiwitten tegelijk zichtbaar werden. Een deep‑learningsysteem identificeerde vervolgens sleutelceltypen — zoals tumorcellen, T‑cellen, B‑cellen, macrofagen en fibroblasten — en classificeerde hun functionele toestand (bijvoorbeeld geactiveerd, delend of uitgeput) evenals hun metabole profiel, oftewel hoe ze energie produceren en gebruiken. In plaats van alleen cellen te tellen, brachten de onderzoekers ook in kaart waar cellen zich ten opzichte van elkaar bevonden, en creëerden ze buurtachtige regio’s binnen elke biopsie.
Energieverslindende tumoren en hun immuonomgeving
Een belangrijk aandachtsgebied was metabolisme — de manieren waarop cellen brandstof genereren om te groeien of ziekte te bestrijden. De onderzoekers definieerden “metabole buurten” met verschillende niveaus en typen energieverbruik, van lage activiteit tot sterk actieve zones rijk aan oxidatieve fosforylering en glycolyse. Ze ontdekten dat zowel tumorcellen als bepaalde immuuncellen, zoals macrofagen, vaak sterke energieproducerende routes vertoonden. Sommige van deze patronen waren verbonden met patiëntuitkomsten. Bijvoorbeeld, tumoren met hoge activiteit in routes die helpen aminozuren te gebruiken en de TCA‑cyclus aan te sturen, behoorden vaker tot patiënten die vroeg na immuuntherapie terugvielen. Daarentegen kwamen sommige plasmacellen (antistofproducerende B‑cellen) met actieve energiepaden binnen de tumor vaker voor bij patiënten die het beter deden, wat suggereert dat niet alle energierijke cellen schadelijk zijn — sommige kunnen effectieve antitumorimmuniteit ondersteunen.
Goede en slechte immuunspeelstukken in het tumorlanschap
Buiten eenvoudige aantallen speelde ook het type en gedrag van immuuncellen een rol. Macrofagen die het cytotoxische molecuul granzyme B droegen, waren sterk geassocieerd met slechtere progressievrije overleving, vooral wanneer ze werden aangetroffen in metabool lage of inactieve buurten. Deze regio’s kunnen voedingsarme of dormante gebieden vertegenwoordigen waar immuunaanvallen verzwakt zijn. Daarentegen leken bepaalde rangschikkingen van regulerende T‑cellen (Tregs) en fibroblasten op de grens tussen tumor en omliggend weefsel te correleren met betere uitkomsten, mogelijk reflecterend dat onderdrukkende cellen aan de randen worden gehouden in plaats van diep in de tumor door te dringen. Verhoudingen van verschillende immuuncellen, zoals granulocyten ten opzichte van CD8‑T‑cellen, correleerden ook met respons, wat benadrukt dat de immuunevenwicht en positionering — niet alleen absolute aantallen — belangrijk zijn.
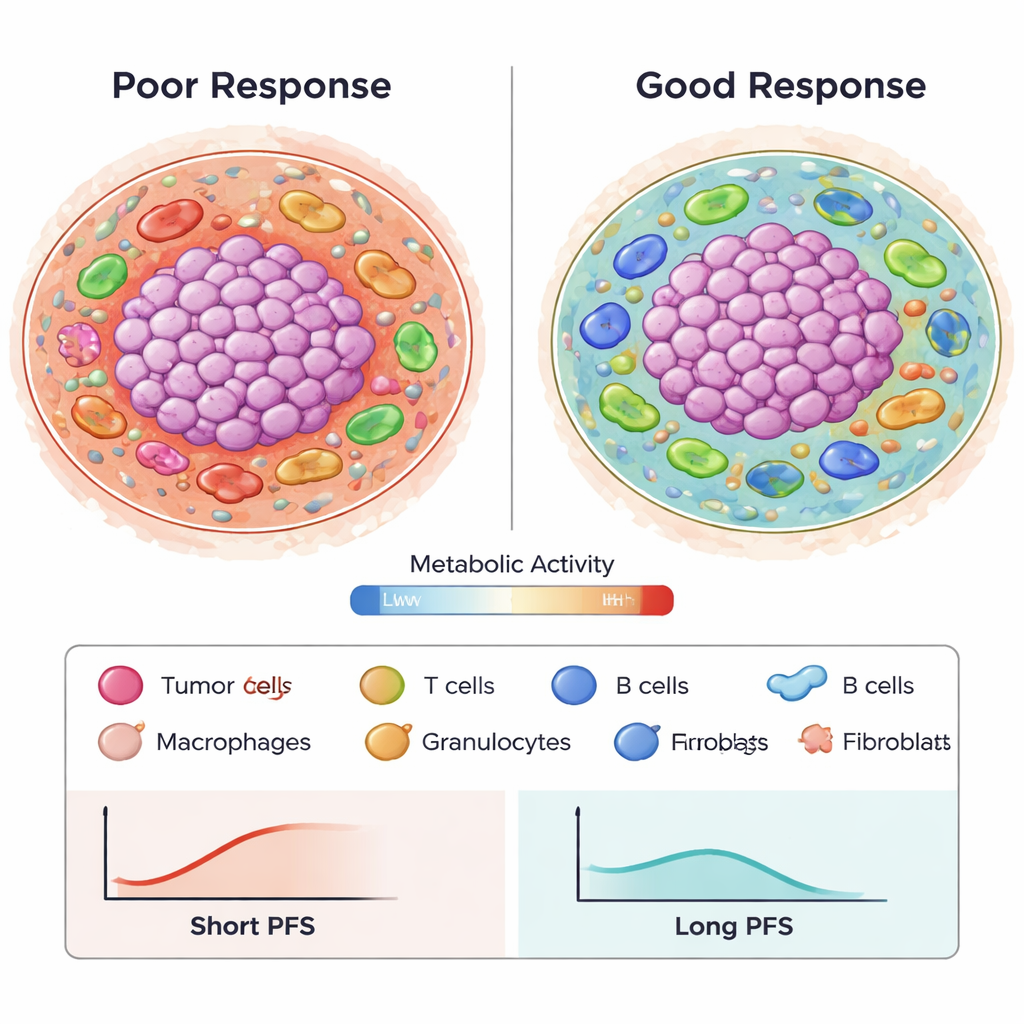
Van complexe beelden naar voorspellende patronen
Om inzicht te krijgen in meer dan een miljoen geconstrueerde ruimtelijke kenmerken die celtypen, afstanden en metabole toestanden beschrijven, gebruikten de auteurs een geavanceerde feature‑selectiemethode (Stabl) en overlevingsmodelleringstools. Ze identificeerden 87 sleutelkenmerken, waarvan veel weerspiegelen hoe metabool actieve tumorcellen interageren met macrofagen en T‑cellen, of hoe specifieke immuunceltypes clusteren nabij bloedvaten en fibroblasten. Met deze kenmerken in Cox‑regressiemodellen bouwden ze een voorspeller die de progressievrije overleving schatte met een nauwkeurigheid (AUC) rond 0,8 over 24 maanden, en die beter presteerde dan traditionele enkele merkers zoals PD‑L1‑kleuring of tumormutatielading in eerder gepubliceerde studies. Belangrijk is dat verschillende kenmerken reproduceerbaar waren in twee onafhankelijke patiëntcohorten, wat suggereert dat de patronen geen toeval zijn.
Wat dit voor patiënten betekent
Voor een leek is de kernboodschap dat waar cellen zich bevinden in een longtumor en hoe ze zichzelf van energie voorzien kan helpen verklaren waarom sommige patiënten goed reageren op immuuntherapie terwijl anderen dat niet doen. Deze studie toont aan dat rijke ruimtelijke en metabole informatie uit een routinematige biopsie, gecombineerd met kunstmatige intelligentie en statistische modellering, signaturen kan onthullen van waarschijnlijk voordeel of resistentie. Hoewel het werk validatie nodig heeft in grotere groepen en in volledige weefseldoorsneden, schetst het een pad naar toekomstige tests die artsen, vóór aanvang van de behandeling, kunnen vertellen welke patiënten waarschijnlijk duurzame controle door immuuntherapie zullen bereiken en welke mogelijk alternatieve of gecombineerde strategieën nodig hebben.
Bronvermelding: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Trefwoorden: immuuntherapieresistentie, niet‑kleincellige longkanker, tumormicro‑omgeving, ruimtelijke biologie, kankermetabolisme