Clear Sky Science · nl
G9a-gemedieerde H3K9me2 orkestreert regeneratie van het darmepitheel via epigenetische silencering van celdelingsgerelateerde genen
Waarom zelfherstel van de darm van belang is
Elke dag wordt het slijmvlies van je darm blootgesteld aan zware omstandigheden: maagzuur, voedseldeeltjes en biljoenen microben. Toch overleeft dit weefsel niet alleen, het herstelt zichzelf voortdurend. Wanneer dat herstelsysteem faalt — na bestraling, bij inflammatoire darmziekten of tijdens ernstige infecties — kunnen mensen pijn, bloedingen en levensbedreigende complicaties ondervinden. Deze studie onthult een verborgen "schakelaar" in darmcellen die hen helpt beslissen wanneer ze uit rust moeten komen en moeten gaan herstellen, en geeft aanwijzingen voor nieuwe behandelingen die het natuurlijke herstelvermogen van de darm kunnen versterken.
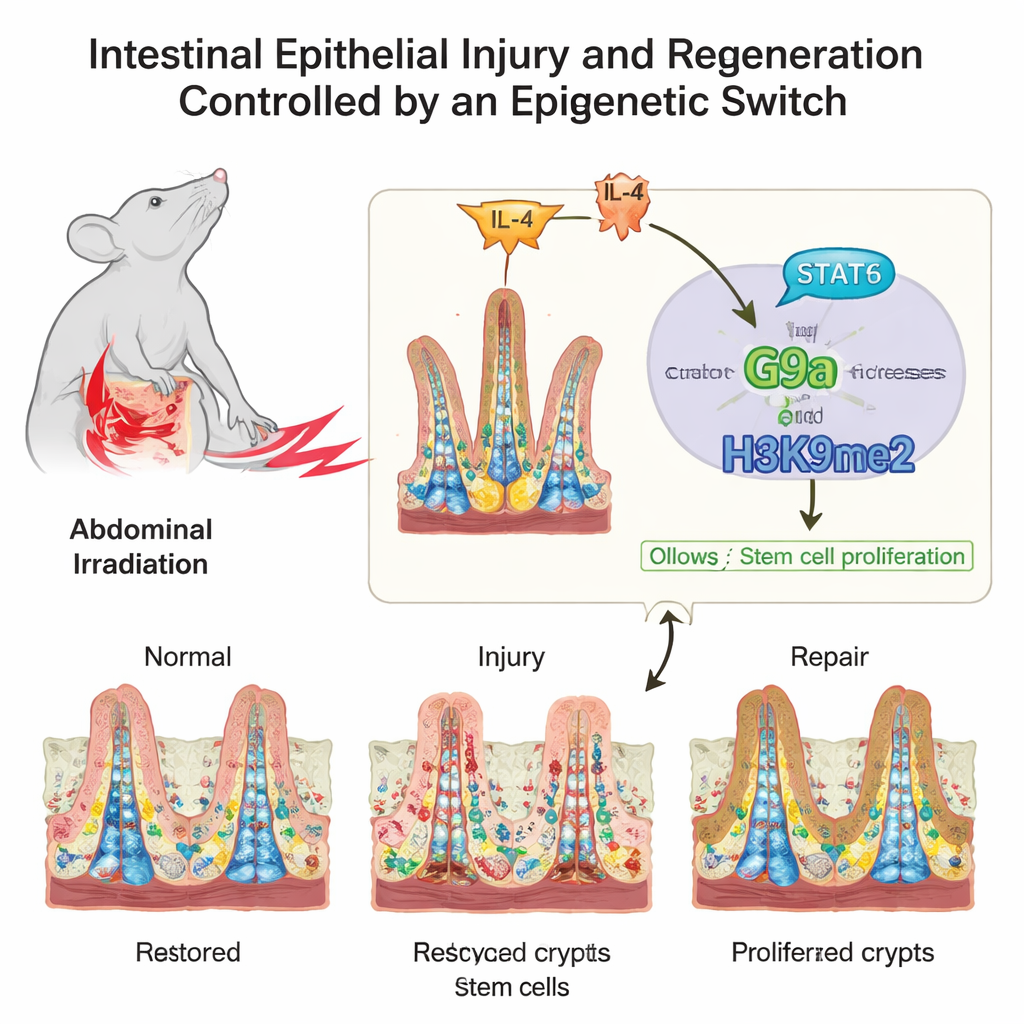
Een fragiele architectuur onder constante stress
Het binnenoppervlak van de darm lijkt onder de microscoop op een besnord tapijt, met vingervormige villi die voedingsstoffen opnemen en zakjes die crypten worden genoemd waar stamcellen wonen. Deze stamcellen, en hun snel delende dochtercellen, moeten een balans vinden tussen gelijkmatige vernieuwing en noodherstel. De auteurs concentreerden zich op hoe chemische labels op DNA-verpakkingsproteïnen, histonen genoemd, deze balans beïnvloeden. Deze labels veranderen de genen zelf niet, maar werken meer als dimmers die clusters genen hoger of lager zetten naarmate de darm van normaal functioneren naar beschadiging en terug naar gezondheid gaat.
Een epigenetisch merkteken dat schade en genezing volgt
Met muizen die aan bestraling waren blootgesteld — een veelvoorkomende oorzaak van darmbeschadiging tijdens kankerbehandeling — scanden de onderzoekers veel verschillende histonmerken in de stamcelrijke crypten. Eén merkteken, bekend als H3K9me2, steeg sterk toen de darm van beschadiging naar herstel overschakelde. Het 'schrijvende' enzym van dit merkteken, een eiwit genaamd G9a, toonde hetzelfde patroon. Het team onderzocht vervolgens menselijke monsters van patiënten die bekkenbestraling hadden gekregen, evenals mensen met de ziekte van Crohn. In beide situaties gingen hogere niveaus van H3K9me2 en G9a in darmcellen samen met betere aanwijzingen voor weefselherstel, wat suggereert dat dit systeem tussen muizen en mensen bewaard blijft.
Als de herstel‑schakelaar kapot is
Om te testen of dit merkteken slechts een toeschouwer is of echt het herstel aanstuurt, verwijderden de wetenschappers G9a specifiek uit het darmslijmvlies van muizen, of blokkeerden ze de activiteit ervan met een geneesmiddel. In beide gevallen daalden de niveaus van H3K9me2. Na bestraling of chemische beschadiging verloren deze muizen meer gewicht, hadden ze kortere en sterker beschadigde darmen, en lieten ze minder regenererende crypten en stamcellen zien dan normale dieren. Zelfs zonder opzettelijke verwonding zag het darmslijmvlies van G9a-deficiënte muizen er onderontwikkeld uit: crypten waren ondieper, villi korter en het aantal stamcellen en hun gespecialiseerde nakomelingen daalde. Kleine "mini-darmen" gekweekt uit deze cellen in een schotel groeiden ook slecht, wat onderstreept dat dit moleculaire systeem centraal staat voor de dagelijkse vernieuwing van de darm.
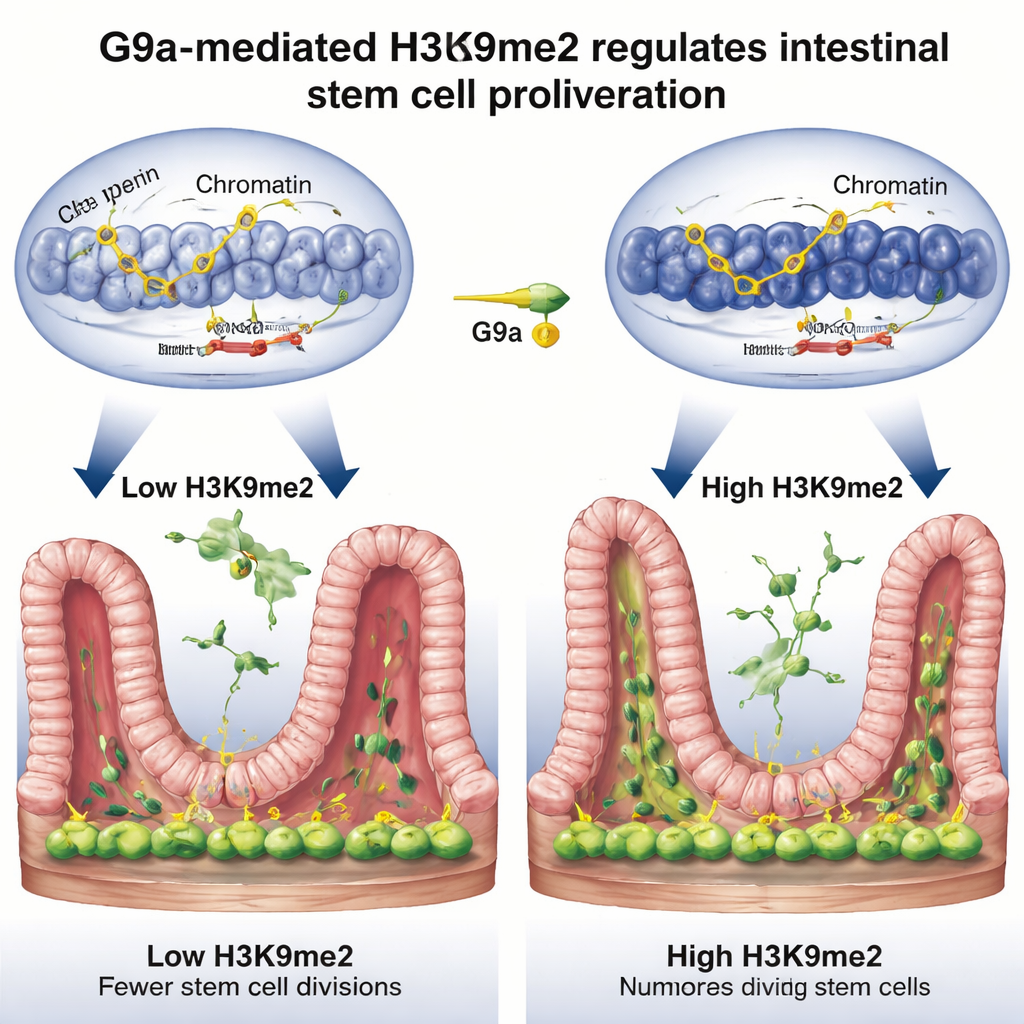
De rem op celdeling loslaten
Dieper gravend vroeg het team welke genen door deze herstel‑schakelaar worden gecontroleerd. Door drie krachtige genoomwijde methoden te combineren, vonden ze dat H3K9me2, aangebracht door G9a, de neiging heeft te zitten op stukken DNA die normaal fungeren als remmen op de celcyclus — genen zoals Rb1cc1, Rb1, Cdkn1a en Pten, die de celdeling vertragen of stoppen. Wanneer G9a ontbrak, verdween het chemische merkteken van deze regio's, opende het omringende DNA zich en werden deze remgenen sterker aangezet, wat leidde tot trage proliferatie van stamcellen. Tijdens normaal herstel na beschadiging stegen de H3K9me2-niveaus bij deze genen, daalde hun activiteit en konden stamcellen vrijer delen en het slijmvlies herstellen. In wezen laten G9a en H3K9me2 tijdelijk de "stop"-signalen verstommen zodat het weefsel kan teruggroeien.
Een signaleringsketen van immuunprikkels naar herstel
De darm handelt niet alleen; hij luistert voortdurend naar signalen van het immuunsysteem. De onderzoekers traceerden één zodanig signaal stroomopwaarts van G9a. Na beschadiging namen de niveaus van de immuunboodschapper IL‑4 toe, wat de activatie van een eiwit genaamd STAT6 in darmcellen teweegbracht. Geactiveerde STAT6 bond direct aan het regelgebied van het G9a-gen en verhoogde de productie ervan. Dit creëerde een keten van bevelvoering: IL‑4 activeert STAT6, STAT6 zet G9a aan, en G9a voegt H3K9me2 toe om celdelingremgenen te onderdrukken, waardoor stamcellen zich kunnen uitbreiden en het beschadigde slijmvlies kunnen herstellen.
Wat dit betekent voor toekomstige behandelingen
Voor niet‑specialisten tonen deze bevindingen aan dat darmherstel niet alleen door genen wordt geleid, maar door omkeerbare chemische merken die fijnafstellen wanneer die genen worden gebruikt. De IL‑4–STAT6–G9a–H3K9me2-route werkt als een intern bedieningspaneel dat de rem op stamceldeling net lang genoeg versoepelt om te genezen, en daarna weer kan worden teruggezet. In de toekomst zouden therapieën die dit pad mild versterken — zoals geneesmiddelen of gengebaseerde instrumenten die G9a op het juiste moment en de juiste plek verhogen — patiënten kunnen helpen sneller te herstellen van bestralingsschade, opvlammingen van inflammatoire darmziekte of andere aandoeningen die het darmslijmvlies beschadigen, terwijl het risico op ongecontroleerde celgroei wordt geminimaliseerd.
Bronvermelding: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Trefwoorden: darmregeneratie, epigenetica, stamcellen, histonmethylatie, inflammatoire darmziekte