Clear Sky Science · nl
Dual-functionele quorum-sensing signaalsynthases DspII en DspI coördineren de virulentieschakelaar in Pseudomonas aeruginosa
Hoe een ziekenhuis-superbug zijn aanvalstactiek verandert
Pseudomonas aeruginosa is een berucht ziekenhuisbacterie die hardnekkige long- en wondinfecties kan veroorzaken, vooral bij kwetsbare patiënten. De bacterie overleeft door te schakelen tussen twee levenswijzen: een beschermde, langzaam delende gemeenschap die een biofilm vormt, en een snelbewegende, agressieve vorm die weefsels binnendringt. Deze studie onthult hoe de bacterie zelf beslist wanneer ze uit een langdurige biofilm breekt en een plotselinge acute aanval inzet, en maakt daarmee potentiële nieuwe kwetsbare plaatsen voor toekomstige behandelingen zichtbaar.
Een microbieel leven tussen verbergen en aanvallen
Veel bacteriële infecties verlopen in fasen. In een vroeg stadium verspreiden vrijzwemmende cellen zich door het lichaam en zetten krachtige middelen in die het gastheerweefsel beschadigen. Later nestelen ze zich vaak in biofilms—dikke, slijmerige lagen die aan oppervlakken blijven kleven zoals katheters, longweefsel of wonden. In deze gemeenschappen zitten de cellen ingekapseld in een beschermend matrix die ze moeilijk te doden maakt met antibiotica of immuunresponsen. Biofilms zijn echter geen doodlopende weg. Cellen kunnen vertrekken, hun beweeglijkheid terugkrijgen en elders nieuwe uitbarstingen van acute infectie veroorzaken. Tot nu toe was onduidelijk hoe Pseudomonas aeruginosa actief deze verschuiving van chronische persistentie terug naar agressieve ziekte coördineert.
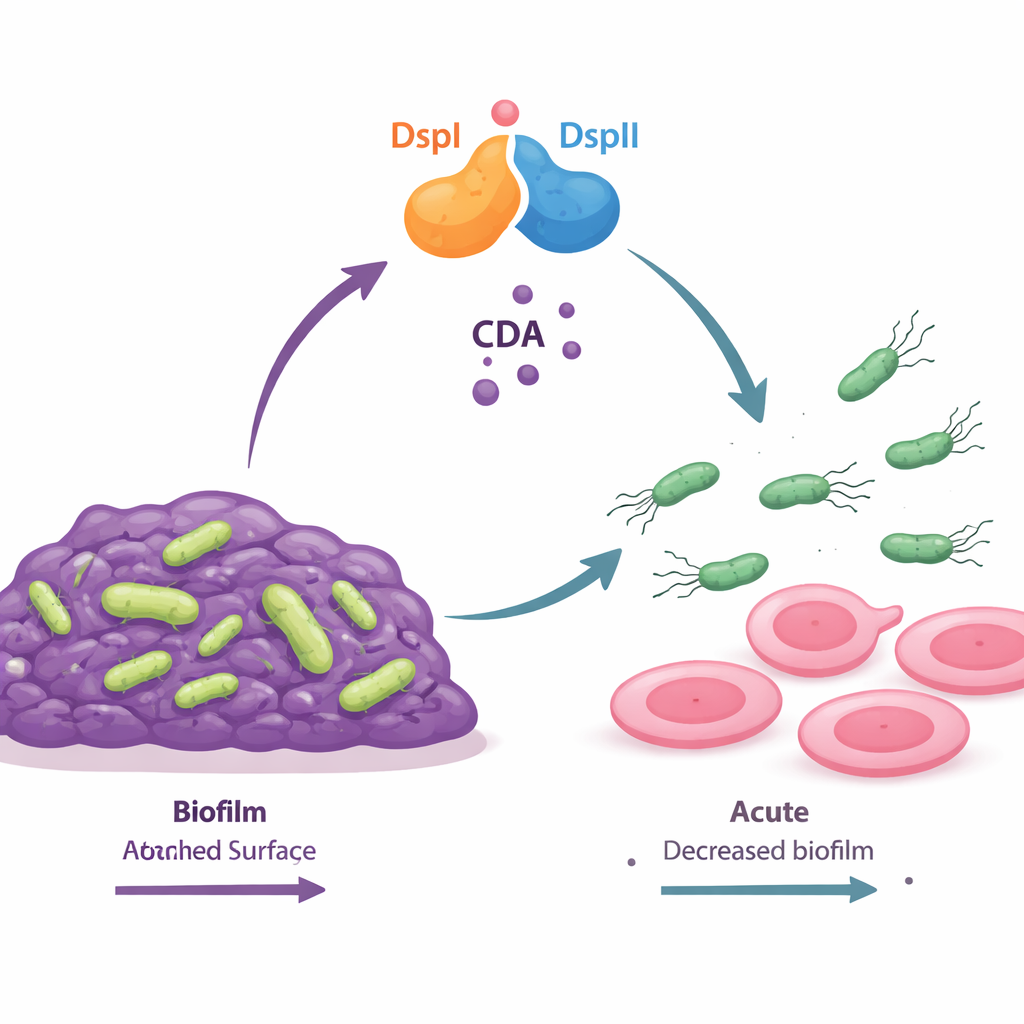
Een tweeeiwit-schakelaar die een chemisch "ga"-signaal maakt
De auteurs ontdekten dat twee bacteriële eiwitten, DspI en DspII genoemd, samenwerken als een soort moleculaire schakelaar. Beide zijn enzymen van hetzelfde algemene type en liggen naast elkaar in het bacteriële genoom; ze worden samen aan gezet naarmate de populatie dichter wordt. Wanneer ze een paar vormen, maken ze een klein vetzuursignaal genaamd cis-2-decenoïnezuur (CDA), behorend tot een bredere groep communicatiemoleculen bekend als DSF-signalen. Mutante bacteriën die ofwel DspI of DspII misten, konden geen CDA meer produceren, vormden ongewoon dikke biofilms en verloren hun vermogen om over oppervlakken te schwermen. Alleen wanneer beide eiwitten samen hersteld werden, herwonnen de cellen normale signaalproductie, biofilmafbraak en beweeglijkheid, wat aantoont dat de twee enzymen als een onderling afhankelijke team functioneren.
Van chemisch signaal naar beweging en ontsnapping
CDA werkt niet op zichzelf; het sluit aan op de interne bedrading van de bacterie. Het team toonde aan dat CDA de niveaus van een ander boodschapper-molecuul, cyclisch di-GMP, verlaagt door de activiteit te verhogen van een specifiek enzym genaamd RbdA dat deze boodschapper afbreekt. Hoge cyclisch di-GMP-niveaus stimuleren normaal gesproken biofilmvorming door de productie van suikerrijke matrix te bevorderen en flagellen, de kleine schroeven die het zwemmen aandrijven, te onderdrukken. Wanneer CDA aanwezig is, dalen de cyclisch di-GMP-niveaus, verschuift een regulator genaamd FleQ van stand, neemt de kleverige suikerproductie af en worden flagellen verlengd en versterkt. Daardoor verslappen biofilms en herstellen cellen hun vermogen om weg te bewegen en nieuwe gebieden te koloniseren.
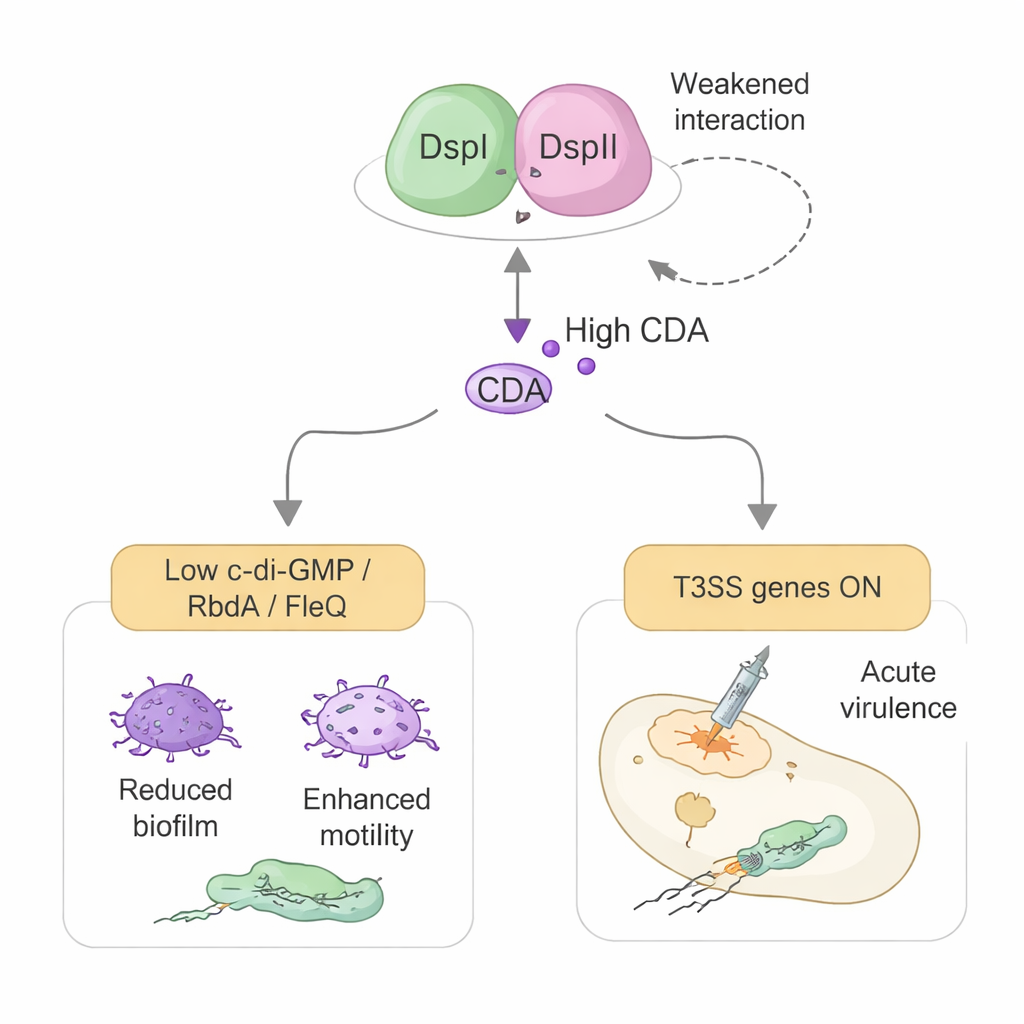
Het herbedraden van het bacteriële wapensysteem
De studie onthult ook een tweede, onverwachte rol voor DspI en DspII die verder gaat dan chemie. Hetzelfde eiwitpaar helpt bij het inschakelen van het type III-secretiesysteem (T3SS) van de bacterie, een spuitachtig apparaat dat wordt gebruikt om toxines rechtstreeks in gastheercellen te injecteren. In plaats van te handelen via CDA werkt dit effect via directe controle van genetische schakelaars. DspI en DspII dempen de productie van twee kleine regulerende RNA's, RsmY en RsmZ, die normaal gesproken de eiwitproductie van het T3SS uitschakelen. Ze doen dit door te binden aan het DNA-controlegebied van één RNA en fysiek te interageren met een hoofdregulator-eiwit genaamd GacA. Wanneer RsmY en RsmZ in toom worden gehouden, komt een downstream activator genaamd RsmA vrij, en worden de genen voor het T3SS en zijn hoofdcontroller ExsA aangezet, wat leidt tot verhoogde cytotoxiciteit in celkweek en dodelijkheid in een insectinfectiemodel.
Een zelfafstemmend systeem met medicijndoelen
Vindingrijk is dat de sterkte van de DspI–DspII-partnership en hun controle over virulentie zelf wordt bijgesteld door CDA-niveaus. Bij lage concentraties—zoals verwacht bij cellen die net een biofilm verlaten—versterkt CDA de interactie tussen de twee eiwitten en bevordert het meer signaalproductie en T3SS-activatie. Bij hoge concentraties binnen dichte biofilms verzwakt CDA hun interactie en vermindert het hun binding aan DNA, waardoor verdere signaalsynthese en de kostbare productie van wapens in achterblijvende cellen wordt beperkt. Deze dubbele rol maakt het DspI–DspII-complex tot een centraal knooppunt dat populatiegrootte, biofilmontsnapping en acute virulentie koppelt. Omdat het verstoren van het complex zowel signaalproductie als toxinesysteemactivatie kan blokkeren, vormt het een aantrekkelijk doelwit voor toekomstige geneesmiddelen die Pseudomonas in een minder schadelijke, chronische staat zouden kunnen houden en gevaarlijke opschommelingen zouden voorkomen.
Bronvermelding: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Trefwoorden: Pseudomonas aeruginosa, biofilmdispersie, quorum sensing, virulentieschakelaar, cis-2-decenoïnezuur