Clear Sky Science · nl
Dynamische handtekening van de activiteit‑stabiliteitswisseling in de evolutie van lactamase
Waarom dit belangrijk is voor antibioticaresistentie
Antibioticaresistentie lijkt vaak een zwarte doos: bacteriën veranderen op de een of andere manier en geneesmiddelen stoppen met werken. Deze studie opent die doos voor een van de bekendste resistentie-enzymen ter wereld, TEM‑1 β‑lactamase, dat bacteriën helpt penicillineachtige antibiotica af te breken. Door te volgen hoe de vorm en bewegingen van dit enzym veranderen terwijl het evolueert om nieuwere middelen aan te vallen, laten de auteurs zien waarom mutaties die de activiteit verhogen vaak de stabiliteit verzwakken, en hoe evolutie slimme manieren vindt om beide in balans te brengen.
Van penicilline‑breker naar breder drugs‑vernietiger
TEM‑1 is oorspronkelijk uitstekend in het afbreken van oudere penicillineantibiotica maar slecht in het aanpakken van nieuwere, omvangrijkere middelen zoals cefotaxime. In veel klinische stammen verschijnt een enkele sleutelmutatie, G238S, vlak bij het actieve centrum van het enzym, het pocket waar antibiotica worden geknipt. Deze mutatie verbetert dramatisch het vermogen van het enzym om cefotaxime te vernietigen, terwijl de oorspronkelijke activiteit tegen penicilline slechts bescheiden wordt aangetast. De auteurs tonen aan dat G238S het pocket niet simpelweg verwijdt; het herschikt hoe meerdere omliggende lussen en helices bewegen, waardoor een nieuwe functionele conformatie ontstaat die grovere geneesmiddelen beter kan herbergen.
Eiwitbeweging als evolutionaire afstemmingsknop
Met geavanceerde nucleaire magnetische resonantie (NMR)-technieken maten de onderzoekers hoe verschillende delen van TEM‑1 bewegen op tijdschalen variërend van biljoensten tot duizendsten van een seconde. Wild‑type TEM‑1 is tamelijk stijf, wat helpt bij het efficiënt verwerken van zijn oorspronkelijke substraten. G238S laat het grootste deel van deze snelle stijfheid intact maar introduceert tragere, zorgvuldig afgestemde bewegingen in veel wanden van het actieve centrum. Deze bewegingen zijn snel genoeg om gelijke tred te houden met de chemie van het enzym en toch niet zo wild dat ze kritische katalytische residuen verstoren. Het resultaat is een “geoptimaliseerd venster” van flexibiliteit: precies genoeg beweging om het pocket voor cefotaxime te openen, terwijl de kernchemie goed gealigneerd blijft.
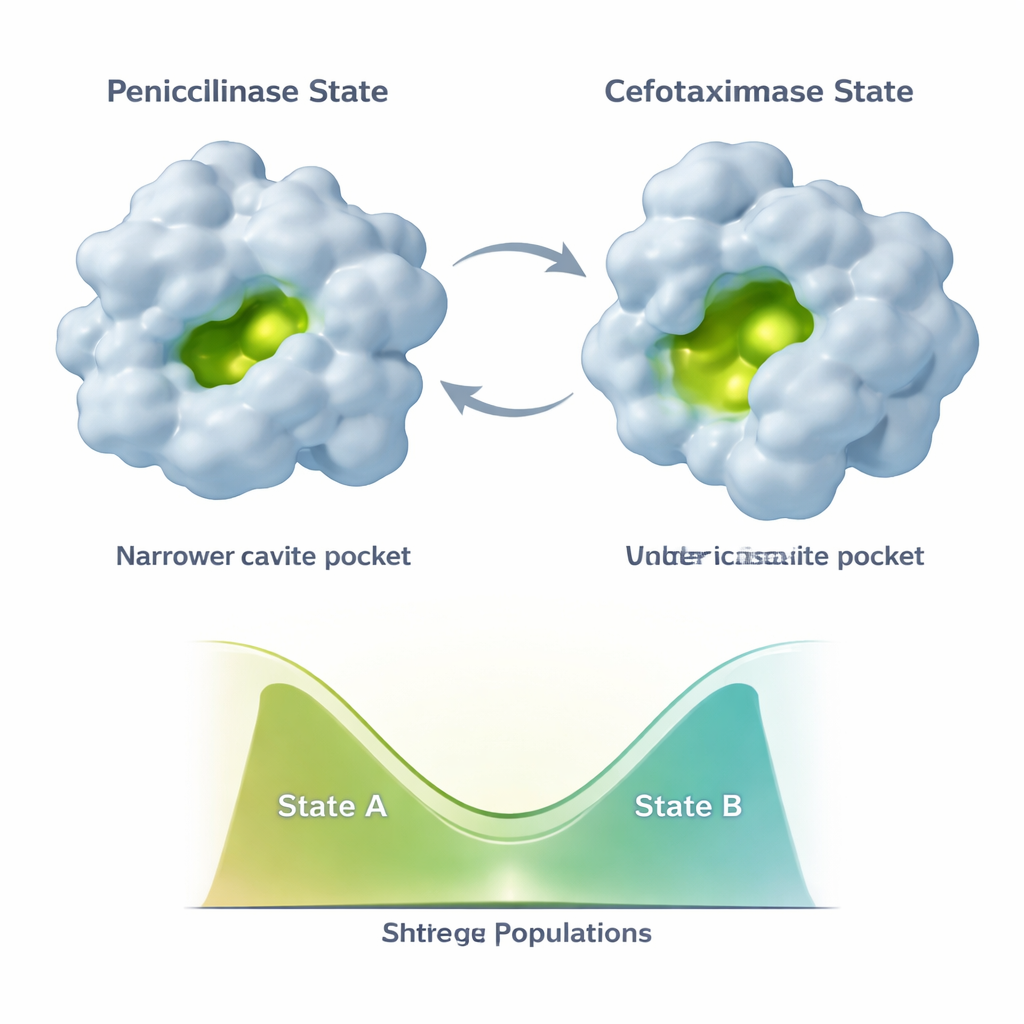
Twee vormen in balans in plaats van één kiezen
Evolutie bevriest TEM‑1 niet in één nieuwe vorm. In plaats daarvan doorloopt het enzym ten minste twee hoofdconformaties: een “penicillinase”-toestand die lijkt op de oorspronkelijke structuur en een meer open “cefotaximase”-toestand die beter geschikt is voor nieuwere middelen. Extra mutaties die later optreden, zoals E104K en A42G, doen iets subtiels. In plaats van simpelweg de nieuwe, cefotaximase‑vriendelijke vorm stabieler te maken, brengen ze het evenwicht tussen de twee toestanden opnieuw in balans. NMR-gegevens tonen dat verschillende delen van het actieve centrum en het ondersteunende geraamte hun populaties onafhankelijk langs dit tweestatencontinuüm kunnen verschuiven. Dit leidt tot een combinatorische set van enzymvarianten, elk met een andere mix van penicilline‑achtige en cefotaxime‑achtige conformaties en dus verschillende katalytische profielen.
Verborgen zwakke plekken en reparaties op afstand
Mutaties die de activiteit verbeteren hebben vaak een verborgen prijs: ze maken het eiwit minder stabiel. In plaats van alleen naar volledige ontvouwing te kijken, bracht het team lokale stabiliteit in kaart op het niveau van korte segmenten met behulp van waterstof‑deuteriumuitwisseling gekoppeld aan massaspectrometrie. G238S bleek niet alleen nabijgelegen lussen te destabiliseren maar ook verre helices en beta‑sheetregio’s die een structureel ruggegraat vormen. Sommige van deze regio’s overlappen met een “cryptisch” allosterisch pocket—een zelden bezochte opening in de kern van het eiwit die kleine moleculen kan binden en de activiteit kan dempen. G238S maakt dit pocket makkelijker te openen, waardoor in feite een milde zelfremmende eigenschap in het enzym wordt ingebouwd. Latere mutaties, met name A42G, versterken dit verzwakte ruggraatnetwerk en verbeteren de lokale stabiliteit rond drie wisselwerkende helices zonder de voordelige dynamiek in het actieve centrum weg te nemen. Met andere woorden: evolutie plakt verafgelegen structurele zwakke plekken dicht in plaats van de oorspronkelijke innovatie ongedaan te maken.
Wat de studie onthult over evolutiestrategie
Voor een niet‑specialist is de kernboodschap dat eiwitten zoals TEM‑1 resistentie niet evolueren door een eenvoudige aan‑/uit‑schakelaar om te zetten. Elke mutatie verandert subtiel hoe het enzym ademt, buigt en zijn tijd verdeelt tussen verschillende werkhoudingen. G238S opent de deur naar een nieuwe taak—het afbreken van nieuwere antibiotica—maar creëert ook lokale kwetsbaarheden en een gedeeltelijk zelfremmende toestand. Secundaire mutaties werken als zorgvuldige versterkingen, stabiliseren het geraamte en verfijnen het evenwicht tussen oude en nieuwe conformaties zodat het enzym zowel actief als duurzaam kan blijven. Deze dynamische kijk op evolutie, waarbij bewegingen en lokale zwaktes net zoveel betekenen als de statische structuur, kan helpen bij het ontwerpen van toekomstige antibiotica en enzym‑gerichte geneesmiddelen die moeilijker door bacteriën te omzeilen zijn.
Bronvermelding: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
Trefwoorden: antibioticaresistentie, beta-lactamase, eiwitevolutie, enzymdynamica, eiwitstabiliteit