Clear Sky Science · nl
Een ruimtelijk gedetailleerde atlas van maagkanker karakteriseert een lymfocyt-geaggregeerde regio
Waarom de buurt rond een tumor ertoe doet
Kanker is niet slechts een hoop losgeslagen cellen; het leeft in een drukke buurt van immuun- en structurele cellen die de tumor kunnen helpen bestrijden of juist ongemoeid kunnen laten groeien. Deze studie brengt die buurt in maagkanker in kaart met ongekende detailnauwkeurigheid en toont hoe kleine immuun-hotspots en koude plekken binnen dezelfde tumor kunnen beïnvloeden of een patiënt reageert op moderne immunotherapieën.
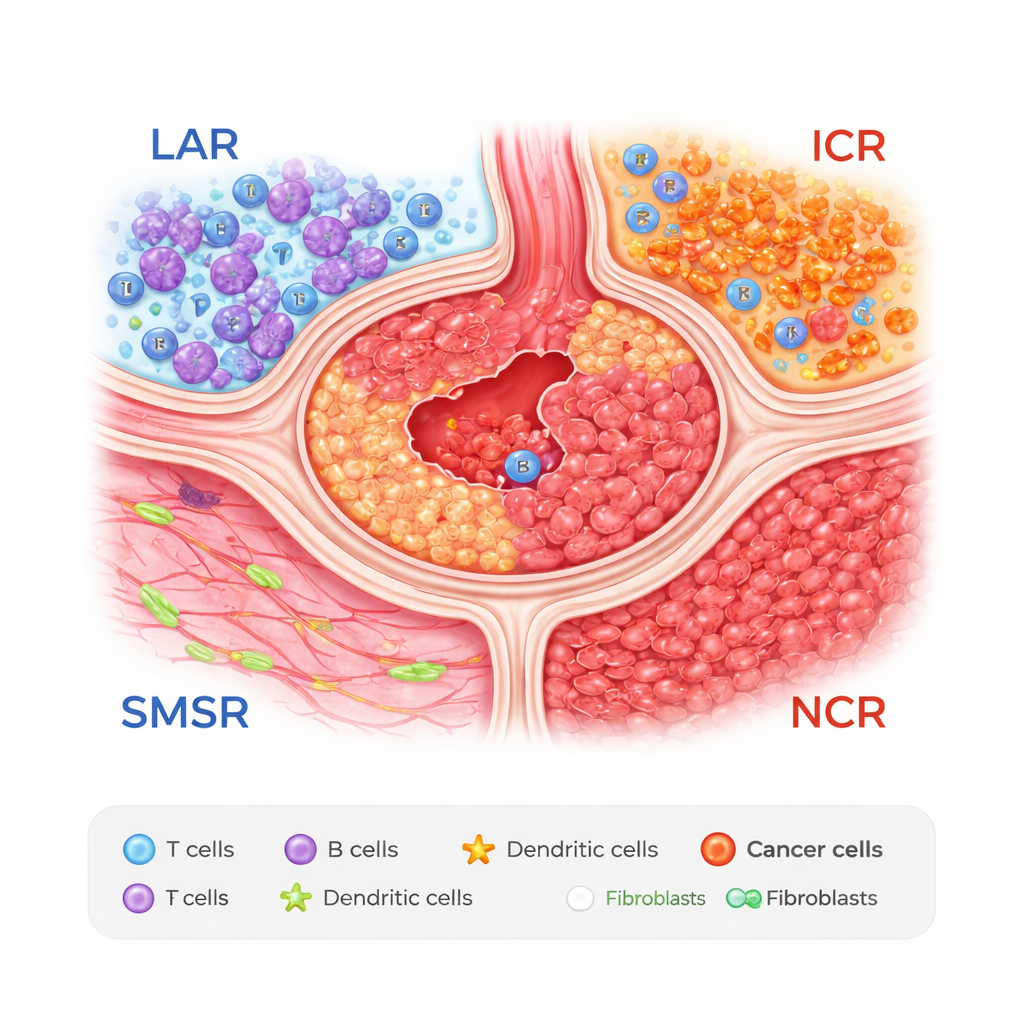
Vier zones binnen een maagtumor
De onderzoekers combineerden twee krachtige technieken: single-cell RNA-sequencing, waarmee genactiviteit in individuele cellen wordt afgelezen, en ruimtelijke transcriptomica, die vastlegt waar die cellen zich bevinden in weefselsneden. Bij onderzoek van monsters van 27 patiënten ontdekten ze dat maagtumoren in vier terugkerende zones zijn te verdelen. Eén zone is een lymfocyt-geaggregeerde regio (LAR), rijk aan clusters van T- en B-cellen die doen denken aan miniatuur-lymfoïde knooppunten. Een andere is een gladde spier- en stromaregio (SMSR), gedomineerd door spier- en bindweefsel. De overige twee zones zijn kanker-dichte gebieden: een immunogene kankerregio (ICR), waar tumorcellen zich mengen met enkele beschermende maagceltypen, en een negatief-immunogene kankerregio (NCR), vol met kwaadaardige cellen en relatief weinig verdedigende immuuncellen.
Immuun-hotspots gekoppeld aan betere uitkomsten
Het team vond dat de LAR-zone verrijkt is voor genen die normaal in lymfeklieren worden gezien, waar immuuncellen worden opgeleid en geactiveerd. Daartoe behoren signalen die helpen lymfocyten aan te trekken en ze te organiseren in structuren die tertiaire lymfatische structuren worden genoemd. Bij analyse van grote openbare kanker-datasets hadden tumoren met hogere expressie van LAR-gerelateerde genen doorgaans een betere overleving van patiënten en een iets grotere kans om te reageren op immuun-checkpointtherapieën die de rem op T-cellen wegnemen. Daarentegen werden genhandtekeningen uit spierrijke of zwaar kankerrijke regio’s meestal geassocieerd met slechtere uitkomsten in meerdere kankertypes.
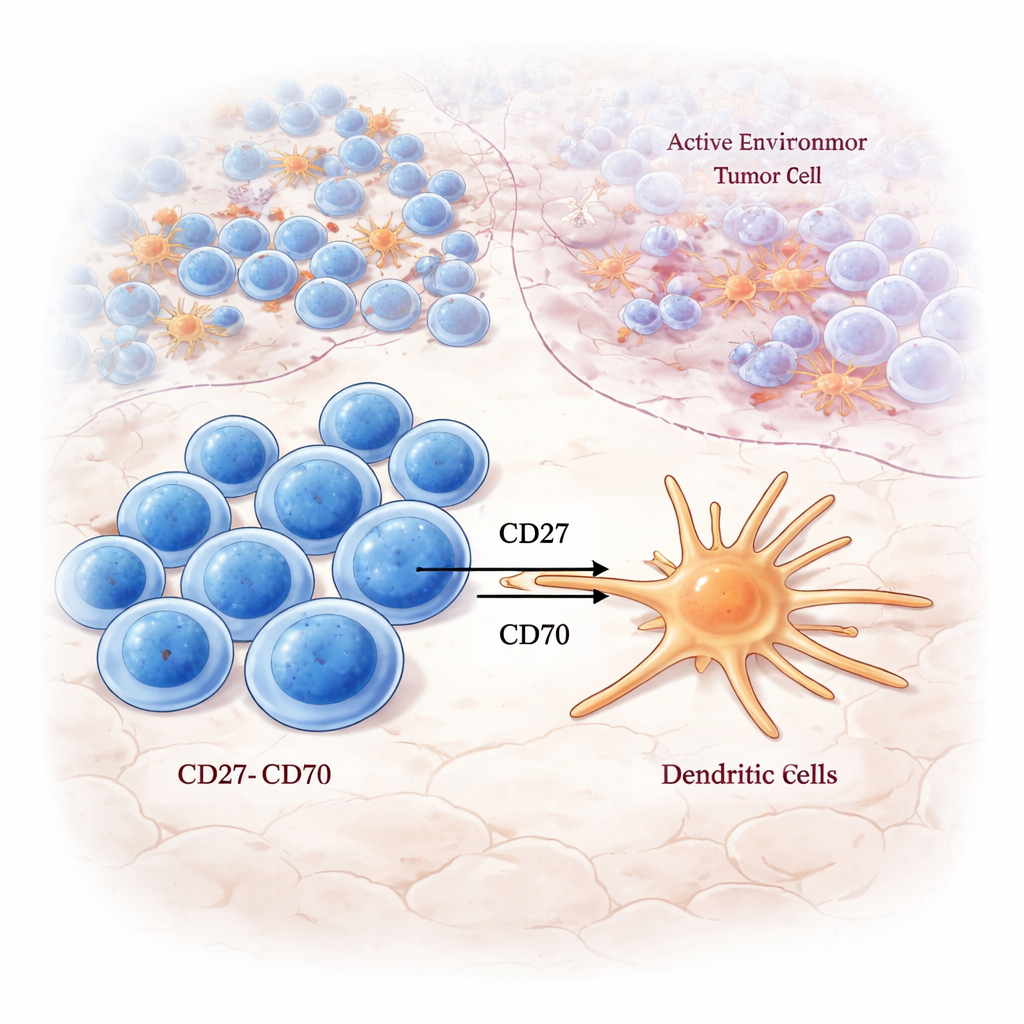
Waar naïeve T-cellen leren vechten
Bij nadere bestudering van de LAR zagen de auteurs sterke activiteit in signaalroutes die centraal staan bij het wakker maken van T-cellen: T-celreceptorsignalisatie, kostimulatiepaden en antigeenverwerking. Naïeve CD8-T-cellen—cellen die zich nog niet volledig hebben gespecialiseerd om een specifiek doelwit aan te vallen—hingen bijzonder samen met deze activatiesignalen binnen de LAR, maar niet elders. Met multikleurkleuring detecteerden ze CD8-T-cellen in de LAR die merkers van zowel vernieuwing als proliferatie droegen, wat suggereert dat deze regio functioneert als een lokale trainings- en expansiezone waar verse tumorbestrijdende cellen worden voorbereid.
Twee varianten van immuurnabijheid
Niet alle LAR’s waren gelijk. Toen de onderzoekers patiënten groepeerden op basis van de cellulaire samenstelling van hun LAR’s, onthulden ze twee patronen. In “Groep A”-tumoren leken LAR’s sterk op klassieke lymfeklieren, rijk aan gespecialiseerde B-cellen en dendritische cellen, en de kankergedeelten naast deze LAR’s zaten vol met geactiveerde, strijdklare lymfocyten. In “Groep B” waren LAR’s minder ontwikkeld en bevatte het aangrenzende kankergewebe meer rustende, minder betrokken T-cellen. Geavanceerde computationele analyse van weefselbeelden bevestigde dat geactiveerde immuuncellen fysiek clusteren nabij deze meer rijpe LAR’s, wat suggereert dat de lokale architectuur kan sturen hoe krachtig het immuunsysteem de tumor aanvalt.
Checkpoint-signalen in de ruimte
De studie bracht ook in kaart waar immuun-"schakelaars" die bekendstaan als checkpointmoleculen tot expressie komen. Stimulerende paren zoals CD27–CD70 concentreerden zich in de LAR, vooral in tumoren van Groep A, en verbinden uitgeputte maar tumorreagerende CD8-T-cellen met dendritische cellen die hun activiteit verder kunnen versterken. Daarentegen waren veel remmende checkpoint-paren, zoals TIGIT–NECTIN2 en LAG3–LGALS3, verrijkt in de NCR, de meest kankerrijke zone. Dit suggereert dat zelfs wanneer T-celreceptorsignalisatie aanwezig is, het omringende checkpoint-landschap de lokale immuniteit kan kantelen richting aanval of onderdrukking, afhankelijk van de tumorregio.
Wat dit voor patiënten betekent
Voor niet-specialisten is de kernboodschap dat waar immuuncellen en signalen zich binnen een tumor bevinden even belangrijk kan zijn als hoeveel er zijn. Dit werk toont aan dat maagkankers onderscheiden immuurnabijheden bevatten, en dat robuuste, op lymfeklieren lijkende regio’s nabij de tumor geassocieerd zijn met actievere, gunstiger gepositioneerde T-cellen en betere uitkomsten. Door deze lymfocyt-geaggregeerde regio’s te herkennen en mogelijk te versterken, zouden toekomstige therapieën beter kunnen worden afgestemd—door geneesmiddelen, combinaties of zelfs gerichte toedieningsbenaderingen te kiezen die de interne immuunbolwerken van de tumor benutten.
Bronvermelding: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Trefwoorden: maagkanker, tumormicro-omgeving, tertiaire lymfatische structuren, ruimtelijke transcriptomica, kankerimmunotherapie