Clear Sky Science · nl
Het uitbreiden van het payload-spectrum bij antilichaam–drugconjugaten door bezorging van hydroxy-bevattende geneesmiddelen via zelf-immolerende fosforamidaten
Slimmere raketten tegen kanker
Kankergeneesmiddelen kunnen buitengewoon krachtig zijn, maar werken vaak als carpetbombing: ze treffen gezonde weefsels bijna even hard als tumoren. Antilichaam–drugconjugaten (ADCs) zijn ontwikkeld om dit probleem te verhelpen door een krachtig middel aan een antilichaam te koppelen dat zich richt op kankercellen, waardoor de behandeling een geleide raket wordt. Dit artikel legt een nieuwe chemische “tussenplug” uit tussen antilichaam en geneesmiddel die deze raketten zowel preciezer als flexibeler maakt, en de deur opent voor veel meer typen kankermedicijnen dan ADCs van vandaag kunnen vervoeren.
Waarom hedendaagse gerichte geneesmiddelen nog beperkt zijn
ADCs bestaan uit drie delen: een antilichaam dat een merker op kankercellen herkent, een toxisch middel (de “payload”) en een chemische koppeling die ze samenbindt. De meeste goedgekeurde ADCs vertrouwen op slechts een paar soorten payloads die DNA beschadigen of de celdeling op vergelijkbare manieren blokkeren. Een belangrijke reden is de koppeling: die moet het geneesmiddel stevig vasthouden terwijl het ADC in de bloedbaan circuleert, en het vervolgens schoon loslaten zodra het in de tumorcel is. Bestaande koppelingen werken goed alleen met bepaalde chemische groepen op geneesmiddelen, vooral amines, en hebben vaak moeite met de vele middelen die alcoholgroepen (–OH) bevatten. Daardoor blijft een groot aantal veelbelovende kankermiddelen onaangeroerd omdat ze niet veilig of efficiënt door huidige ADC-ontwerpen kunnen worden afgeleverd.
Een truc lenen van antivirale pillen
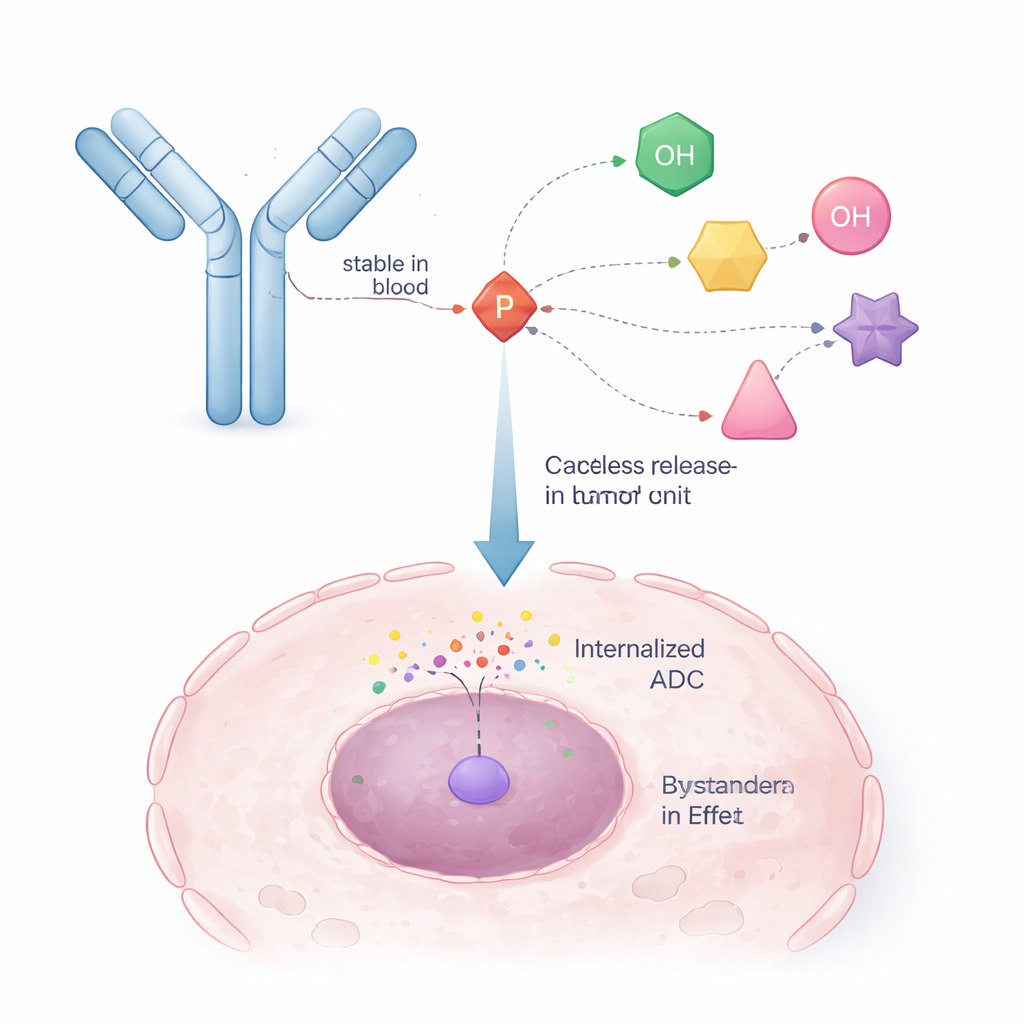
De onderzoekers grepen naar een strategie die al is bewezen bij antivirale middelen, de zogeheten ProTides. In die geneesmiddelen maskeert een fosforhoudende eenheid tijdelijk een geladen fosfaatgroep zodat het middel cellen kan binnendringen, en valt die eenheid binnenin uit elkaar om de actieve vorm vrij te geven. De auteurs herontwierpen dit concept zodat één arm van de fosforcore wordt gebruikt om aan een antilichaam te koppelen, terwijl de andere armen het kankergeneesmiddel vasthouden. Dit creëert een “zelf-immolerende” koppeling: wanneer een interne trigger (zoals een enzym in een tumorcel) een klein deel van de structuur afknipt, stort de fosforunit gecontroleerd in en komt het oorspronkelijke geneesmiddelmolecuul vrij met zijn alcoholgroep hersteld en ongemodificeerd.
Het bouwen van een veelzijdige chemische plug
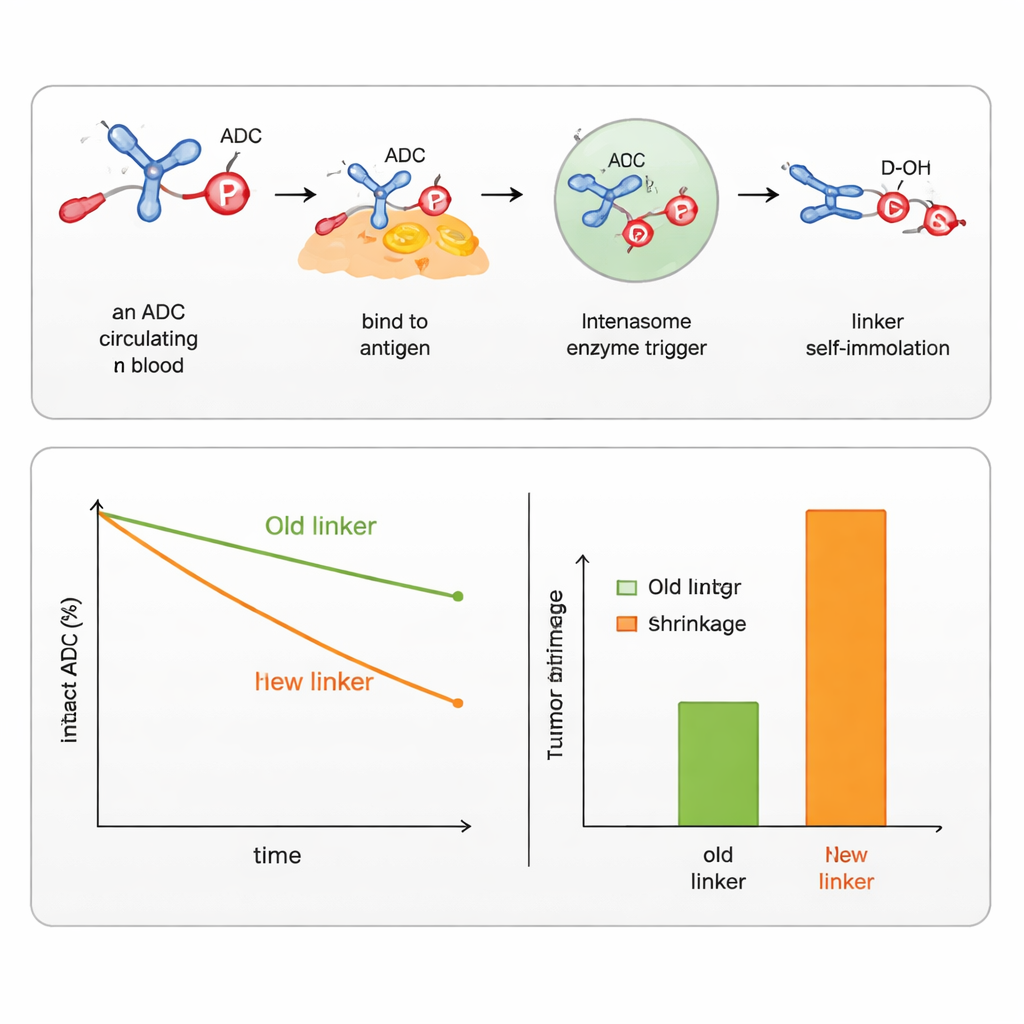
Het team liet zien dat door het aanpassen van de groepen rond het fosforatoom ze konden fijnafstemmen hoe stabiel de koppeling in bloed is en hoe snel deze binnen cellen uiteenvalt. Ze ontwierpen varianten die reageren op verschillende typen triggers die veel voorkomen in kankercellen, waaronder esterases en proteasen (enzymen die specifieke bindingen knippen), evenals enzymen die suikergroepen herkennen of reducerende omstandigheden in celcompartimenten. Met deze ontwerpen konden ze zowel aromatische alcoholen (zoals het chemotherapeuticum SN38) als alifatische alcoholen (zoals DXd, de payload in een goedgekeurd borstkanker-ADC) koppelen en vrijgeven. Vergeleken met bestaande commerciële schakelaars voor SN38 en DXd hielden de nieuwe fosforamideetkoppelingen de geneesmiddelen langer aan het ADC gebonden in serum, leverden meer medicijn aan tumoren en veroorzaakten sterkere tumorkrimping in muizen, terwijl ze minder effect op gezonde cellen lieten zien.
Het ontsluiten van veel nieuwe kanker-payloads
Om te testen hoe breed inzetbaar de koppeling was, assembleerden de onderzoekers ADCs die tien verschillende geneesmiddelen droegen die allemaal ten minste één –OH-groep bevatten maar op zeer verschillende manieren in kankercellen werken. Dit omvatte remmers van DNA-synthese, eiwitvouwing (HSP90), energie‑metabolisme (NAMPT en DHODH) en eiwitvertaling, evenals bekende middelen zoals paclitaxel en gemcitabine. Ondanks de grote verscheidenheid aan structuren konden ze uniforme ADCs maken met hoge geneesmiddellading voor al deze middelen. In celstudies over meerdere kankertypen toonden de meeste van deze ADCs nanomolaire of zelfs sub‑nanomolaire potentie en duidelijke selectiviteit voor cellen die het antilichaamdoel tot expressie brachten, wat bevestigt dat de koppeling consequent actief geneesmiddel binnen de juiste cellen kon vrijmaken.
Gemcitabine als etalagevoorbeeld
Gemcitabine is een veelgebruikte chemotherapie, maar in conventionele vorm wordt het zo snel uit het lichaam geklaard dat patiënten grote herhaalde doses moeten ontvangen, wat beperkt hoeveel veilig kan worden gegeven. Met de fosforamideetkoppeling hechtten de auteurs gemcitabine aan een HER2‑gericht antilichaam op elk van twee alcoholposities en toonden aan dat beide versies hun volledige activiteit herwonnen zodra ze in kankercellen waren. In muismodellen met HER2‑positieve tumoren produceerde een enkele dosis van het gemcitabine‑ADC — met ongeveer duizend keer minder totale gemcitabine dan typische vrije‑geneesmiddelregimes — sterke en selectieve tumorgroei‑onderdrukking. Het gedrag van het ADC in de bloedbaan kwam nauw overeen met dat van het naakte antilichaam, en hoge doses werden goed verdragen in ratten, wat op een ruime veiligheidsmarge wijst.
Wat dit betekent voor toekomstige kankerbehandeling
Voor niet‑specialisten is de kernboodschap dat dit werk een nieuwe, zeer aanpasbare chemische connector levert die antilichamen in staat stelt een veel breder scala aan kankergeneesmiddelen te dragen dan voorheen, en dat op een veiligere manier. Door ervoor te zorgen dat geneesmiddelen bevestigd blijven tijdens de circulatie en pas schoon worden vrijgegeven nadat het ADC in een kankercel is opgenomen, verbeteren fosforamideetkoppelingen hoeveel medicijn de tumor bereikt en verminderen ze nevenschade aan gezond weefsel. Even belangrijk is dat ze bestaande krachtige kleine‑molecuulgeneesmiddelen — met zeer verschillende vormen en werkingsmechanismen — kunnen herbestemmen als gerichte therapieën. Dit kan het aanbod van beschikbare ADCs voor patiënten sterk vergroten en helpen tumoren aan te pakken die resistent zijn geworden tegen de momenteel beperkte set payloads.
Bronvermelding: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Trefwoorden: antilichaam–drugconjugaten, kanker medicijnafgifte, zelf-immolerende schakelaars, fosforamideetchemie, gerichte chemotherapie