Clear Sky Science · nl
Ligand-gestuurde regiodivergente en enantioselectieve C–H-cyanatie van secundaire amines
Waarom het veranderen van kleine bindingen belangrijk is voor grote geneesmiddelen
Veel topverkopende geneesmiddelen bevatten kleine, stikstofhoudende bouwstenen die amines worden genoemd. Fijne veranderingen in hoe de atomen rond deze amines verbonden zijn, kunnen een zwak middel omzetten in een krachtig, specifiek geneesmiddel — of in iets inactiefs of zelfs schadelijks. Dit artikel beschrijft een nieuwe manier om deze aminebouwstenen naar wens te modificeren, waardoor chemici precies kunnen kiezen waar op het molecuul gereageerd wordt en welke spiegelbeeldvorm wordt gemaakt, beide cruciaal voor het ontwerpen van veiligere en effectievere medicijnen.
Een plek kiezen op een druk molecuul
Amines in geneesmiddelen hebben vaak meerdere zeer vergelijkbare koolstof–waterstof (C–H)-bindingen die zich normaal gesproken bijna hetzelfde gedragen. Chemici willen graag één van die waterstoffen vervangen door een nuttige groep, zoals een cyano‑groep (–CN), zonder de rest van het molecuul te verstoren. Dat is lastig omdat standaardreacties meestal naar de meest reactieve plaats verlopen die door de moleculaire structuur wordt bepaald, en niet door de keuze van de chemicus. Hier werken de auteurs met eenvoudige, flexibele secundaire amines die twee verschillende koolstofketens aan het stikstofatoom dragen. Ze laten zien dat ze, uitgaande van hetzelfde amine, de reactie naar een van twee naburige posities kunnen leiden — ofwel naast een kleine N‑methylgroep (de zogeheten α′‑plek) of één koolstof verderop aan de andere keten (de β‑plek) — door simpelweg de ligand rond een koperkatalysator te veranderen.
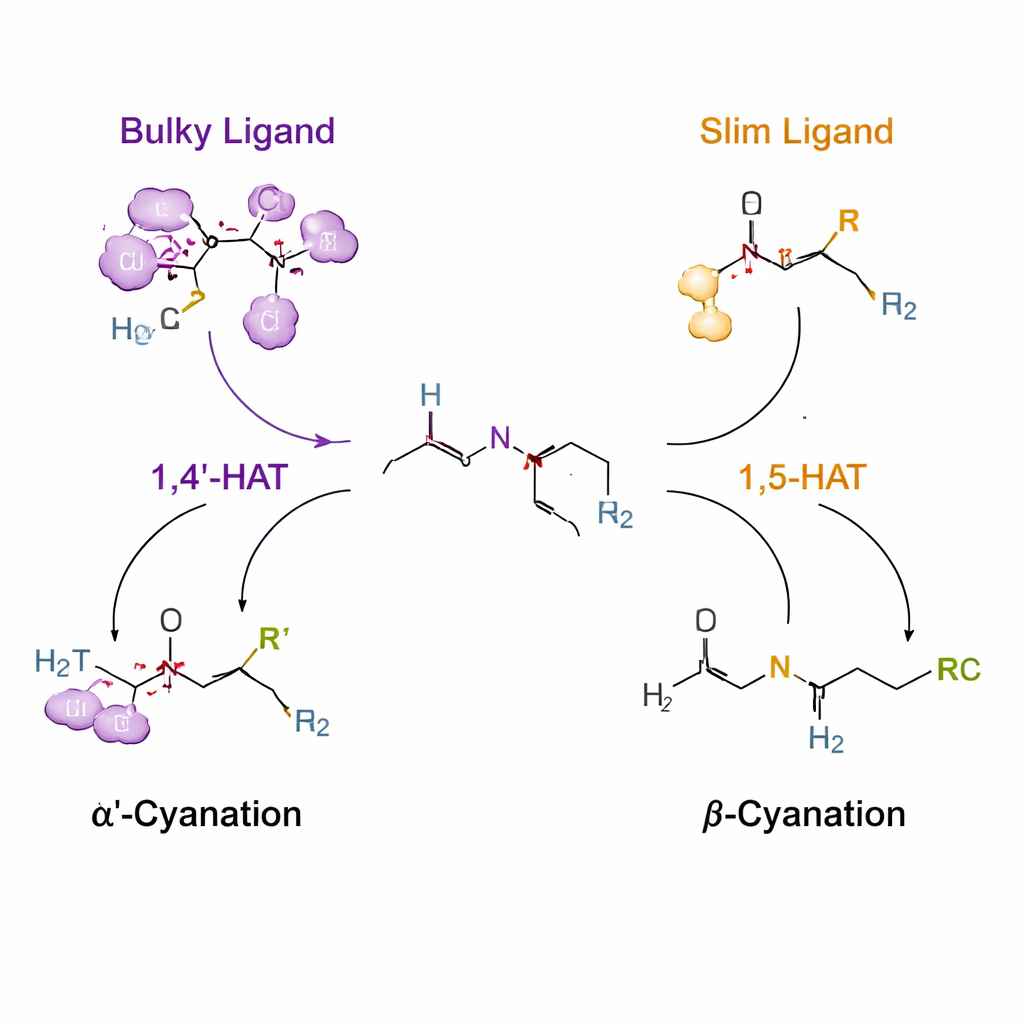
Geleide waterstof-‘sprongen’ gebruiken om reactiviteit te sturen
De sleuteltruc berust op een proces dat waterstofatoomoverdracht heet, waarbij een kortlevende, stikstofgecentreerde radicaal een waterstof van een nabijgelegen koolstof wegrukt. Dergelijke radicalen geven normaal de voorkeur aan een bepaalde afstand, waarbij een zespersoons "bereik" bekend als 1,5‑HAT vaak favoriet is. De auteurs koppelen een tijdelijke ureum- en chloorhandgreep aan het amine zodat onder koperkatalyse dit stikstofradicaal gevormd wordt en een waterstof kan grijpen van ofwel de α′‑ ofwel de β‑positie. Door liganden — organische moleculen die rond het koper wikkelen — te ontwerpen, hervormen ze de omgeving van het radicaal. Een zeer volumineuze ligand (genoemd L14) duwt het systeem richting een ongewone 1,4′‑HAT‑stap die de N‑methylgroep target en selectieve α′‑cyanatie geeft. Slankere liganden (zoals L8) laten het conventionele 1,5‑HAT‑pad toe, waardoor de reactie in plaats daarvan naar de β‑positie wordt gestuurd.
Van controle over positie naar controle over handigheid
Buiten de keuze waar gereageerd wordt, wil het team ook controle over handigheid, ofwel chiraleiteit, wat cruciaal is omdat veel geneesmiddelen bestaan als links- en rechtsdraaiende vormen die zich verschillend gedragen in het lichaam. Om dit te bereiken, introduceren ze chirale liganden — moleculen die zelf een gedraaide vorm hebben — in het kopercomplex. Twee dergelijke liganden, L24 en L41, geven een sterke voorkeur voor één spiegelbeeld wanneer de reactie een cyano‑groep installeert op β‑posities, inclusief zowel benzyliche plekken (naast aromatische ringen) als allylische plekken (naast dubbele bindingen). Over een breed scala aan amine‑startmaterialen levert de methode β‑gecyanate producten met uitstekende selectiviteit voor zowel positie als handigheid, en het werkt op gramschaal, wat aantoont dat het proces praktisch en robuust is voor synthese.
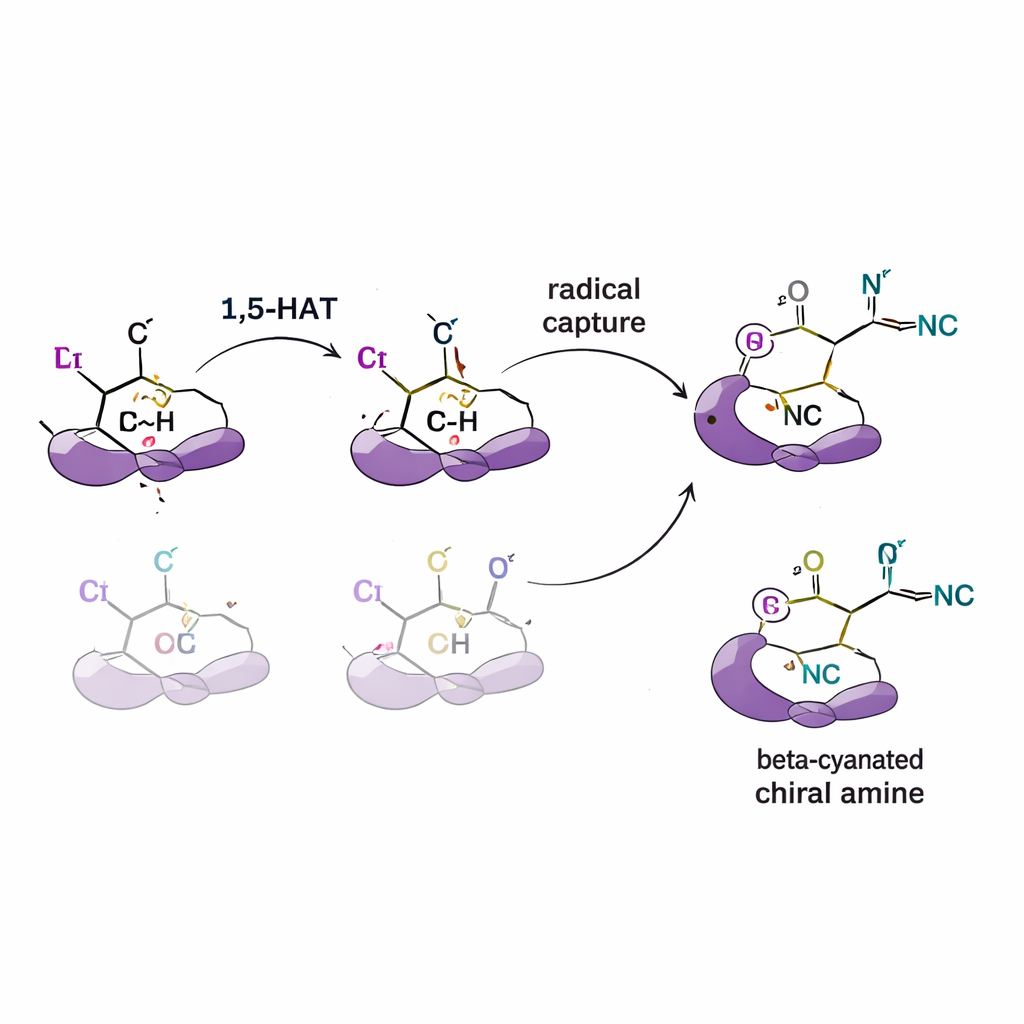
De achterliggende mechaniek testen van de selectiviteit
Om te achterhalen hoe deze controle ontstaat, voeren de auteurs een reeks mechanistische experimenten uit. Door radicale "vallen" toe te voegen, bevestigen ze dat reactieve radicaalintermediaren inderdaad betrokken zijn. Met substraten waarin bepaalde waterstoffen door deuterium (een zwaardere vorm van waterstof) zijn vervangen, detecteren ze kinetische isotoopeffecten die wijzen op de waterstofoverdrachtsstap als de trage, selectiviteitsbepalende stap van de reactie. Labelingexperimenten tonen ook dat waterstof in één enkele, eenrichtingsstap verplaatst wordt in plaats van heen en weer te pendelen tussen posities. Complementaire computersimulaties (density functional theory) ondersteunen deze bevindingen en geven aan dat de vorm en bulk van de ligand de energie van concurrerende waterstofoverdrachtsroutes en de manier waarop het radicaal vervolgens met koper en cyanide combineert om een voorkeurs‑spiegelbeeld te geven, veranderen.
Wat dit betekent voor toekomstig geneesmiddelontwerp
Al met al introduceert dit werk een flexibele strategie om veelvoorkomende aminegroepen op twee nauw verwante posities naar wens te herontwerpen, met fijne controle over moleculaire handigheid. Door alleen de ligand op een koperkatalysator te verwisselen, kunnen chemici kiezen of ze een cyano‑groep op een kleine N‑methylunit of op het aangrenzende koolstofatoom van een andere zijgroep plaatsen, en dat toepassen op vele complexe, medicijnachtige moleculen. Omdat cyano‑groepen waardevolle opstapjes zijn naar veel andere functionele groepen, zal deze "dial‑a‑site" en "dial‑a‑hand" benadering het waarschijnlijker maken om nieuwe geneesmiddelen te verkennen en te optimaliseren die gebaseerd zijn op hetzelfde basale amineskelet.
Bronvermelding: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Trefwoorden: aminetransformaat, waterstofatoomoverdracht, koperkatalyse, enantioselectieve cyanatie, medicinale chemie