Clear Sky Science · nl
Dubbele genomische lokalisaties en genregulerende functies van MBD-2 met en zonder NuRD in Caenorhabditis elegans dat DNA-methylering mist
Hoe piepkleine wormen de regels van genregulatie herschrijven
Onze cellen gebruiken chemische labels op DNA en eiwitten om te onthouden welke genen aan of uit moeten staan. Een van de meest bekende labels, DNA-methylering, ontbreekt in sommige dieren—en toch groeien en reproduceren die dieren zich normaal. Dit artikel onderzoekt hoe een kleine worm, Caenorhabditis elegans, genregulatie regelt zonder DNA-methylering en onthult een onverwacht flexibel back-upsysteem dat onze kijk op epigenetica kan veranderen.
Een ontbrekend DNA-merkje roept een grote vraag op
Bij zoogdieren helpt een chemisch merkje, 5‑methylcytosine (5mC), bij het stilleggen van genen tijdens ontwikkeling, X-chromosoominactivatie en de verdediging tegen springende genen. Eiwitten genaamd MBD2 en MBD3 lezen deze merktekens en rekruteren een groot eiwitcomplex, het NuRD-complex, dat chromatine kan herschikken en deactiveren. Vreemd genoeg zijn veel ongewervelden, waaronder C. elegans en fruitvliegen, 5mC en de enzymen die het aanbrengen kwijtgeraakt—maar ze behielden wel een MBD2/3-achtig eiwit. Dat roept een puzzel op: waarom zou een “DNA-methyleringslezer” bewaard blijven in een genoom dat DNA-methylering niet meer gebruikt, en wat doet het in plaats daarvan?
Een scaffold-eiwit waar wormen niet zonder kunnen
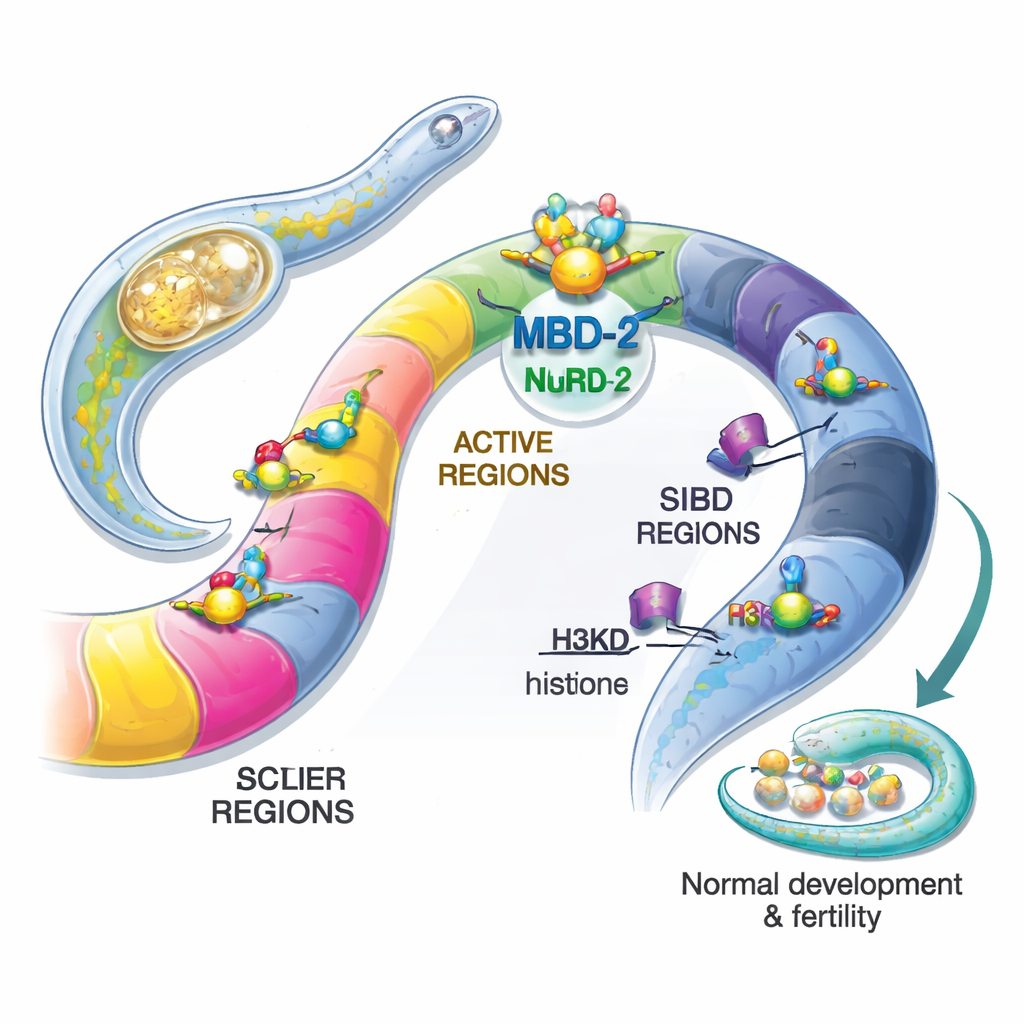
De auteurs concentreerden zich op de wormversie van dit eiwit, MBD‑2 genoemd. In tegenstelling tot zijn zoogdierverwanten heeft worm-MBD‑2 het klassieke methyl-bindende domein dat 5mC herkent verloren, maar het behoudt flexibele en coiled-coil segmenten die aan andere eiwitten kunnen hechten. Door MBD‑2 met fluorescente merkers te labelen, toonde het team aan dat het in de kernen van bijna alle cellen aanwezig is gedurende het hele leven van de worm, wat consistent is met een brede rol in genregulatie. Met genetische manipulatie maakten ze vervolgens wormen die helemaal geen MBD‑2 misten, of alleen het coiled-coilgebied misten dat het contact met NuRD medieert. Beide mutaties leidden tot ernstige problemen: dieren waren klein, bewogen slecht, ontwikkelden misvormde voortplantingsstructuren en waren grotendeels onvruchtbaar. Dit toonde aan dat MBD‑2 essentieel is voor normale ontwikkeling en vruchtbaarheid, zelfs in afwezigheid van DNA-methylering.
Het NuRD-machine herbouwen in een methyleringsvrije wereld
Om te onderzoeken of worm-MBD‑2 nog steeds met NuRD samenwerkt, haalden de auteurs getagde MBD‑2 uit wormextracten en identificeerden ze partners door massaspectrometrie. De meeste bekende NuRD-componenten waren aanwezig, wat bevestigt dat MBD‑2 als kernscaffold in dit complex fungeert, net zoals MBD2/3 bij zoogdieren. Toen het coiled-coilgebied werd verwijderd, gingen veel van deze interacties verloren, vooral die met nucleosoom-remodellerende eiwitten. Tegelijkertijd toonde grootschalige RNA-sequencing aan dat meer dan een kwart van alle wormgenen in MBD‑2-mutanten hun activiteit veranderde, met veel meer genen die aan gingen dan uit. Dit patroon geeft aan dat MBD‑2, vaak samen met NuRD, over het algemeen als repressor fungeert om ongepaste genexpressie stil te houden, terwijl het ook helpt de juiste activiteit van een subset sterk geëxpresseerde genen te onderhouden.
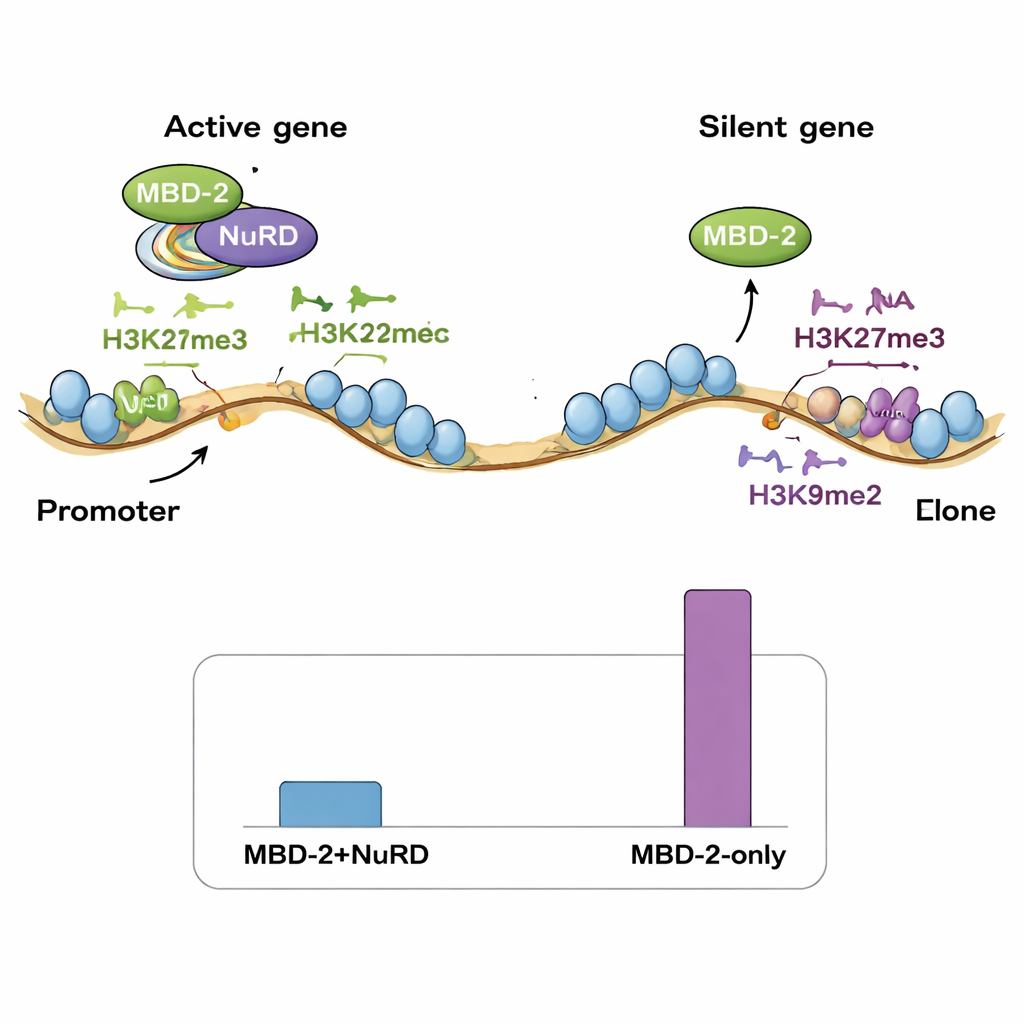
Twee bindingsmodi op het genoom
Vervolgens bracht het team in kaart waar MBD‑2 langs het genoom zit met ChIP‑seq en vergeleek deze locaties met bestaande kaarten van NuRD-componenten en verschillende histonmerken. Verrassend genoeg overlappen slechts een klein deel van de MBD‑2-locaties nauw met NuRD-eiwitten en merktekens van open, actief chromatine. De overgrote meerderheid van MBD‑2-locaties lag elders, in de chromosomale “armen” die rijk zijn aan repressieve histonmerken zoals H3K27me3 en H3K9me2/3. Met andere woorden, MBD‑2 vertoont een dubbele gedragspatroon: op een minderheid van locaties gaat het mee met NuRD om actieve genen fijn af te stemmen, maar op veel meer locaties bindt het onafhankelijk in al stilstaande regio’s. Ook het patroon van binden binnen genen blijkt van belang—wanneer MBD‑2 zich nabij genstarters opstapelt, leidt verlies van het eiwit vaak tot activatie van die genen, terwijl binding dieper in genlichamen vaak gepaard gaat met verminderde expressie bij verwijdering van MBD‑2.
Een evolutionaire back-up voor ontbrekende DNA-methylering
De auteurs stellen voor dat, in soorten die DNA-methylering hebben verloren, repressieve histonmerken—vooral H3K27me3—kunnen zijn uitgebreid om een vergelijkbare regulerende rol te vervullen. Worm-MBD‑2 lijkt te zijn herbestemd: in plaats van 5mC op DNA te lezen, associeert het nu met chromatinegebieden die door specifieke histonmodificaties zijn gemarkeerd, terwijl het nog steeds het NuRD-complex ankerde door zijn geconserveerde eiwit-interactiedomeinen. Dit werk laat zien dat een oud toolkit voor genstillegging door evolutie kan worden omgebouwd: het chemische merkje op DNA kan verdwijnen, maar de bijbehorende eiwitmachinerie overleeft door over te schakelen op alternatieve signalen. Voor niet-specialisten is de kernboodschap dat genregulatie opmerkelijk flexibel is—cellen kunnen een belangrijk epigenetisch merkje verliezen en toch complexe controle over duizenden genen behouden door meer te leunen op andere chromatinetekens en de veelzijdige scaffold-rollen van eiwitten zoals MBD‑2.
Bronvermelding: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Trefwoorden: epigenetica, chromatine, genregulatie, C. elegans, histonmodificatie