Clear Sky Science · nl
Een zeer dynamisch mononucleair non‑heme ijzenezym voor de tweestaps biosynthese van isonitrilen
Hoe bacteriën exotische chemische gereedschappen maken
Isonitrilen zijn kleine maar krachtige chemische groepen die functioneren als Zwitserse zakmessen: ze kunnen metalen binden, op veel verschillende manieren reageren en dienen vaak als het “aanvalsdeel” van sterke natuurlijke antibiotica en toxines. Sommige ziekteverwekkende bacteriën, waaronder de tuberculoseverwekker Mycobacterium tuberculosis, zetten isonitrilen op vetmoleculen om daarmee metalen van hun gastheer te ontfutselen. Dit artikel onderzoekt hoe een van hun enzymen, Rv0097 genoemd, dit buitengewoon veeleisende stukje chemie in twee nauwkeurig gechoreografeerde stappen tot stand brengt.
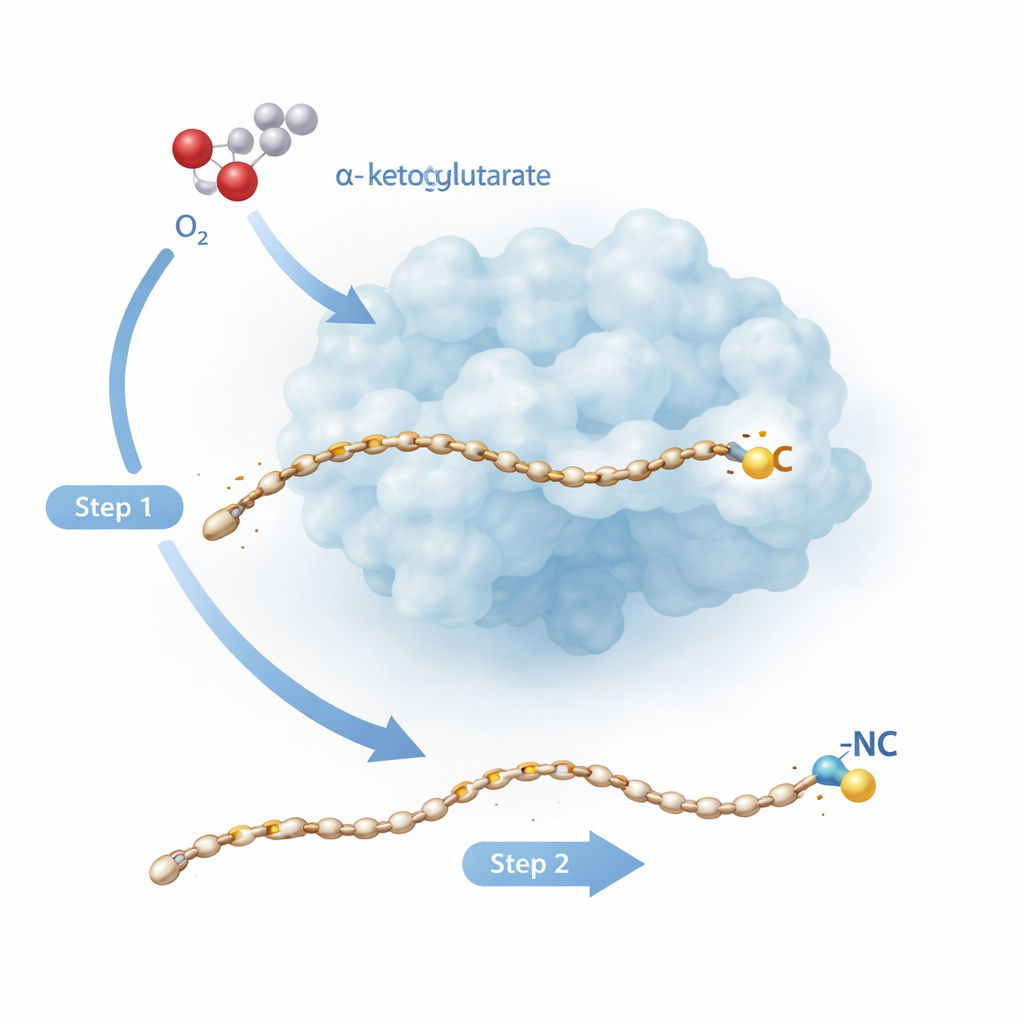
Een moleculaire metamorfose in twee stappen
Rv0097 behoort tot een grote familie van ijzafhankelijke enzymen die normaal gesproken eenvoudigere taken vervullen, zoals het toevoegen van zuurstof op één plek van een molecuul. Hier is de klus zwaarder: beginnend met een “glycyl–vetzuur” bouwsteen moet het enzym een gloednieuwe isonitrilegroep vormen, waarbij beide sleutelatomen — het koolstof‑ en het stikstofatoom — afkomstig zijn uit hetzelfde kleine glycinefragment. Eerder werk aan een verwant enzym, ScoE, suggereerde dat dit niet in één keer kan gebeuren. In plaats daarvan zijn twee afzonderlijke reactieve “halfcycli” nodig, elk aangedreven door een ijzer‑zuurstof‑soort die ontstaat wanneer het enzym een hulpstof, α‑ketoglutaraat, uiteenrijt en hiervan zuurstof combineert met die uit de lucht. De nieuwe studie richt zich op het tuberculose‑enzym Rv0097 om op atomair niveau te volgen hoe een enzym deze twee radicale stappen na elkaar uitvoert op hetzelfde substraat zonder de controle te verliezen.
Het enzym bevriezen in actie
Middels röntgenkristallografie legden de onderzoekers zestien hoogresolutie‑momentopnamen van Rv0097 vast in verschillende toestanden: leeg, gebonden aan zijn vetsubstraat (een tien‑koolstofmolecuul genaamd CADA), gebonden aan de hulpstof α‑ketoglutaraat, en in combinaties die vluchtige reactietussenproducten nabootsen. Deze structuren tonen dat Rv0097 een gespleten persoonlijkheid heeft. In rust is zijn actieve centrum grotendeels afgesloten, waarbij een sleutelaminzuur (fenylalanine 102) tussen twee orientaties schakelt die het lange vetstaart‑pocket droog houden en klaar voor hydrofobe binding. Wanneer CADA bindt, klikt dit residu in een enkele orientatie en wordt de polaire “kop” van het substraat verankerd door geladen zijketens terwijl de olieachtige staart in een nauw tunnelletje nestelt. Mutaties in dit poortpaar van residuen (F102 en het nabijgelegen glycine G204) blokkeren of laten juist te veel water binnen, waardoor de activiteit scherp afneemt en de voorkeur voor ketenlengtes van het enzym verandert.
Bewegende deksels en dynamische lussen
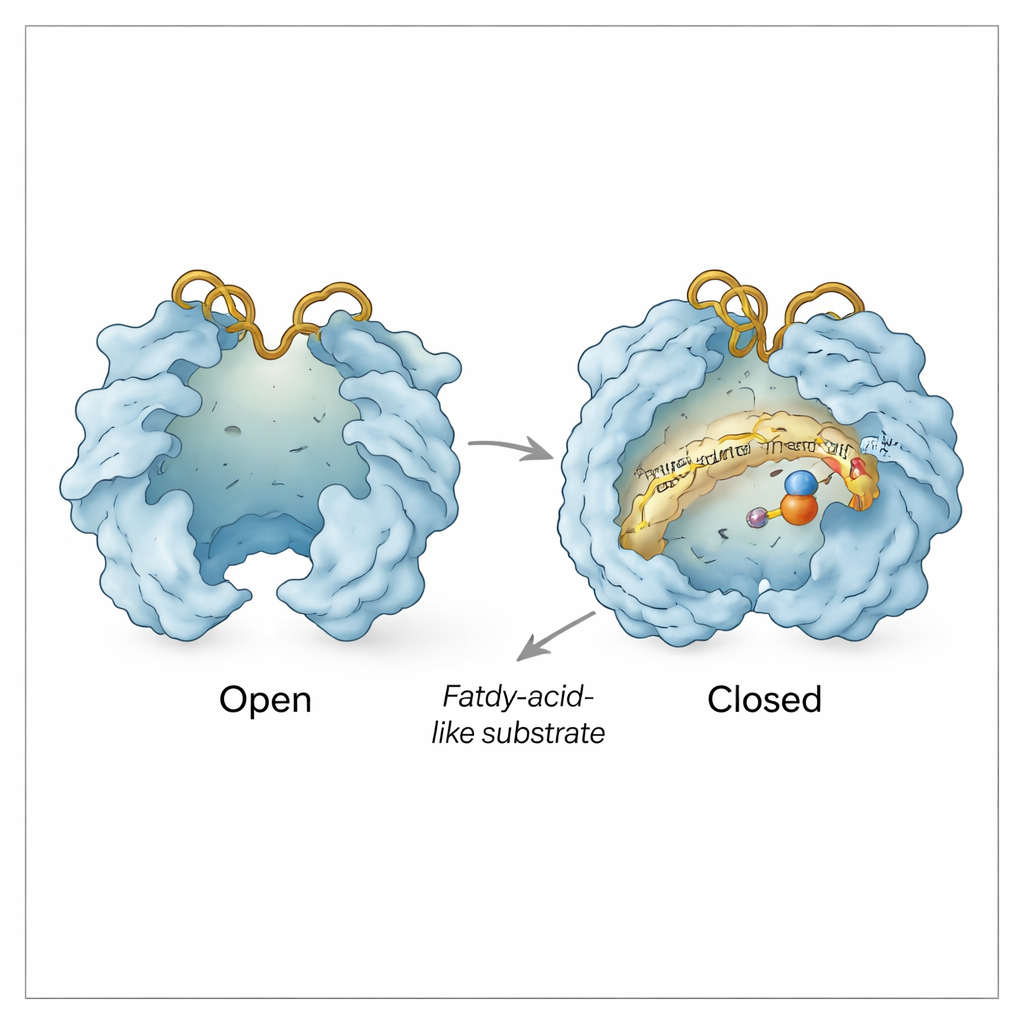
Buiten het substraatholte gedraagt Rv0097 zich als een klein machientje met bewegende deuren. Het team observeerde “open” en “gesloten” conformaties waarin twee dekselachtige regio’s uit elkaar zwaaien of samenkomen boven het actieve centrum. Openen maakt het ijzercentrum zichtbaar en creëert een pad voor α‑ketoglutaraat en het substraat om binnen te komen; sluiten schermt de chemie af van het omringende water zodra de reactie aan de gang is. Twee flexibele oppervlakte‑lussen, de His‑lus en de Arg‑lus naar de histidine en arginine daarin genoemd, fungeren als een extra poort. In sommige structuren zwaaien deze lussen naar binnen zodat het arginine‑residu α‑ketoglutaraat kan grijpen; in andere zwaaien ze naar buiten en lijken een zijkanaal te creëren waarlangs afgewerkte hulpfragmenten (succinaat en kooldioxide) kunnen vertrekken en een vers α‑ketoglutaraat kan binnenglippen voor de tweede stap—terwijl het substraatafgeleide tussenproduct op zijn plek geklemd blijft.
Een kwetsbaar tussenproduct beschermen
Biochemische assays ondersteunen dit structurele beeld. De eerste helft van de reactie zet CADA om in een hoogreactief imine‑tussenproduct dat snel uiteen zou vallen als het in oplossing terechtkwam. Door het afbraakproduct chemisch te vangen, tonen de auteurs aan dat het grootste deel van dit tussenproduct alleen wordt gedetecteerd wanneer het enzym nog aanwezig is, wat impliceert dat het gebonden en beschermd blijft binnen Rv0097 tussen de twee halfreacties. De structuren verklaren hoe: subtiele herpositioneringen van de His‑ en Arg‑lussen, samen met kleine verschuivingen van nabijgelegen residuen, lijken het tussenproduct in een beschutte holte te verzegelen terwijl kleine moleculen zoals α‑ketoglutaraat, succinaat en kooldioxide via gecontroleerde kanalen kunnen uitwisselen.
Waarom dit belangrijk is voor TB en verder
Samen onthullen deze resultaten Rv0097 als een zeer dynamische, enkel‑eiwit‑productielijn die ijzergebaseerde chemie twee keer achtereen op hetzelfde substraat toepast zonder ooit een gevaarlijk halfproduct los te laten. Voor tuberculosebacteriën vormt deze precisie de basis voor de productie van isonitrile‑gedecoreerde moleculen die hen helpen essentiële metalen in het lichaam te bemachtigen, en genetische studies wijzen uit dat de route belangrijk is voor hun overleving tijdens infectie. Voor chemici en medicijnontwerpers biedt het werk een blauwdruk om verwante enzymen te ontwerpen die nieuwe isonitrile‑houdende verbindingen maken, en het suggereert dat het verstoren van Rv0097’s bewegende deksels en poorten een manier zou kunnen zijn om nieuwe antibiotica te ontwikkelen.
Bronvermelding: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Trefwoorden: biosynthese van isonitrilen, non‑heme ijzenezym, Mycobacterium tuberculosis, enzymdynamica, metaal‑chelaterende natuurlijke producten