Clear Sky Science · nl
Ontregeling van ijzerhomeostase maakt alvleesklierkanker gevoeliger voor irreversibele elektroporatie
Elektriciteit en ijzer inzetten tegen een dodelijke kanker
Alvleesklierkanker behoort tot de moeilijkst te behandelen kankers; zelfs agressieve lokale therapieën slagen er vaak niet in te voorkomen dat de tumor terugkeert. Deze studie onderzoekt een nieuwe manier om een bestaande procedure — irreversibele elektroporatie, die tumoren doodt met korte, krachtige elektrische pulsen — effectiever en veiliger te maken. Door op slimme wijze het ijzermetabolisme van kankercellen te verstoren, tonen de onderzoekers aan dat ze overlevende cellen in een destructieve vorm van celdood kunnen duwen, wat mogelijk de kans op terugkeer van de tumor vermindert.
Waarom elektrische pulsen op zichzelf niet genoeg zijn
Irreversibele elektroporatie (IRE) behandelt tumoren door dunne elektroden in of rondom de tumor te plaatsen en snelle, hoogspanningspulsen af te vuren. Deze pulsen maken permanente gaten in celmembranen, doden veel kankercellen en wekken een immuunrespons op. Maar het elektrische veld is niet overal gelijkmatig. Gebieden die net iets zwakkere pulsen krijgen, kunnen kankercellen in leven laten, en die overlevenden kunnen een nieuwe tumor vormen. Toen het team alvleesklierkankercellen en muizentumoren die aan een subletaal elektrisch veld waren blootgesteld nader onderzocht, vonden ze dat deze cellen in plaats van te sterven door het ijzerafhankelijke proces ferroptose, een breed antioxidatief verdedigingsprogramma inschakelden. Belangrijke beschermende genen, waaronder genen die helpen bij het neutraliseren van ijzergerelateerde schade, werden omhooggeregeld, waardoor de cellen de storm konden doorstaan en herstellen.
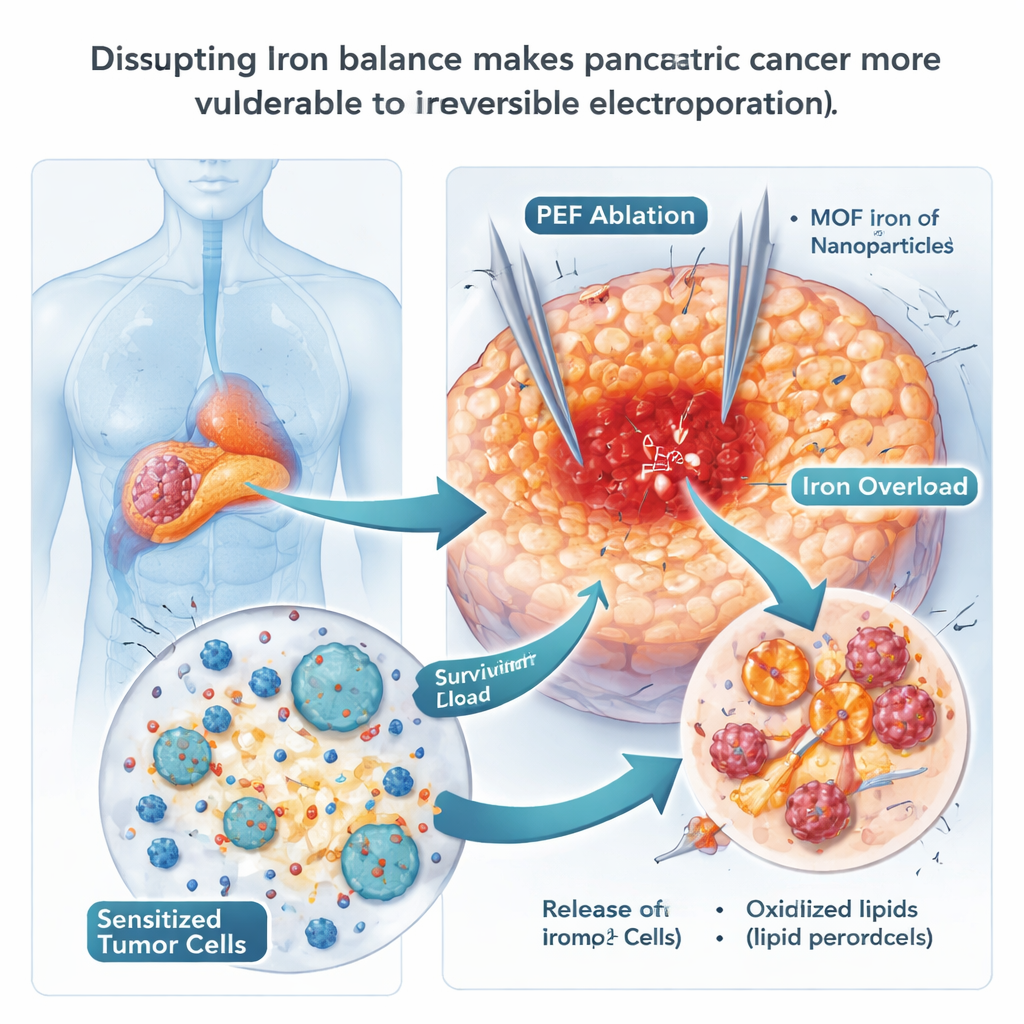
Ijzernanodeeltjes gebruiken om cellen naar vernietiging te duwen
Aangezien ferroptose afhankelijk is van ijzer, testten de wetenschappers of ijzerrijke nanodeeltjes kankercellen over de rand konden duwen. Ze gebruikten speciaal ontworpen metaal–organische raamwerkdeeltjes die ijzer bevatten (MOF-Fe), die snel ijzer vrijgeven in de zure compartimenten van cellen. In kweek schoten alvleesklierkankercellen die deze deeltjes opnamen omhoog in vrije ijzerconcentratie en geïnduceerde lipide-oxidatie in hun membranen — klassieke kenmerken van ferroptose — en vormden ze veel minder kolonies. Bij muizen vertraagde de combinatie van MOF-Fe met IRE de teruggroei van tumoren langer dan een van beide behandelingen afzonderlijk, en tumoren vertoonden meer tekenen van oxidatieve schade. Dit voordeel was echter tijdelijk: na ongeveer drie weken begonnen de tumoren weer te groeien, wat suggereert dat de kanker een manier had gevonden zich aan de ijzerbelasting aan te passen.
Richten op de ijzervoorraad van de cel
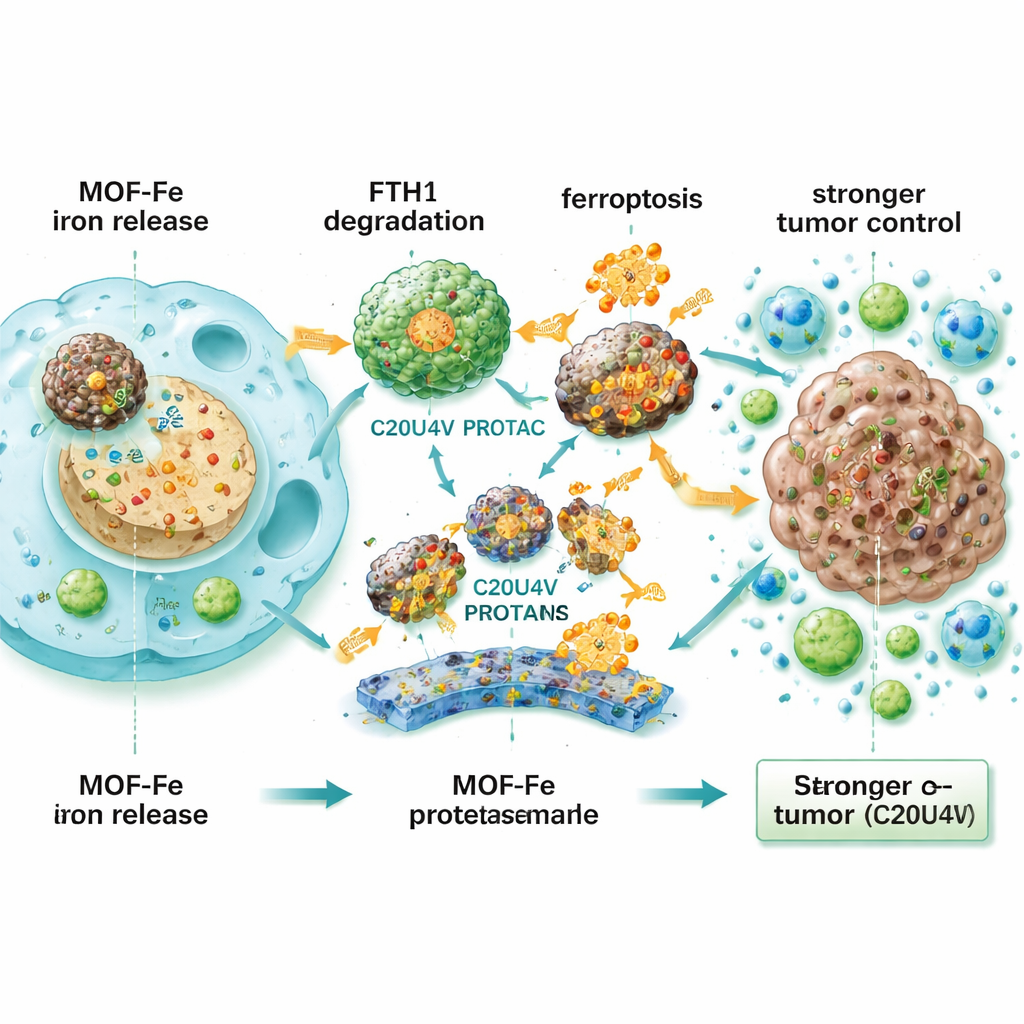
Om deze resistentie te begrijpen, analyseerde het team welke eiwitten veranderden na MOF-Fe-behandeling. Een opvallende was ferritine zwaarketen 1 (FTH1), onderdeel van het ijzeropslageiwitcomplex — het moleculaire equivalent van een vuurvaste kluis voor overtollig ijzer. Wanneer FTH1-expressie experimenteel werd verhoogd, werden kankercellen weerbaarder tegen ferroptose; wanneer FTH1 werd verlaagd, werden ze kwetsbaarder. Dit wees op FTH1 als een centraal schild tegen ijzergedreven celdood. De onderzoekers creëerden daarop een ontworpen molecuul, C20U4V, opgebouwd uit arachidonzuur (een zeer oxideerbaar vet) gekoppeld aan een PROTAC-scaffold die specifieke eiwitten naar het afbraaksysteem van de cel dirigeert. In aanwezigheid van MOF-Fe bond C20U4V zich aan ferritine en recruiteerde het voor tagging en afbraak, waardoor FTH1-niveaus scherp daalden en de cel niet langer veilig ijzer kon opsluiten.
Van kweekschalen naar mini-tumoren en muizen
Wanneer MOF-Fe en C20U4V werden gecombineerd, toonden alvleesklierkankercellen hogere oxidatieve stress, meer beschadigde membraanlipiden, zieke mitochondriën en een sterk verminderde capaciteit om opnieuw te groeien. Deze synergie was ook zichtbaar in driedimensionale, van patiënten afgeleide organoïden — kleine tumorachtige structuren gekweekt uit echte patiëntweefsels — waar het geneesmiddelenpaar zowel de omvang als het aantal organoïden deed ineenstorten. Omdat C20U4V vettig is en niet in water oplost, verpakte het team het in kleine, reactieve-zuurstof-gevoelige micellen (M-C20U4V) die in de bloedbaan circuleren en het middel kunnen vrijgeven in gestreste, beschadigde tumoren. In muismodellen met alvleeskliertumoren onder de huid en in de alvleesklier zelf, kromp een drievoudige combinatie van IRE, MOF-Fe en M-C20U4V tumoren veel effectiever en verlengde de overleving vergeleken met elke enkele of dubbele behandeling. Behandelde tumoren lieten minder delende cellen, meer markers van ferroptose en zwaardere infiltratie door T-cellen en andere immuuncellen zien, wat aangeeft dat de strategie niet alleen kankercellen direct doodt maar ook het immuunsysteem helpt de tumor te herkennen en aan te vallen.
Wat dit voor patiënten zou kunnen betekenen
Voor niet-specialisten is het kernidee eenvoudig: alvleeskliertumoren ontsnappen vaak na elektrische pulsendestruction omdat sommige kankercellen overleven en zich snel aanpassen. Dit werk laat zien dat het beladen van die cellen met ijzer en tegelijkertijd het uitschakelen van hun ijzer‑“veiligheidskluis” hen in een zelfdestructieve toestand kan dwingen waartegen ze zich niet gemakkelijk kunnen verzetten. Hoewel deze benadering nog experimenteel is en uitgebreide tests op veiligheid en toepasbaarheid bij mensen zou vereisen, suggereert het dat het fijn afstemmen van hoe tumoren met een basiselement als ijzer omgaan, een onvolmaakte lokale behandeling kan veranderen in een beslissendere klap tegen een van de dodelijkste kankers.
Bronvermelding: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Trefwoorden: alvleesklierkanker, irreversibele elektroporatie, ferroptose, ijzernanodeeltjes, PROTAC-therapie