Clear Sky Science · nl
Menselijke type‑1 innate lymfoïde cellen sturen differentiatie van leukemiestamcellen en beperken de ontwikkeling van acute myeloïde leukemie
Waarom onze eigen immuuncellen ertoe doen bij leukemie
Acute myeloïde leukemie (AML) is een agressieve bloedkanker die vaak terugkeert, zelfs na intensieve chemotherapie. Een belangrijke veroorzaker is een kleine populatie “starter”‑leukemiecellen die de ziekte opnieuw kunnen laten opvlammen. Deze studie toont aan dat een weinig bekende tak van het immuunsysteem, type‑1 innate lymfoïde cellen (ILC1s), deze startercellen kan sturen weg van gevaarlijke ontwikkelingspaden en zo helpt de leukemie in experimentele modellen te vertragen. Het werk schetst ook een mogelijke manier om hulpzame ILC1s te produceren uit donornavelstrengbloed als toekomstige behandeling.
Het probleem van hardnekkige leukemiestartercellen
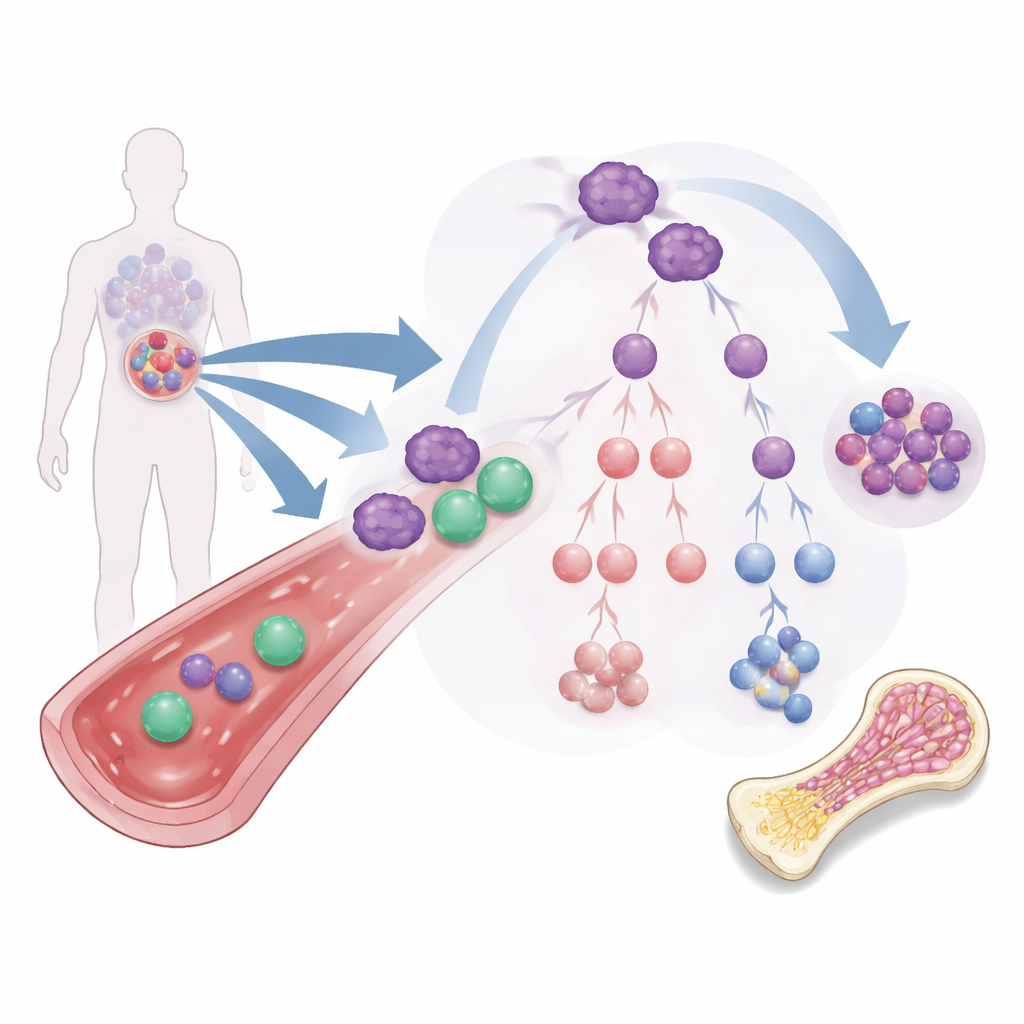
De meeste AML‑behandelingen richten zich op het merendeel van de leukemiecellen die circuleren in bloed en beenmerg. Maar een zeldzamere subset, bekend als leukemiestamcellen, gedraagt zich meer als zaden: ze kunnen zichzelf vernieuwen, zijn bestand tegen standaardmedicatie en kunnen de kanker opnieuw opbouwen. Deze cellen kunnen langs meerdere takken uitrijpen tot verschillende leukemische celtypes, waarvan sommige nog steeds het vermogen tot zelfvernieuwing behouden of de kanker afschermen voor het immuunsysteem. Vanwege deze vertakkende “stamboom” is het simpelweg verkleinen van de zichtbare leukemie niet voldoende; therapieën moeten het lot van deze startercellen veranderen of ze geheel verwijderen.
Een ontbrekende verdedigingslinie bij patiënten
ILC1s zijn snel reagerende immuuncellen die geen eerdere blootstelling nodig hebben om bedreigingen te herkennen. De onderzoekers vergeleken ILC1s in het bloed van gezonde vrijwilligers met die van AML‑patiënten. Ze ontdekten dat patiënten in het algemeen minder ILC1s hadden en dat de aanwezige cellen minder actief waren. Met single‑cell RNA‑sequencing en flowcytometrie liet het team zien dat patiënt‑ILC1s lagere niveaus van sleutel‑doodmaakmoleculen en belangrijke immuunsignalen produceerden en minder activeringsreceptoren op hun oppervlak vertoonden. Opmerkelijk was dat patiënten met hogere verhoudingen ILC1s de neiging hadden minder leukemieblaasjes te hebben, wat suggereert dat wanneer deze cellen aanwezig en functioneel zijn, ze helpen de ziekte onder controle te houden.
Hoe gezonde ILC1s leukemiecellen van schadelijke paden afleiden
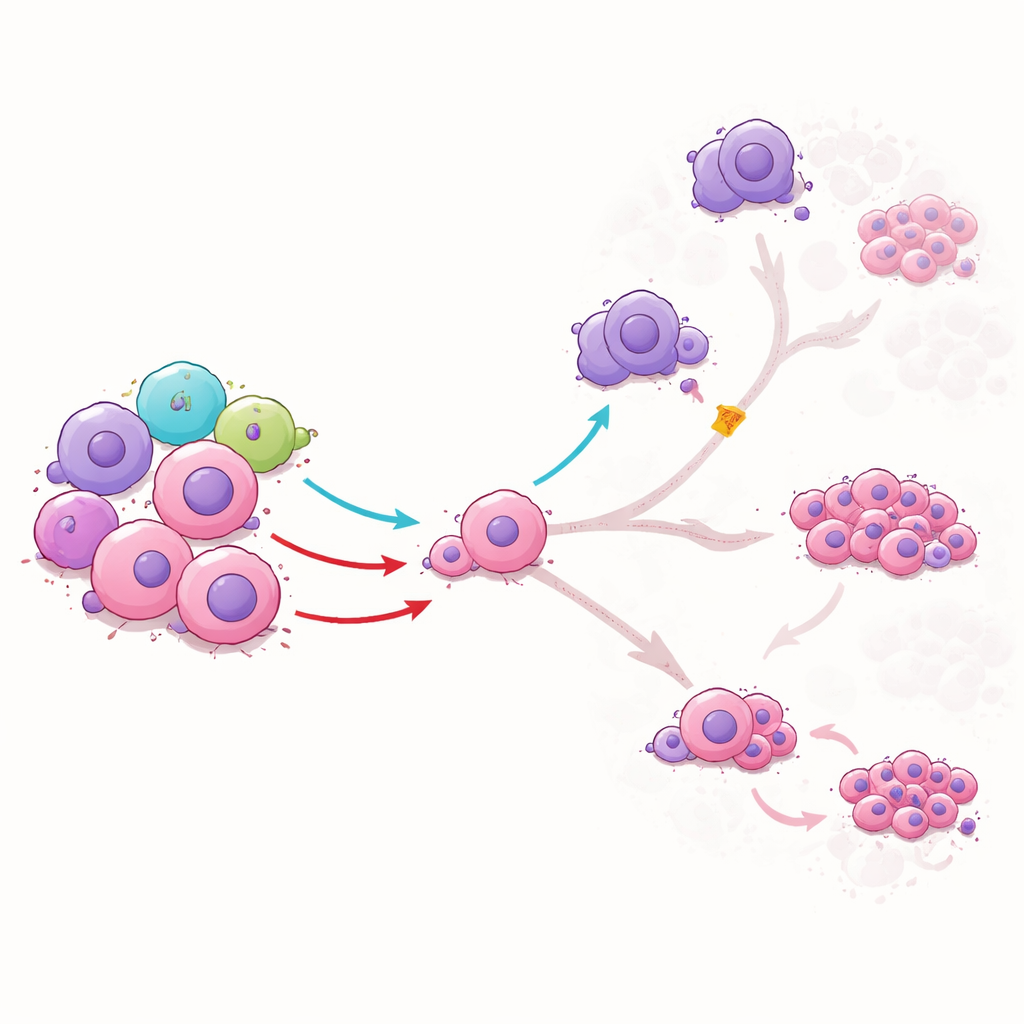
Om te begrijpen wat ILC1s daadwerkelijk met leukemiestamcellen doen, kweekte het team ze samen in het laboratorium. ILC1s van gezonde donoren vernietigden de stamcellen niet simpelweg; in plaats daarvan veranderden ze hoe deze cellen maturationeerden. Eén ILC1‑signaal, TNFα genoemd, duwde stamcellen in een tussenstaat en verminderde hun overgang naar meer gevaarlijke, snel delende leukemiecellen. Het beperkt ook het vermogen van stamcellen om macrofaag‑achtige cellen te worden die normaal immuunreacties onderdrukken en leukemie voeden. Een ander signaal, IFNγ, beperkte de voortgang van stamcellen naar bepaalde vormen die erg resistent tegen behandeling zijn. Wanneer de onderzoekers deze signalen met antilichamen blokkeerden, verdwenen de beschermende effecten, wat aantoont dat ILC1s de leukemieontwikkeling sturen via specifieke chemische boodschappen.
Navelstrengbloed omzetten in een immuuntherapie
Aangezien natuurlijke ILC1s zeldzaam zijn in volwassen bloed, zocht het team naar een hernieuwbare bron. Ze toonden aan dat stamcellen uit gedoneerd navelstrengbloed in kweek kunnen worden gestuurd om een bepaalde subset van ILC1s te worden die een oppervlakte‑marker genaamd CD161 mist maar toch de juiste transcriptiefactoren en dodelijke middelen draagt. Deze in het laboratorium gegroeide ILC1s vermeerderden zich ongeveer 700‑voudig, vielen leukemiestamcellen aan terwijl ze normale bloedvormende stamcellen spaarden, en droegen sterke cytotoxische moleculen. Toen ze werden overgebracht in gespecialiseerde muizen met menselijke leukemiestamcellen, verminderden deze ILC1s de leukemiegroei en verlengden ze de overleving — een effect dat afhankelijk was van IFNγ. In directe vergelijkingen presteerden ze ten minste even goed als op vergelijkbare wijze gegenereerde natural killer‑cellen.
Wat dit kan betekenen voor toekomstige behandeling
Samengevat onthult de studie dat bij AML een natuurlijke immuunrem — de ILC1‑populatie — zowel gekrompen als verzwakt is. Wanneer ze afkomstig zijn van gezonde donoren of gegenereerd uit navelstrengbloed, kunnen ILC1s leukemiestamcellen wegsturen van de meest schadelijke en therapieresistente loten, het aantal leukemie‑ondersteunende macrofaag‑achtige cellen verminderen en de ziekte in muismodellen vertragen. Voor een niet‑specialist is de kernboodschap dat wetenschappers niet alleen leren kankercellen te doden, maar ook de vroegste leukemiezaden te “coachen” in minder gevaarlijke richtingen met behulp van het eigen snelle‑reactie immuunsysteem. Met verdere ontwikkeling en veiliger, opschaalbare productie zouden op ILC1‑ gebaseerde celtherapieën op een dag bestaande behandelingen kunnen aanvullen om te voorkomen dat AML terugkeert.
Bronvermelding: Li, Z., Ma, R., Tang, H. et al. Human type-1 innate lymphoid cells control leukemia stem cell differentiation and limit acute myeloid leukemia development. Nat Commun 17, 2377 (2026). https://doi.org/10.1038/s41467-026-68582-2
Trefwoorden: acute myeloïde leukemie, leukemiestamcellen, innate lymfoïde cellen, kankerimmunotherapie, navelstrengbloed