Clear Sky Science · nl
Identificatie van Chlamydia pneumoniae en activatie van het NLRP3‑inflammasoom in het netvlies bij de ziekte van Alzheimer
Waarom microben in het oog van belang zijn voor geheugen
De ziekte van Alzheimer wordt meestal gezien als een probleem van plaques en kluwen in de hersenen. Deze studie suggereert dat een veelvoorkomende longontsteking‑veroorzakende bacterie, Chlamydia pneumoniae, zich stilletjes kan nestelen in het licht‑gevoelige weefsel achter in het oog — het netvlies — en zo kan bijdragen aan de ontsteking en zenuwbeschadiging die bij Alzheimer gezien worden. Omdat het netvlies niet‑invasief kan worden afgebeeld, wijst dit werk erop dat oogonderzoeken mogelijk ooit kunnen helpen bij het opsporen van infectie‑gerelateerde hersenziekten en het sturen van vroegtijdige behandeling.
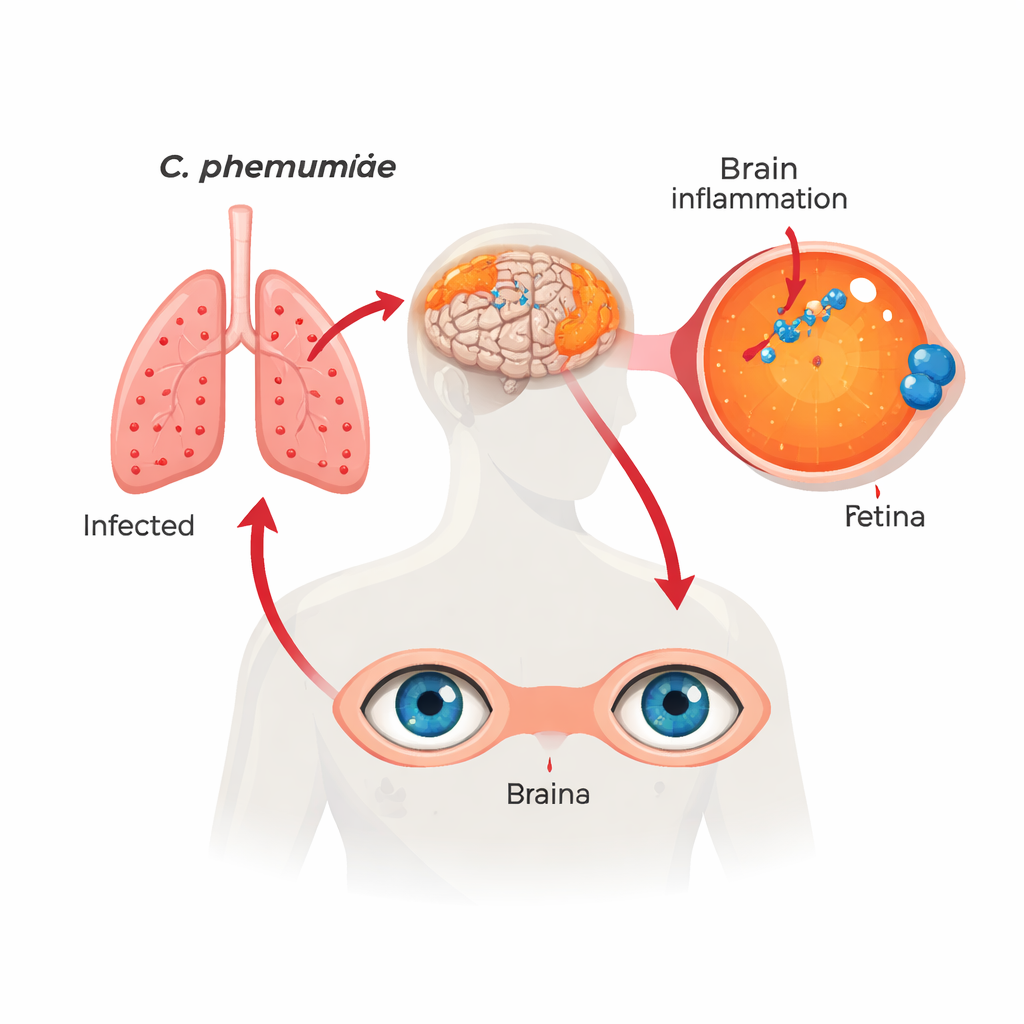
Een bekende infectie op een onverwachte plek
De onderzoekers bestudeerden netvliezen en corresponderende hersenmonsters van meer dan 100 overledenen die normale cognitie, milde cognitieve stoornis of Alzheimer‑dementie hadden gehad. Met verschillende onafhankelijke technieken — waaronder specifieke antilichamen, genetische probes, kleuringstechnieken en DNA‑tests — vonden ze duidelijke aanwijzingen voor Chlamydia pneumoniae binnen netvliescellen. Deze bacteriële “inclusies” kwamen het meest voor en waren het talrijkst bij mensen met Alzheimer, minder bij mensen met milde stoornis en het minst bij wie cognitief normaal waren gebleven. De hoeveelheid bacteriën in het netvlies weerspiegelde sterk de hoeveelheid in de hersenen, wat suggereert dat zowel oog als hersenen betrokken zijn bij dezelfde langdurige infectie.
Verbanden tussen bacteriën, plaques en denkvermogen
De vondst van de kiem was slechts de eerste stap; de kernvraag was of dat van betekenis was voor de ziekte. Het team mat klassieke Alzheimer‑markers in dezelfde weefsels. Ze zagen dat een hogere bacteriële belasting in het netvlies samenhing met meer amyloïde‑beta‑afzettingen — het kleverige eiwit dat plaques vormt — evenals bepaalde afwijkende vormen van tau‑eiwit. Mensen wiens hersenen meer bacterieel signaal droegen, hadden ook meer vezelkluwens, ernstiger algemene Alzheimer‑pathologie en meer hersenatrofie. Klinisch scoorden degenen met een hogere bacteriële belasting in het netvlies doorgaans lager op geheugen‑ en denkvaardigheidstests en hadden zij verder gevorderde dementie. Dragers van het APOE ε4‑genvariant, een sterke erfelijke risicofactor voor Alzheimer, droegen meer van de bacterie in zowel netvlies als hersenen, wat wijst op een mogelijke gen‑infectie‑interactie.
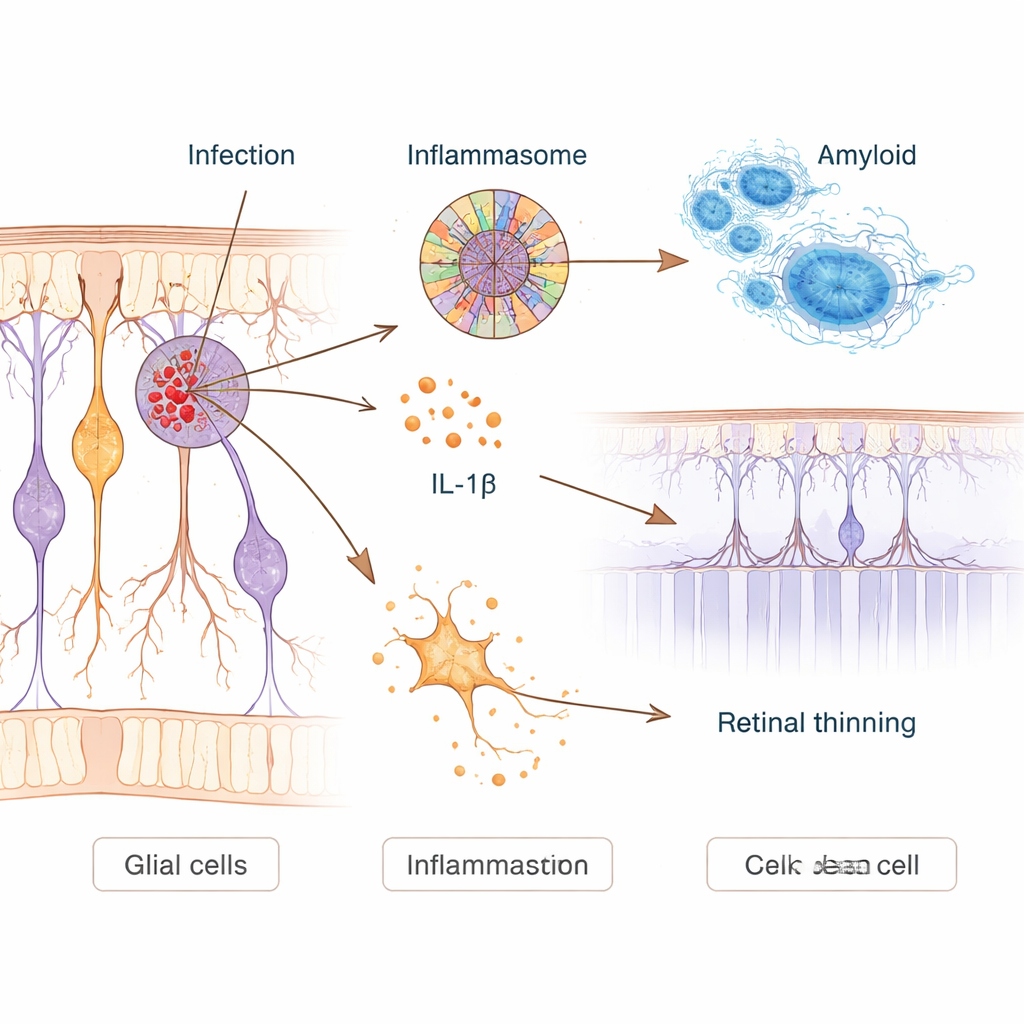
Hoe infectie toxische ontsteking kan opwekken
Om oorzaak en gevolg te onderzoeken, infecteerden de wetenschappers in het laboratorium menselijke zenuwachtige cellen en Alzheimer‑modelmuizen met Chlamydia pneumoniae. In gekweekte neuronen verhoogde de infectie de productie van amyloïde‑beta en schakelde ze een moleculair alarmsysteem in dat het NLRP3‑inflammasoom wordt genoemd. Dit systeem werkt als een cellulaire val: eenmaal geactiveerd, geeft het ontstekingsboodschappers vrij zoals interleukine‑1β en kan het gaten in celmembranen slaan, wat leidt tot een explosieve vorm van celdood. Geïnfecteerde neuronen toonden duidelijke tekenen van membraanschade en activatie van deze paden. Bij muizen was een enkele neusdosis van de bacterie voldoende om de hersenen te bereiken, waar het aantal amyloïde‑plaques toenam, immuuncellen werden geactiveerd en het optreden op geheugen‑ en visueel gebaseerde doolopertaken na enkele maanden verslechterde.
Retinale immuuncellen onder druk
In menselijke ogen brachten de onderzoekers in kaart hoe infectie samenwerkte met lokale ondersteunende cellen die normaal neuronen beschermen. Stervormige astrocyten en Müller‑cellen, evenals microglia — de huishoudelijke opruimers van hersenen en netvlies — stapelden zich rond geïnfecteerde locaties. Chemische handtekeningen van het NLRP3‑inflammasoom en de downstream celdoodroutes waren sterk verhoogd in netvliezen van mensen met Alzheimer, en namen al toe bij degenen met milde cognitieve stoornis. Veel geïnfecteerde cellen droegen markers van zowel vurige ‘pyroptotische’ dood als meer bekende apoptose. Hoewel meer microglia werden aangetrokken in Alzheimer‑netvliezen, leek elke bacterie door minder microglia te worden aangeraakt of opgenomen dan in gezonde ogen, wat suggereert dat het opruimsysteem overbelast of aangetast raakt naarmate de ziekte vordert.
Het oog gebruiken om hersengezondheid af te lezen
Aangezien het netvlies toegankelijk is voor hoogwaardige beeldvorming bij levende mensen, vroegen de onderzoekers of retinale metingen gerelateerd aan Chlamydia pneumoniae konden helpen bij het voorspellen van de Alzheimer‑status. Ze gebruikten machine‑learningmodellen om retinale infectieniveaus te combineren met markers zoals amyloïde‑beta‑afzettingen, ontsteking en plaatselijke weefselverdunning. Bepaalde combinaties — vooral retinale bacteriën samen met amyloïde — onderscheidden Alzheimerpatiënten van controles met hoge nauwkeurigheid en correleerden met ziektestadium en cognitieve testscores. Hoewel meer werk en grotere studies nodig zijn, suggereren de resultaten dat een eenvoudige oogtest op termijn niet alleen klassieke Alzheimerveranderingen, maar ook een verborgen infectiecomponent kan onthullen, wat de deur opent voor vroegtijdig gebruik van antibiotica of middelen die het inflammasoom dempen bij mensen met risico.
Wat dit voor patiënten kan betekenen
Voor niet‑specialisten is de kernboodschap dat Alzheimer mogelijk niet uitsluitend wordt aangedreven door ontspoord eiwitgedrag; langdurige infecties kunnen als brandstof zijn die een langzaam smeulend vuur aanwakkert. Deze studie levert sterke aanwijzingen dat een veelvoorkomende luchtwegbacterie zich in netvlies en hersenen kan vestigen, schadelijke ontsteking kan veroorzaken en geheugenverlies kan verergeren bij kwetsbare personen. Als toekomstige klinische studies bevestigen dat het behandelen van zulke infecties of het blokkeren van het inflammasoompad het verval vertraagt, zouden routinematige netvliesafbeelding en gerichte therapieën kunnen uitgroeien tot een meer proactieve, gepersonaliseerde benadering om dementie te voorkomen of uit te stellen.
Bronvermelding: Gaire, B.P., Koronyo, Y., Vit, JP. et al. Identification of Chlamydia pneumoniae and NLRP3 inflammasome activation in Alzheimer’s disease retina. Nat Commun 17, 771 (2026). https://doi.org/10.1038/s41467-026-68580-4
Trefwoorden: Ziekte van Alzheimer, netvlies, Chlamydia pneumoniae, neuro‑inflammatie, amyloïde‑beta