Clear Sky Science · nl
HIF onderhoudt een transcriptionele regelkring van EPAS1-expressie bij heldercelniercelcarcinoom
Waarom nierkanker extra aandacht verdient
Heldercelniercelcarcinoom is de meest voorkomende vorm van nierkanker, en veel patiënten krijgen tegenwoordig middelen die een eiwit genaamd HIF‑2α blokkeren. Deze medicijnen kunnen tumoren doen krimpen, maar ze werken niet bij iedereen even goed. Deze studie stelt een eenvoudige maar belangrijke vraag: wat zorgt ervoor dat sommige niertumoren zoveel HIF‑2α produceren, en kan begrip van deze "aan-schakelaar" ons helpen voorspellen wie het meest baat heeft bij behandeling en hoe we nieuwe therapieën kunnen ontwerpen?
De zuurstofsensor die ontspoort
Gezonde niercellen gebruiken een bewakingsprotein genaamd VHL om zuurstof-sensoren, bekend als HIFs, strak onder controle te houden. Als er genoeg zuurstof is, markeert VHL HIF-eiwitten voor afbraak, waardoor ze geen genen kunnen inschakelen die bloedvatgroei en celdeling bevorderen. Bij heldercelnierkanker gaat VHL meestal verloren of raakt beschadigd. Daardoor ontsnapt één lid van de HIF-familie, HIF‑2α (gecodeerd door het EPAS1-gen), aan afbraak en hoopt zich op. Eerder werk toonde aan dat hoge HIF‑2α-activiteit samenhangt met snellere tumorgroei en slechtere uitkomsten, en dat blokkade van HIF‑2α tumoren bij sommige patiënten kan vertragen of stoppen. De moleculaire stappen die de EPAS1-genactiviteit in niertumoren verhogen, waren echter onvoldoende begrepen.
Een verborgen DNA-schakelaar voor een kankergen
Met tumormonsters van patiënten, enkelcelligedata en kankercelmodellen laten de auteurs zien dat het boodschapper-RNA van HIF‑2α duidelijk hoger is in heldercelniertumoren dan in normaal nierweefsel of andere niertumortypen. Vervolgens scannen ze het EPAS1-gebied van het genoom op chemische en structurele tekenen van actieve regulerende DNA. Dit onthult een krachtige enhancer—een soort verafgelegen genschakelaar—ongeveer 70.000 DNA-letters stroomopwaarts van EPAS1 die specifiek actief is in helderceltumoren. In tumorcellen is het chromatine bij deze enhancer open, versierd met activatiemerkjes, en vormt het fysieke lussen naar de EPAS1-promoter, terwijl dit gebied in normale nierbuiscellen grotendeels stil is. Activiteit van deze enhancer correleert met hogere EPAS1-niveaus in grote kankerdatasets. 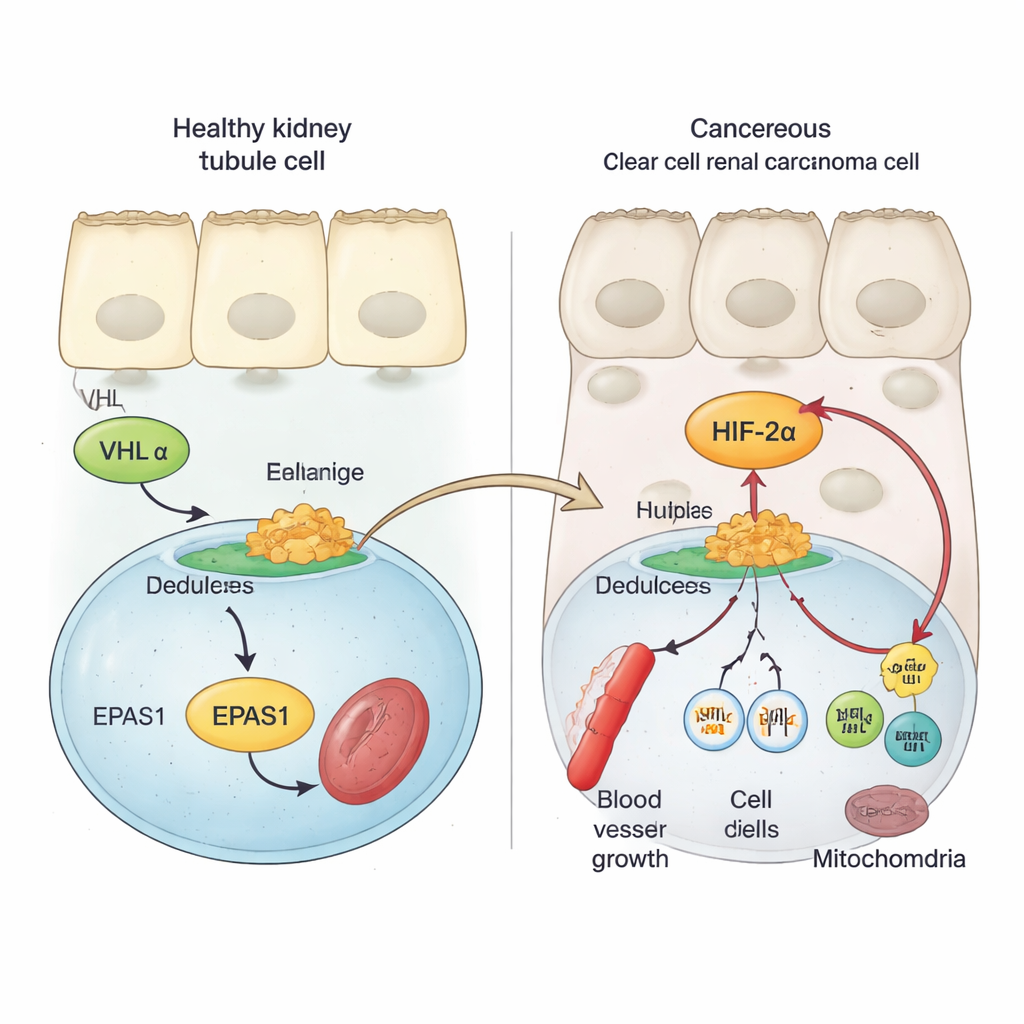
Een zichzelf versterkende lus aangedreven door nier-identiteitsfactoren
De studie vindt dat HIF-eiwitten meer doen dan reageren op lage zuurstof—ze stimuleren eigenlijk hun eigen productie. Wanneer de onderzoekers VHL herstellen of een belangrijke HIF-partner (HIF‑1β) verwijderen, dalen EPAS1-niveaus en wordt de enhancer minder toegankelijk. Directe in kaart gebrachte eiwit–DNA-contacten tonen dat HIF bindt aan twee enhancerregio's stroomopwaarts van EPAS1, inclusief de heldercel-specifieke enhancer. In nierkankercellen is deze enhancer ook bezet door PAX8 en HNF‑1β, transcriptiefactoren die bijdragen aan niercelidentiteit en waarvan bekend is dat ze tumorgroei ondersteunen. Het verstoren van PAX8 of HNF‑1β, of het muteren van hun bindingssites binnen de enhancer, vermindert HIF‑2α-RNA en -eiwit en verzwakt de enhanceractiviteit. Gezamenlijk onthullen deze bevindingen een autoregulerende kring: HIF‑2α, samenwerkend met nier-lijnagefactoren, verhoogt de activiteit van een EPAS1-enhancer, wat op zijn beurt leidt tot meer productie van HIF‑2α.
Genetisch risico en tumorgedrag komen samen op hetzelfde circuit
Het EPAS1-gebied is al lange tijd aangemerkt in genoomwijde studies als een hotspot voor nierkankerrisico, waarbij bepaalde geërfde varianten samenhangen met hogere kankerkansen en met VHL-mutaties in tumoren. Door genetische data te combineren met genexpressiemetingen tonen de auteurs aan dat personen die de hoog-risico versie van een sleutelvariant in EPAS1 dragen, de neiging hebben hogere HIF‑2α-niveaus in hun tumoren te hebben—en zelfs in normale nierbuiscellen wanneer HIF experimenteel gestabiliseerd wordt. Dit suggereert dat geërfde DNA-verschillen kunnen afstemmen hoe sterk de enhancer reageert, waardoor sommige nieren gevoeliger zijn om HIF‑2α hoger op te voeren zodra VHL verloren gaat. Experimenten in glioblastoomcellen tonen dat dezelfde enhancer ook in bepaalde hersentumoren kan worden ingeschakeld, wat erop wijst dat dit regelmodule mogelijk in andere kankers wordt hergebruikt waar HIF‑2α belangrijk is. 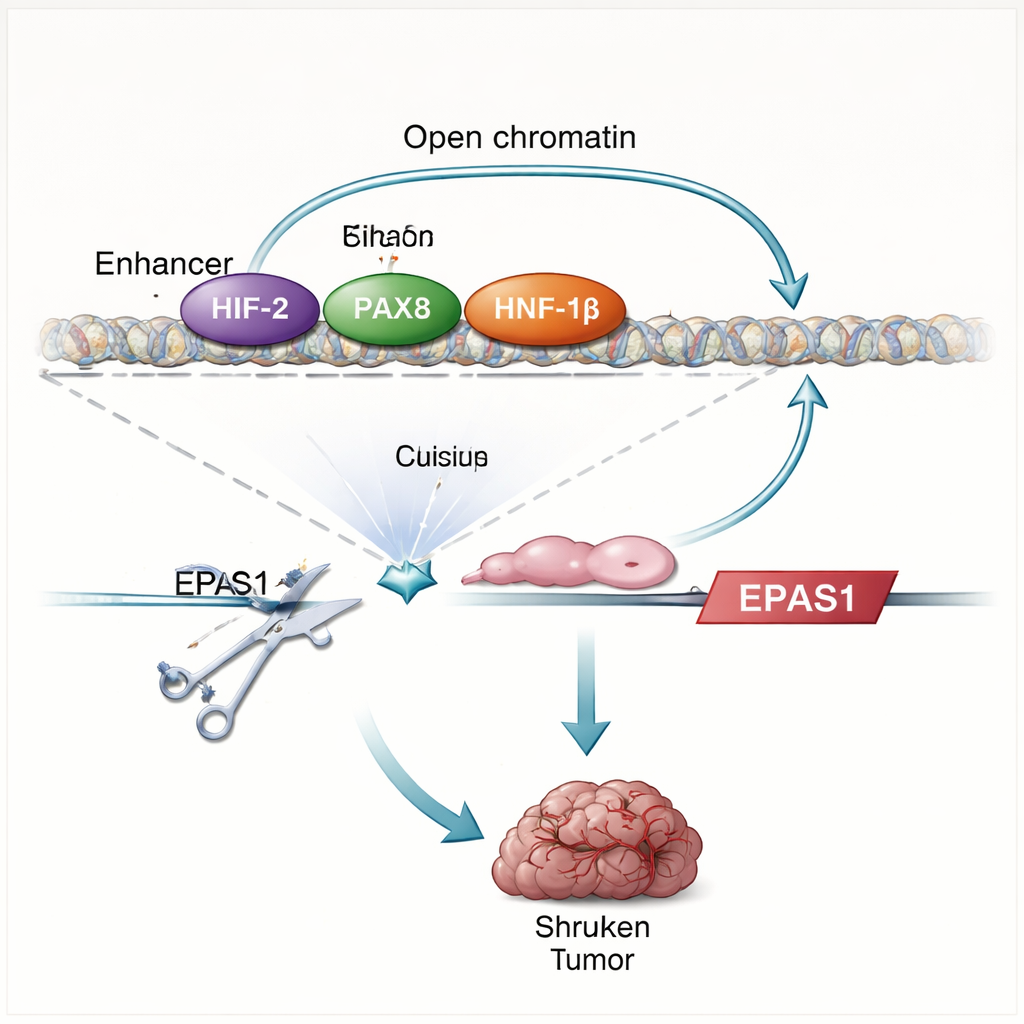
De lus doorbreken om tumorgroei te stoppen
Om te testen hoe essentieel deze enhancer is, gebruiken de onderzoekers CRISPR-genoomediting om de HIF-bindmotieven daarin te beschadigen in nierkankercellijnen en verse patiënttumorcellen. Deze ingreep verlaagt HIF‑2α-RNA met ongeveer een derde tot de helft, verlaagt de niveaus van bekende HIF‑2α-doelgenen zoals CCND1 en VEGFA, en verzwakt het bredere hypoxie-genprogramma. Wanneer de bewerkte cellen in muizen worden geïmplanteerd, vormen ze grotendeels geen tumoren, in schril contrast met controlearcellen. Het patroon van genveranderingen na enhancerdisruptie weerspiegelt nauwkeurig de effecten van directe blokkade van HIF‑2α met een klinisch middel, wat benadrukt dat dit enkele DNA-element een belangrijke motor is van het HIF‑2α-pad in deze kankers.
Wat dit betekent voor patiënten en therapieën
Voor niet-specialisten is de kernboodschap dat de auteurs een zelfversterkende DNA-schakelaar hebben ontdekt die een belangrijk kankerverhogend eiwit, HIF‑2α, aanhoudend ingeschakeld houdt in heldercelniertumoren. Deze schakelaar is afhankelijk van zowel het verlies van de VHL-rem als van nier-specifieke helper-eiwitten, en wordt beïnvloed door geërfde genetische varianten. Omdat de enhancer zeer actief is in veel helderceltumoren en sterk gekoppeld is aan de mate van activiteit van het HIF‑2α-pad, kan het meten van de activiteit ervan—of het rechtstreeks doelwitten van de enhancer—helpen patiënten te identificeren die het meeste voordeel hebben van huidige HIF‑2α-remmers en kan het nieuwe manieren bieden om dit pad af te sluiten wanneer tumoren resistent worden tegen medicijnen.
Bronvermelding: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Trefwoorden: heldercel niercelcarcinoom, HIF-2α, EPAS1-enhancer, VHL-mutatie, genetica van nierkanker