Clear Sky Science · nl
Atroposelectieve onderbroken CuAAC-reactie met cyclische diarylijodoniumnsen
Waarom deze nieuwe chemie ertoe doet
Chemici hebben al lange tijd vertrouwd op een eenvoudige "click"-reactie om moleculaire bouwstenen snel en schoon aan elkaar te klikken, een truc die alles ondersteunt van geneesmiddelenonderzoek tot zelfherstellende materialen. Dit artikel beschrijft een slimme variatie op die klassieke click-reactie waarmee wetenschappers complexere, driedimensionale moleculen met precieze handigheid kunnen bouwen — structuren die zeer gewild zijn in moderne geneesmiddelen en geavanceerde materialen.
Een klassieke click-reactie een nieuwe taak geven
Het uitgangspunt is de kopergekatalyseerde azide–alkyn cycloadditie, vaak kortweg CuAAC genoemd. Die verbindt twee kleine componenten — een azide en een alkyn — tot een vijfring genaamd een triazool onder milde omstandigheden en met opmerkelijke betrouwbaarheid. Traditioneel eindigt de reactie zodra koper de triazoolring heeft gevormd. In recente jaren hebben chemici echter geleerd dit proces te "onderbreken", door een vluchtig koper–triazoolintermediair met een derde partner te vangen om complexere producten te bouwen. Tot nu toe konden die onderbrekingen de moleculaire handigheid (chiraleiteit) niet op algemene wijze beheersen, wat hun bruikbaarheid voor het maken van verfijnde, chirale moleculen beperkte.
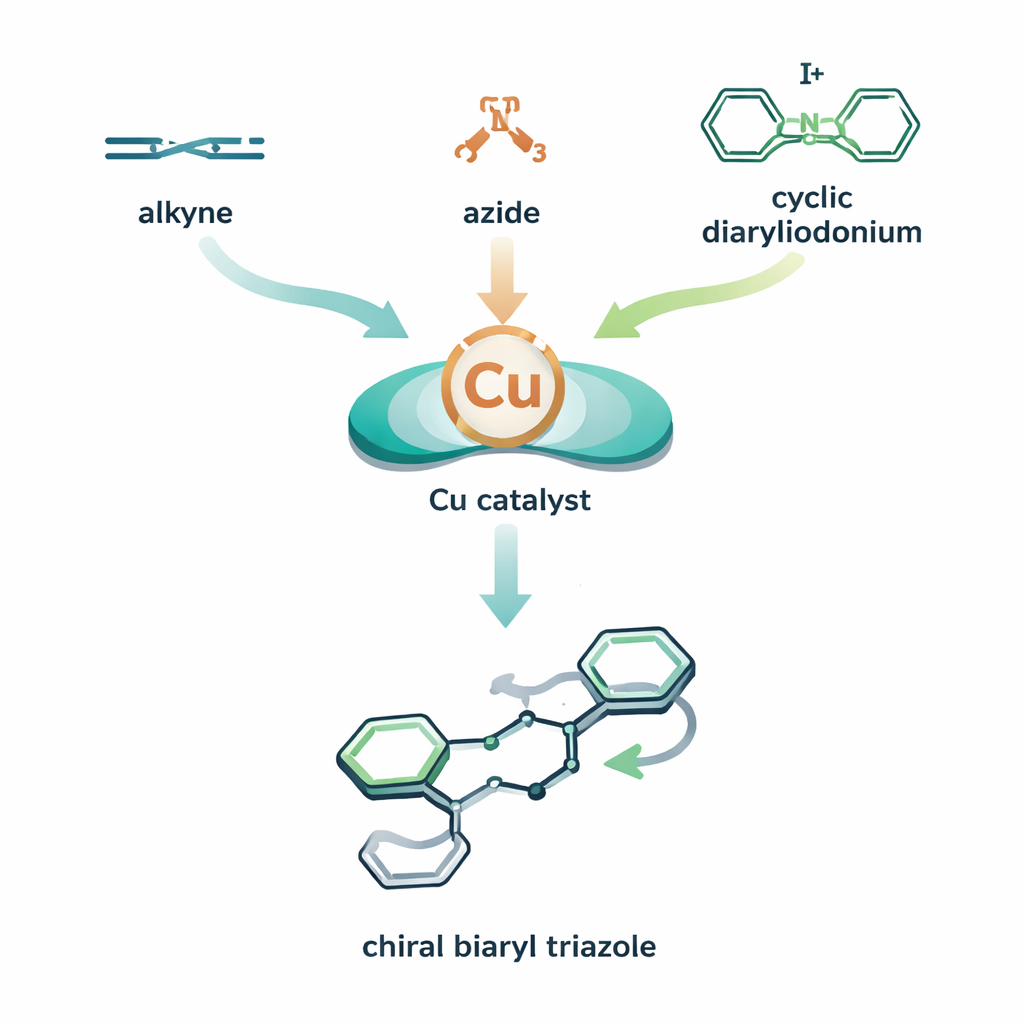
Een moleculaire puzzel van drie onderdelen met een twist
De auteurs combineren twee kopergebaseerde reactiecycli tot één georkestreerd proces. In hun ontwerp helpt een kopercatalysator eerst het alkyn en de azide een koper–triazoolintermediair te vormen. Voordat dit intermediair geneutraliseerd wordt, wordt een derde component — een ringvormig, zeer reactief jodiumhoudend molecuul dat een cyclisch diarylijodonium wordt genoemd — ingebracht. Koper infiltreert in deze ring en opent die vervolgens, waarbij één van de aromatische ringen aan de triazool wordt vastgehecht. Het resultaat is een biaryle triazool: twee ringsystemen verbonden rond een binding die als een chiraal as kan fungeren, vergelijkbaar met een propeller die links- of rechtsom kan draaien. Door koper te combineren met een zorgvuldig gekozen chiraal ligand, stuurt het team het proces zo dat de ene draai veel vaker wordt gevormd dan de andere, en bereiken zij hoge atroposelectiviteit (controle over welke axiale "hand" wordt gemaakt).
Testen hoe flexibel en betrouwbaar de methode is
Om te begrijpen hoe algemeen deze reactie kan zijn, varieerden de onderzoekers systematisch elk van de drie bouwstenen. Ze toonden aan dat veel verschillende alkynen, waaronder die met elektronrijke, elektronenarme en heteroaromatische ringen, kunnen deelnemen terwijl ze nog steeds goede opbrengsten en een sterke voorkeur voor één chirale vorm geven. Bepaalde volumineuze substituties verbeterden de selectiviteit maar konden de opbrengst verminderen, wat een afweging tussen sterische belemmering en efficiëntie blootlegde. De azidepartners werkten het beste wanneer ze afgeleid waren van eenvoudige ester- of amidegroepen of van benzyliche posities, en een reeks van dergelijke aziden leverde sterk verrijkte chirale producten. Het cyclische diarylijodoniumcomponent kon ook worden afgestemd: sommige substituties behielden zowel opbrengst als selectiviteit, terwijl andere, vooral nabij het reactieve jodiumcentrum, de reactie vertraagden of de prestaties verlaagden. Over het geheel genomen leverde de studie een brede verzameling nieuwe atropisomere biaryle triazolen die in één stap toegankelijk zijn.
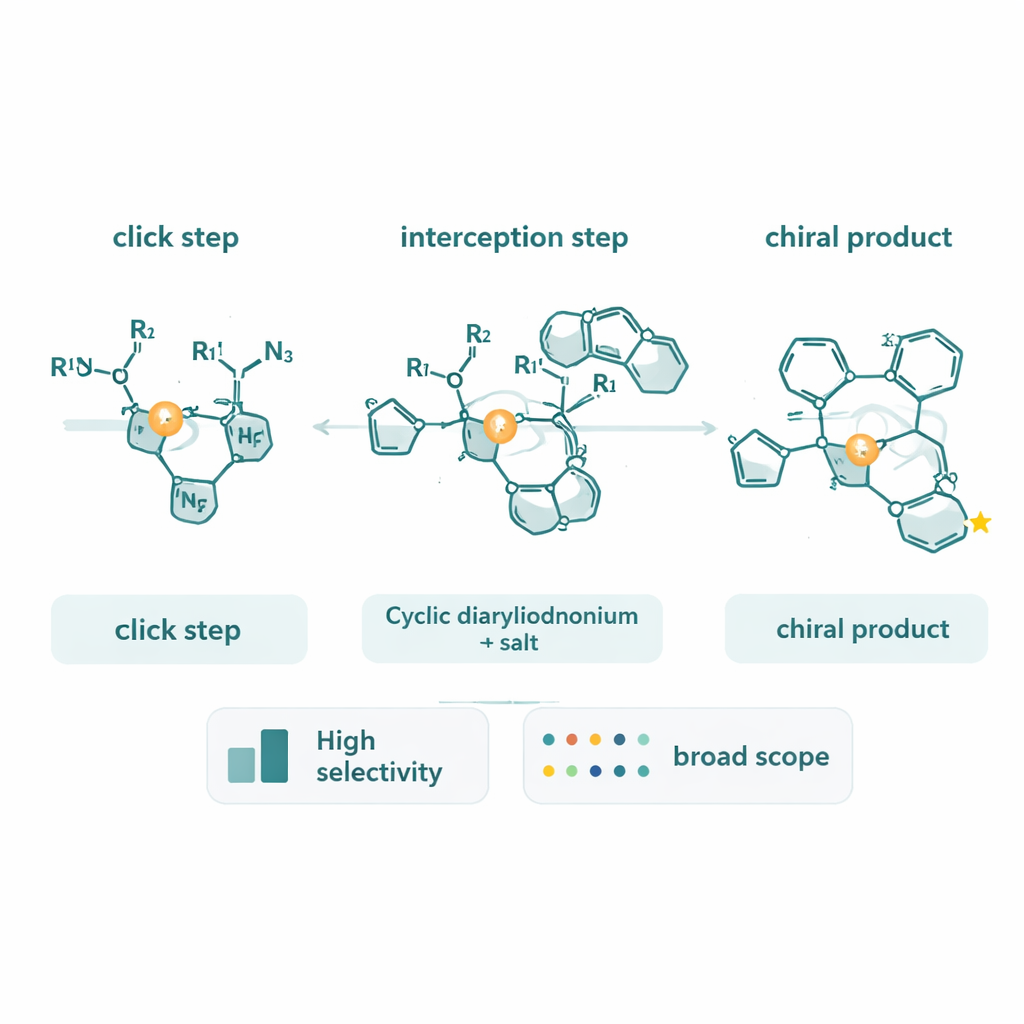
Onder de motorkap van de reactie kijken
Naast het maken van nieuwe moleculen wijdde het team aanzienlijke inspanning aan het achterhalen hoe de reactie daadwerkelijk verloopt. Met deuteriumgelabelde alkynen observeerden zij een ongebruikelijk omgekeerd kinetisch isotoopeffect, wat wijst op een snelheidsbepalende stap waarin het alkyncarbone zijn bindingskarakter verandert in plaats van simpelweg een C–H-binding te verbreken. Calorimetrische reactieverloopanalyse toonde aan dat de reactiesnelheid sterk afhankelijk is van de concentraties van het alkyn en de azide, maar slechts zwak van het cyclische diarylijodonium. Deze metingen ondersteunen een beeld waarin het vormen en transformeren van het koper–triazoolcomplex, en de oxidatieve additie daarvan in de diarylijodoniumring, samen het tempo van de reactie bepalen. Zij vonden ook dat de chirale triazoolproducten zelf aan koper kunnen kleven en de katalysator vertragen, wat aanwijzingen geeft voor manieren om het systeem verder te optimaliseren.
Wat dit vooruit betekent
In gewone bewoordingen hebben de onderzoekers een goed bekende click-reactie een nieuwe truc geleerd: in plaats van simpelweg twee stukken aan elkaar te klikken, helpt zij nu drie componenten samen te brengen tot complexe, propellerachtige moleculen en kiest ze vrijwel uitsluitend één voorkeurstwist. Dit biedt een schaalbare route naar chirale biaryle triazolen, structuren die waardevol zijn als potentiële geneesmiddelen, katalysatoren en functionele materialen. De mechanistische inzichten — vooral hoe het sleutelintermediair wordt onderschept en hoe het product de katalysator kan vergiftigen — bieden een routekaart voor het ontwerpen van nog efficiëntere en selectievere versies van deze chemie. Voor niet‑specialisten is de belangrijkste conclusie dat een al krachtig moleculair "Lego"-gereedschap net veelzijdiger is geworden, waardoor chemici fijnere controle hebben bij het bouwen van ingewikkeldere en nuttigere driedimensionale vormen.
Bronvermelding: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Trefwoorden: clickchemie, koperkatalyse, chirale biarylen, atropisomeer, triazool