Clear Sky Science · nl
Een microfysiologisch menselijk mini-blaasje onthult de wisselwerking tussen urine en urotheel in weefselweerstand en UPEC‑recidief bij urineweginfecties
Waarom de samenstelling van uw urine ertoe doet
De meesten van ons beschouwen urine louter als afval, maar de samenstelling verandert voortdurend met wat we drinken, eten en onze gezondheidstoestand. Deze studie laat zien dat die veranderingen geen onschuldige achtergrondruis zijn: ze kunnen rechtstreeks beïnvloeden hoe goed de blaas zich verdedigt tegen urineweginfecties (UWI) en hoe gemakkelijk infecties terugkeren na antibioticabehandeling. Met een klein in het lab gekweekt “mini‑blaasje” laten de onderzoekers zien hoe geconcentreerde urine het blaasklierweefsel ongemerkt kan verzwakken en ziekteverwekkende bacteriën nieuwe manieren kan bieden om zich te verbergen en behandeling te overleven.
Een mini‑blaas in het lab bouwen
Om deze verborgen dynamieken te onderzoeken, ontwikkelde het team een duimgrote menselijke “mini‑blaas” op een microfluïdisch chip. Ze zaaiden menselijke blaasoppervlaktecellen in een zacht 3D‑skelet en stimuleerden ze tot het vormen van meerdere georganiseerde lagen, vergelijkbaar met het echte blaasoppervlak. De bovenste ‘paraplu‑’cellen vormden een dichte, lekbestendige barrière, terwijl diepere lagen cellen bevatten die het weefsel in de loop der tijd kunnen vernieuwen. Het apparaat liet ook urineachtige vloeistof door een centrale kanaal stromen en stelde het weefsel in staat zacht uit te rekken en te ontspannen, waarmee de vullings‑ en ledigingscycli van een echte blaas werden nagebootst. Structurele tests en hoge resolutie‑beeldvorming bevestigden dat dit mini‑orgaan zich sterk gedraagt als zijn volle‑grote tegenhanger.
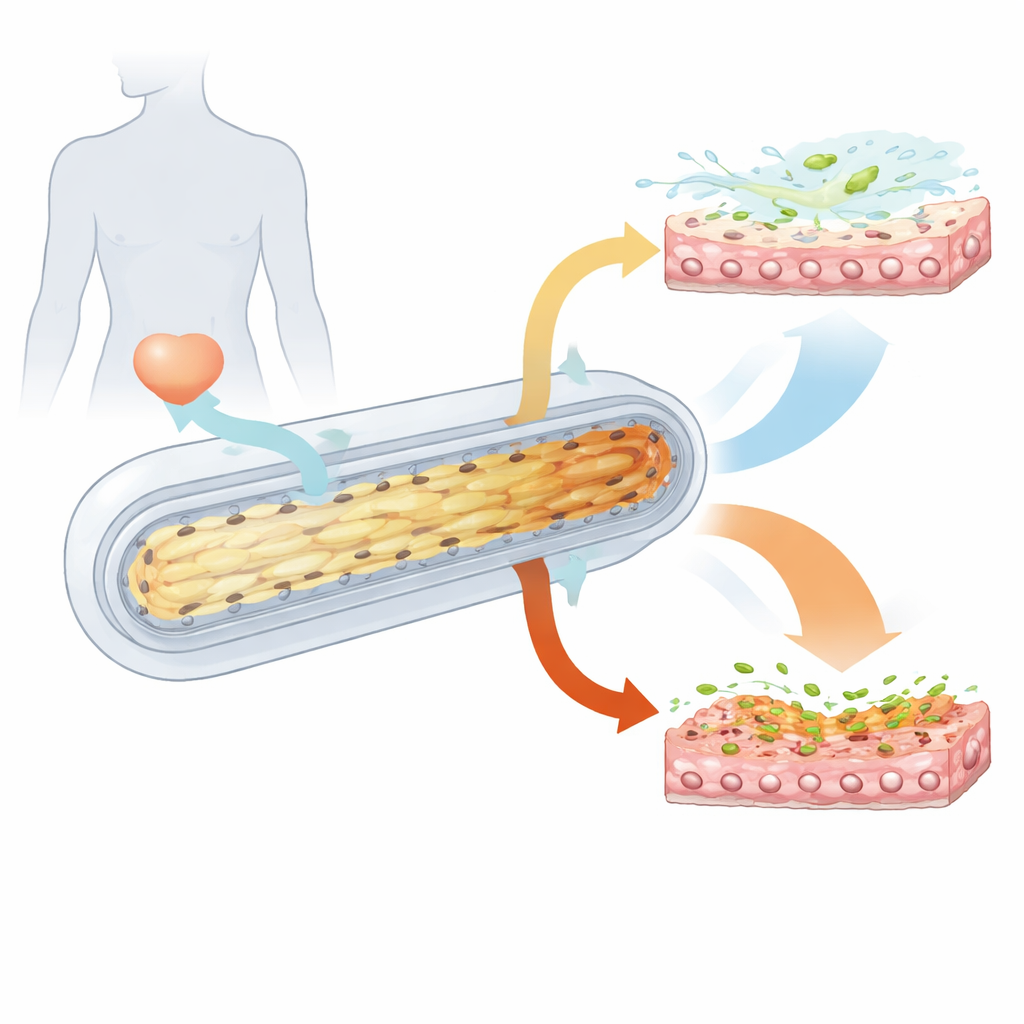
Wanneer urine ongunstig wordt
Menselijke urine kan verdund of sterk geconcentreerd zijn, afhankelijk van hydratatie en gezondheid. De onderzoekers maakten twee synthetische urinemengsels: één met “lage opgeloste stoffen” en één met “hoge opgeloste stoffen”, die de onder- en bovengrens van natuurlijke urineconcentraties benaderen. Wanneer mini‑blaasjes dagenlang werden blootgesteld aan hoge‑oplosmiddel‑urine, degradeerde het weefsel geleidelijk. Meer cellen gingen dood, het totaal aantal cellen nam af en de normaal dichte verbindingen tussen cellen werden lek. Patronen in genactiviteit wezen op verminderde cel‑cel‑hechting, zwakkere weefselvernieuwing en afgezwakte aangeboren immuun‑signalering. Daarentegen ondersteunde urine met lage concentratie oplossingsstoffen celgroei, sterkere tight junctions en een gezondere differentiatie van het blaasepitheel. Kortom: herhaalde blootstelling aan zeer geconcentreerde urine maakte het weefsel structureel zwakker en minder paraat om een vroege immuunreactie te geven.
Hoe zwak weefsel infectie in de hand werkt
Het team infecteerde de mini‑blaasjes daarna met uropathogene Escherichia coli (UPEC), de belangrijkste bacteriële oorzaak van UWI’s, en spoelde periodiek het kanaal om urineren na te bootsen. Na elke “lediging” werden veel bacteriën weggespoeld, maar sommige bleven kleven aan of drongen het blaasoppervlak binnen en bouwden geleidelijk een verborgen weefselgeassocieerde populatie op. Door het belangrijkste aanhechtingsmechanisme van de bacteriën te blokkeren met de suiker D‑mannose verminderden de onderzoekers deze ingebedde populatie en zagen ze minder weefselschade, wat aantoont dat bacteriën die op en in het weefsel leven de urine tussen ledigingen helpen herbevolken. Wanneer mini‑blaasjes vooraf werden blootgesteld aan urine met hoge opgeloste stoffen, drongen meer bacteriën het weefsel binnen en waren standaardantibiotica zoals ciprofloxacine minder in staat ze te verdrijven, zelfs als vrij zwevende bacteriën in de urine nog effectief werden verwijderd.
Verborgen overlevers na antibiotica
Het beeld werd nog opvallender met fosfomycine, een veelgebruikt antibioticum dat de bacteriële celwand raakt. In urine met hoge concentratie opgeloste stoffen deed fosfomycine slecht werk in het verminderen van de bacteriële lading, en vrije bacteriën veranderden vaak van staafvorm naar grote, fragiele, celwand‑deficiënte sferen. Vergelijkbare bolvormige vormen zijn waargenomen in urine van patiënten met terugkerende UWI’s. Met geavanceerde 3D‑elektronenmicroscopie gecombineerd met fluorescentiebeeldvorming vonden de onderzoekers dat dergelijke bolvormige bacteriën niet alleen in de urine ronddreven maar ook genesteld zaten tussen en onder blaascellen diep in de wand van het mini‑blaasje. Deze beschutte vormen overleefden de behandeling en droegen later bij aan bacteriële herschikking, wat helpt verklaren waarom infecties kunnen oplaaien nadat klachten kort zijn afgenomen.
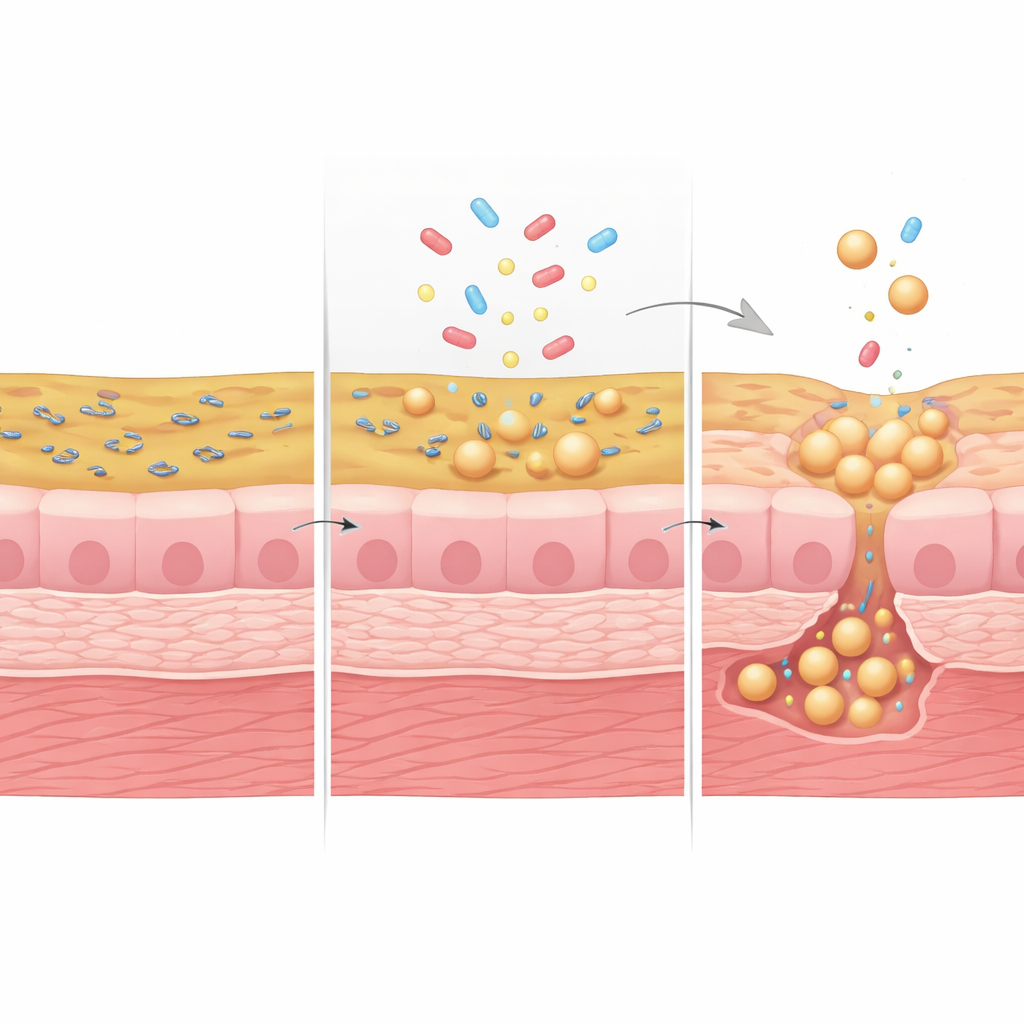
Wat dit betekent voor patiënten
Dit werk toont aan dat de omgeving van de blaas geen louter decor is, maar een actieve rol speelt in infectie‑ en behandeluitkomsten. Geconcentreerde urine verzwakt het blaasepitheel, dempt zijn immuunverdediging en maakt het mogelijk dat bacteriën dieper binnendringen en speciale celwand‑deficiënte vormen aannemen die moeilijk door zowel antibiotica als immuuncellen te elimineren zijn. Het nieuwe mini‑blaasplatform laat zien hoe urinesamenstelling, blaasweefselgezondheid en bacterieel gedrag nauw met elkaar verbonden zijn. Voor mensen die gevoelig zijn voor terugkerende UWI’s kunnen factoren die urine meer concentreren — zoals te weinig vochtinname of bepaalde medische aandoeningen — subtiel het risico vergroten door de weefselweerstand te ondermijnen en verborgen reservoirs van bacteriën te stimuleren. Het begrijpen en uiteindelijk aanpassen van dit microklimaat, naast betere antibiotica‑strategieën, kan cruciaal zijn om de vicieuze cirkel van herhaalde infecties te doorbreken.
Bronvermelding: Paduthol, G., Nikolaev, M., Sharma, K. et al. A microphysiological human mini-bladder reveals urine-urothelium interplay in tissue resilience and UPEC recurrence in urinary tract infections. Nat Commun 17, 2322 (2026). https://doi.org/10.1038/s41467-026-68573-3
Trefwoorden: urineweginfectie, blaasorganoïde, uropathogene E. coli, antibiotica‑tolerantie, urineconcentratie