Clear Sky Science · nl
De celwand openbreken voor efficiënte DNA‑levering aan diatomeeën
Algen als kleine groene fabrieken
Diatomeeën — microscopische algen die in de oceaan zweven — produceren stilletjes ongeveer een vijfde van het organische koolstof op aarde, helpen mariene voedselnetwerken te voeden en slaan kooldioxide op. Wetenschappers willen deze taaie, snelgroeiende organismen omvormen tot kleine groene fabrieken voor de productie van brandstoffen, voedingsmiddelen en gespecialiseerde chemicaliën. Maar er is een belangrijke hindernis: het is verrassend moeilijk om nieuwe DNA betrouwbaar in diatoomcellen te krijgen. Deze studie pakt dat praktische probleem frontaal aan en beschrijft nieuwe manieren om genetische instructies en genoombewerkingsgereedschappen langs de harde buitenwand van diatomeeën te sluizen.
De schaal van oceaanmicroben verzachten
Het werk concentreert zich op de modeldiatoom Phaeodactylum tricornutum, een favoriet in laboratoria omdat het genoom goed in kaart is gebracht en er al enkele basale genetische hulpmiddelen bestaan. De auteurs redeneerden dat de celwand, de eerste fysieke barrière die elk DNA moet passeren, een belangrijke knelpunten was. Door cellen te behandelen met een enzym genaamd alcalase verwijderden ze deze wand gedeeltelijk of volledig, waardoor fragiele “sferoplasten” en “protoplasten” ontstonden die veel gemakkelijker te penetreren zijn. Wanneer ze daarna electroporatie gebruikten — korte elektrische pulsen die tijdelijke poriën openen — steeg het aantal succesvolle transformanten dramatisch, ongeveer twee ordes van grootte in vergelijking met eerdere methoden. Zelfs piepkleine hoeveelheden DNA, tot één nanogram, waren voldoende om gemodificeerde cellen terug te krijgen. 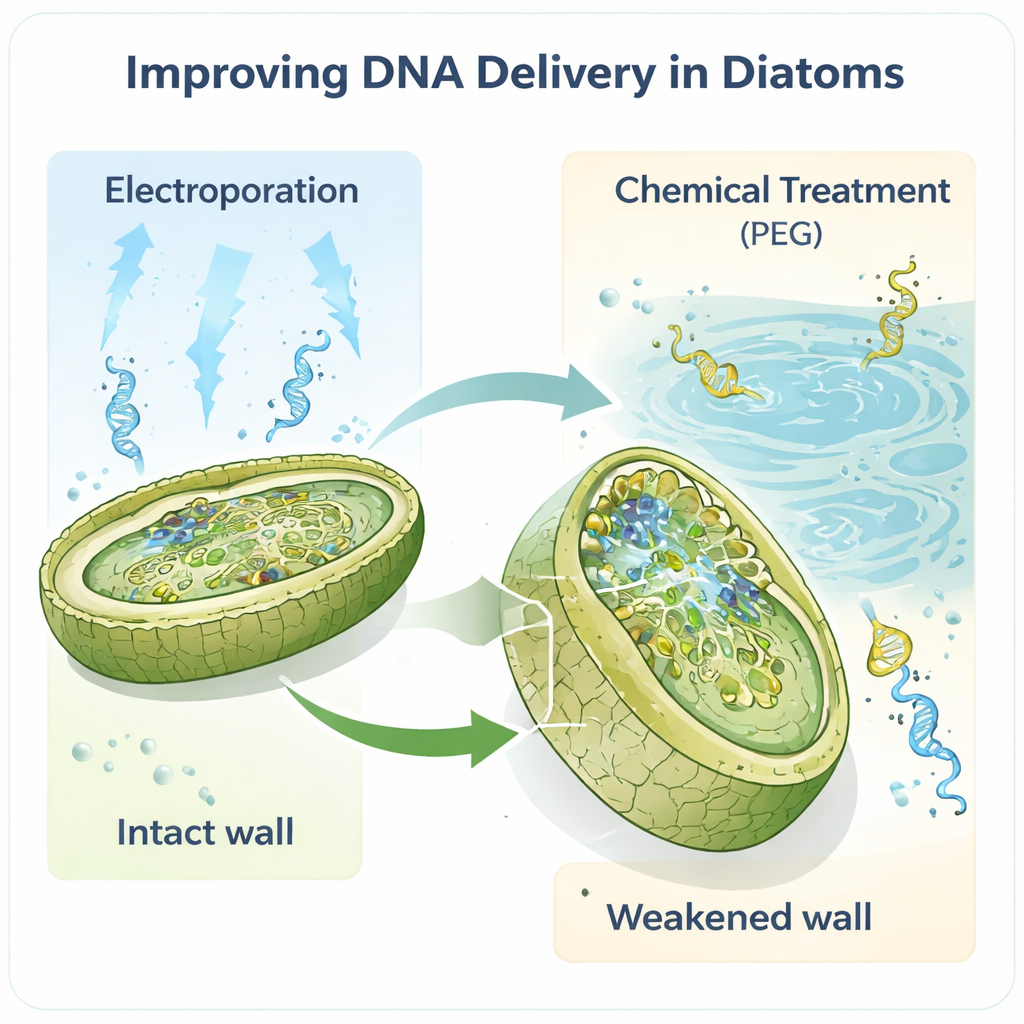
Snel DNA‑transport zonder omweg via bacteriën
Traditionele methoden om diatoomgenetica te wijzigen vertrouwen vaak op bacteriële “koeriers” om grote cirkelvormige DNA‑moleculen, episomen genoemd, naar algen te brengen. Hoewel effectief is die aanpak traag, technisch veeleisend en kan ze delicaat DNA destabiliseren. De nieuwe protocollen tonen aan dat zowel electroporatie als een verfijnde chemische methode met polyethyleenglycol (PEG) episomen rechtstreeks in diatoomcellen kunnen brengen, zonder de bacteriële tussenstap. Opmerkelijk genoeg konden episomen tot 55,6 duizend basenparen lengte intact worden afgeleverd en teruggewonnen. Dezelfde strategieën werkten ook in een tweede soort, Thalassiosira pseudonana, die een zwaarder gemineraliseerde wand heeft, wat suggereert dat dit een breed toepasbare gereedschapsset is in plaats van een truuk voor één soort.
De cel laten bouwen aan zijn eigen genetische cirkels
Terwijl ze onderzochten hoe electroporeerd DNA zich in de cellen gedroeg, stuitte het team op een verrassende vaardigheid: diatomeeën kunnen DNA‑fragmenten zelf aan elkaar zetten. Lineaire stukken van episomen drongen de cel binnen en werden hersteld tot cirkels, hetzij door onnauwkeurige “niet‑homologe” koppeling, hetzij door nauwkeuriger, overlapgestuurde “homologe” reparatie. De auteurs doopten dit proces “diatom in vivo assembly”, of DIVA. Door overlappende fragmenten te ontwerpen, bewerkten ze cellen om twee, drie of vier stukken tot volledige episomen samen te voegen met hoge succespercentages, soms zelfs met opname van kleine synthetische cassettejes die fluorescerende merkers of nieuwe functies toevoegen. Deze eigenschap verandert de diatoomkern in een miniatuur DNA‑werkplaats en kan arbeidsintensieve assemblagestappen vervangen die gewoonlijk in gist of E. coli worden uitgevoerd.
Genoom bewerken alleen met eiwitcomplexen
Buiten het toevoegen van episomen toonden de onderzoekers aan dat ze kant‑en‑klare CRISPR–Cas9 eiwit‑RNA‑complexen rechtstreeks in diatoomcellen konden afleveren met hun geoptimaliseerde electroporatiemethode. Door te mikken op een gen dat PtAPT heet, dat de gevoeligheid voor een toxische adenine‑achtige stof reguleert, genereerden ze duizenden resistente mutanten zonder extra DNA in het genoom te introduceren. Velen van deze mutanten droegen kleine inserties of deleties op de doellocatie; sommige vingen zelfs stukjes “drager‑DNA” op die waren toegevoegd om de elektrische schok te bufferen. Het team leverde vervolgens in één stap zowel CRISPR‑complexen als episomen mee en ontdekte dat ongeveer één op de tien koloniën zowel een genomische wijziging als een selecteerbaar episoom droeg — een efficiënte manier om anders onzichtbare genveranderingen te volgen. 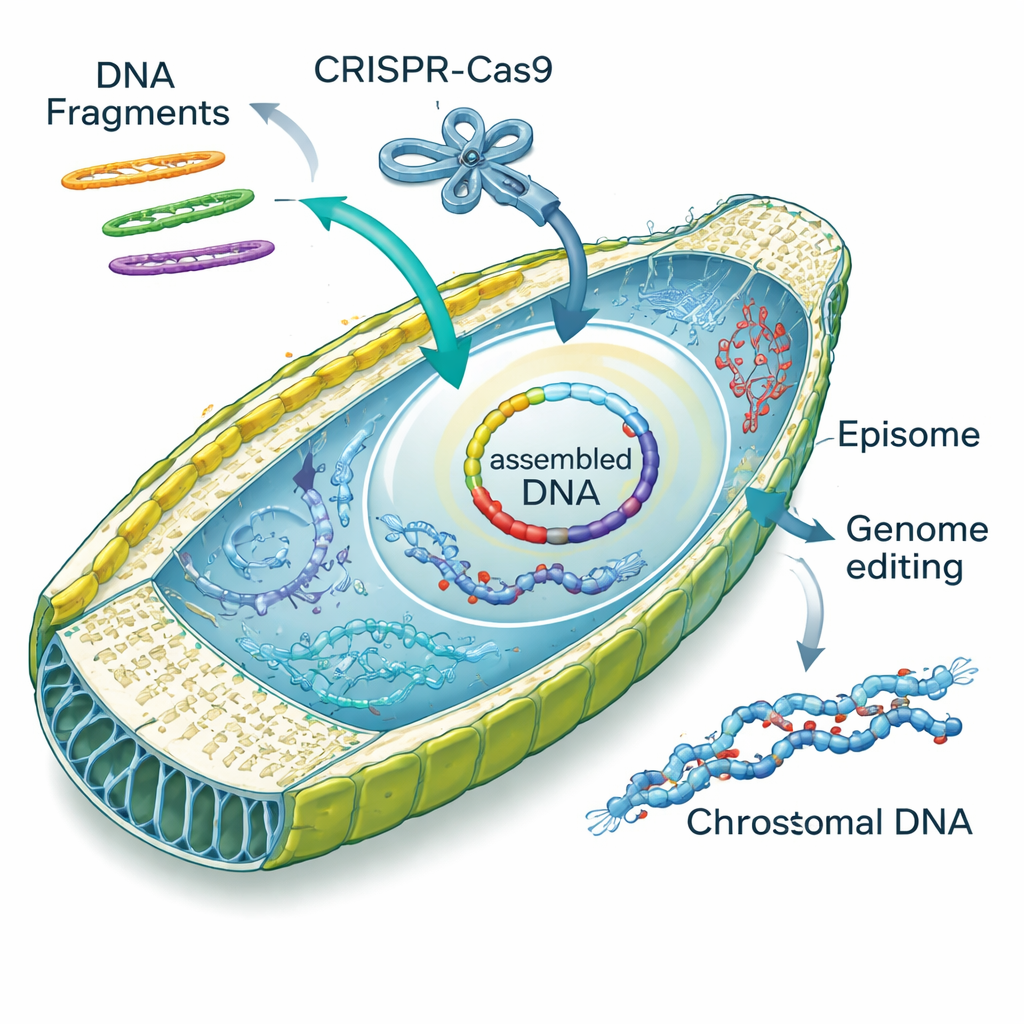
Op weg naar ontwerpdiatomeeën voor een duurzame toekomst
Voor niet‑specialisten is de kernboodschap dat diatomeeën veel dichter bij praktische, programmeerbare organismen komen. Door de celwand voorzichtig te breken of te verzachten veranderden de auteurs een kieskeurige, laagopbrengende procedure in een robuuste pijplijn die weinig DNA verbruikt, werkt met grote genetische constructen en zelfs de cel toestaat zijn eigen DNA te assembleren en te bewerken. Deze vooruitgang verkort het pad van een door de computer ontworpen sequentie naar een levend, getest stam. Op de lange termijn zouden dergelijke hulpmiddelen de pogingen kunnen versnellen om diatomeeën met volledig synthetische chromosomen te bouwen en deze oceaanmicroben te benutten voor schonere brandstoffen, klimaatvriendelijke chemie en nieuwe biologische ontdekkingen.
Bronvermelding: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Trefwoorden: diatoombiotechnologie, genetische transformatie, CRISPR-genoombewerking, synthetische biologie, microalgen‑engineering