Clear Sky Science · nl
Structuren van nucleotide-gebonden menselijke telomerase in verschillende stappen van de cyclus voor het toevoegen van telomerische DNA-herhalingen
Waarom de uiteinden van onze chromosomen ertoe doen
Elke keer dat een cel zich deelt, worden de beschermende kapjes aan de uiteinden van onze chromosomen — de zogeheten telomeren — een beetje korter. Als ze te kort worden, stoppen cellen met delen of functioneren ze niet goed, wat bijdraagt aan veroudering en ziekte. Een moleculair apparaat dat telomerase heet, kan deze kapjes weer opbouwen en is buitengewoon actief in de meeste vormen van kanker. Deze studie onthult, met ongekende detaillering, hoe menselijke telomerase telomeren stap voor stap vastgrijpt en verlengt, wat aanwijzingen geeft voor hoe we dit enzym in de toekomst mogelijk kunnen bijsturen bij ouderdomsgebonden aandoeningen en kanker.
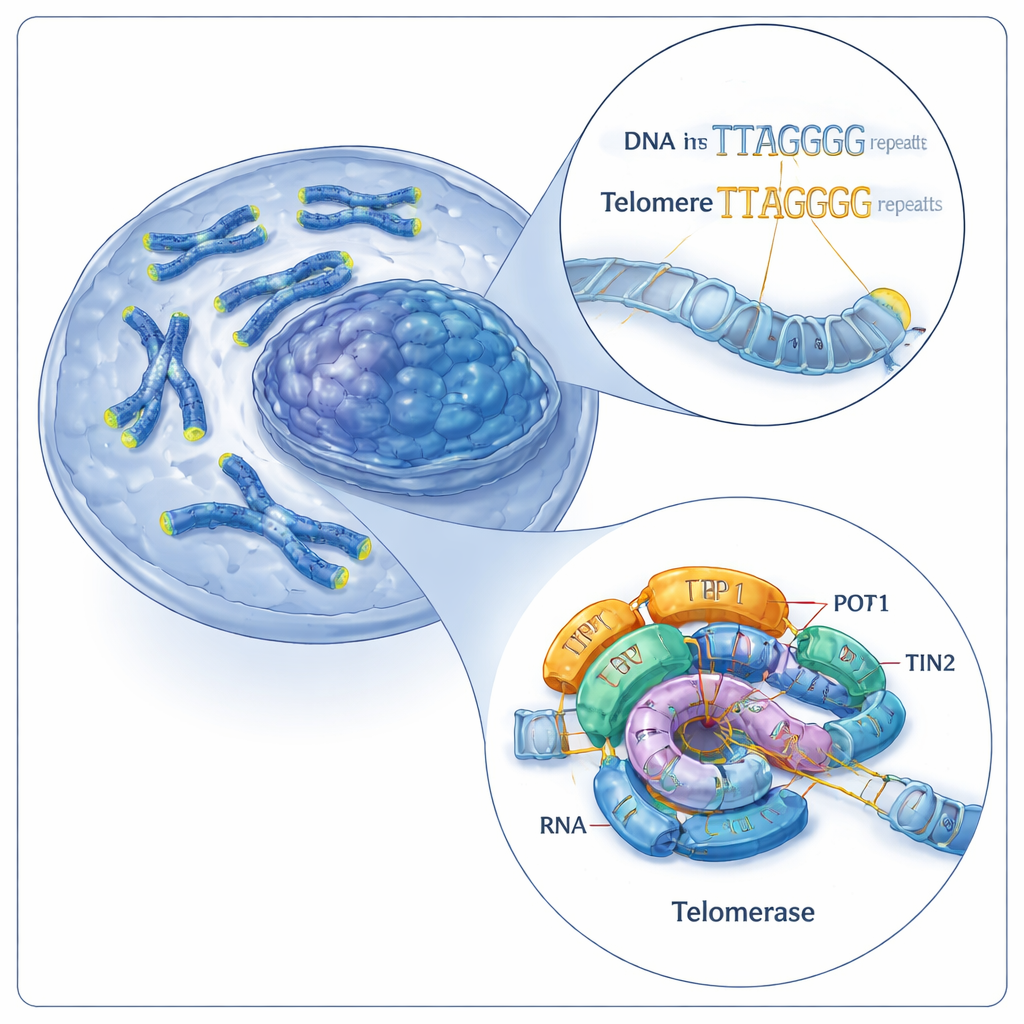
Het reparatieteam voor de chromosoomkap van de cel
Telomeren bestaan uit korte, herhaalde DNA-sequenties (bij mensen een patroon van zes letters: TTAGGG). Telomerase verlengt telomeren door meer van deze herhalingen aan de uiteinden van chromosomen toe te voegen. Het doet dit met twee hoofdcomponenten: een eiwit genaamd telomerase reverse transcriptase (TERT) en een ingebouwd RNA-molecuul (hTR) dat als sjabloon fungeert. Samen vormen deze componenten een katalytische kern, die verder wordt ondersteund door hulp-eiwitten bekend als shelterin, waaronder een trio genaamd TPP1–POT1–TIN2. Eerder werk had menselijke telomerase slechts in één werktoestand in beeld gebracht, waardoor een belangrijke vraag open bleef: hoe slaagt dit apparaat erin herhaaldelijk nieuwe herhalingen toe te voegen zonder van het DNA los te raken?
Telomerase in actie bevroren
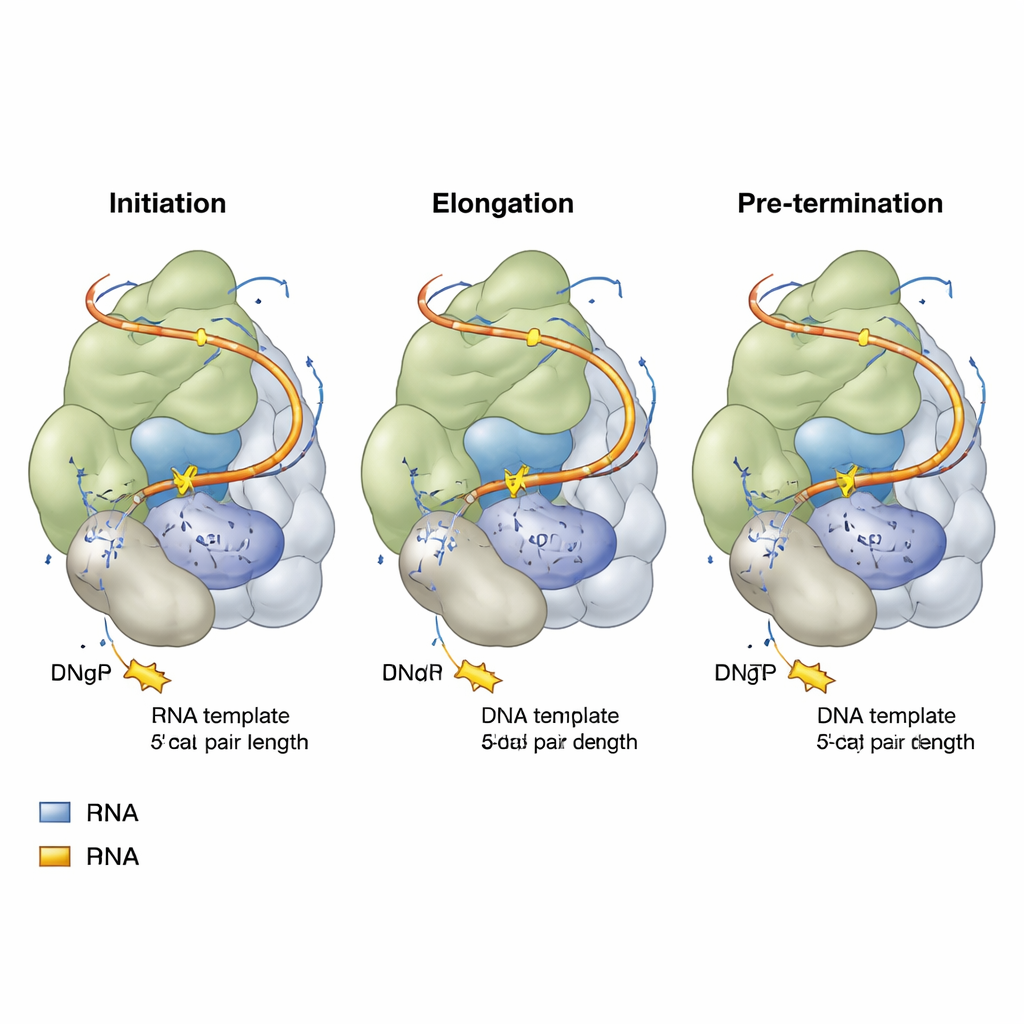
De onderzoekers bouwden menselijke telomerase opnieuw op in humane cellen en assembleerden het vervolgens met zorgvuldig ontworpen stukken telomerisch DNA en niet-reactieve nucleotide-analogen — moleculen die lijken op de letters van DNA maar niet volledig kunnen worden ingebouwd. Met behulp van hoge-resolutie cryo-elektronenmicroscopie vingen ze momentopnamen van telomerase in drie sleutelstadia van zijn cyclus voor het toevoegen van herhalingen: het begin (initiëren), het midden van het kopiëren (verlenging) en net voordat een herhaling wordt voltooid (pre-terminatie). Iedere opname toonde de katalytische kern van telomerase die een korte hybride van DNA en RNA omarmt, met een binnenkomend nucleotide gepositioneerd in het actieve centrum, klaar om aan de groeiende DNA-keten te worden toegevoegd.
Een klein ritsje dat een groot proces regelt
Bij alle drie de stadia kwam een verrassend thema naar voren: de DNA–RNA-hybride binnen telomerase blijft in wezen dezelfde lengte — slechts vier basenparen lang, tijdelijk uitgebreid tot vijf wanneer een nieuw nucleotide binnenkomt. Een specifiek aminozuur in TERT, bijgenaamd een 'ritskop', markeert consequent het einde van deze korte hybride en voorkomt dat deze langer wordt. Terwijl nieuwe DNA-letters worden toegevoegd, smelt een basenpaar aan het verre uiteinde weg, zodat de hybride nooit verder uitgroeit dan dit krappe venster van vier tot vijf paar. Dit compacte ontwerp vergemakkelijkt waarschijnlijk het scheiden en verplaatsen van de strengen, waardoor het enzym zich kan verplaatsen en de volgende herhaling kan starten zonder het DNA volledig los te laten. Subtiele verschillen in welke DNA- en RNA-letters dit korte hybride bezetten verklaren waarom sommige telomerische eindsequenties sterker aan telomerase binden dan andere.
Flexibele RNA-verbindingen en bewegende onderdelen
Het RNA-sjabloon binnen telomerase zweeft niet vrij; het is vastgemaakt door flexibele stukken aan beide zijden, de zogeheten 5′- en 3′-templateschakels. Terwijl telomerase vordert van initatie naar pre-terminatie, wordt de upstream (5′) schakel strakgetrokken als een bungeekoord en bereikt uiteindelijk een volledig uitgerekte toestand die helpt het einde van een herhaling te signaleren. Ondertussen puilt de downstream (3′) schakel naar buiten en nadert een andere RNA-structuur (de P6.1-stam-lus) en nabijgelegen eiwitgebieden. Als deze schakels te kort of te lang worden, of als P6.1 wordt gewijzigd, daalt het vermogen van telomerase om herhaling na herhaling toe te voegen sterk. Belangrijk is dat bepaalde eiwitregio’s — het TEN-domein en een telomerase-specifieke insert die de TRAP-wig wordt genoemd — als verstelbare geleiders fungeren en zowel het DNA als deze RNA-schakels raken. Mutaties die het volume van de TRAP-wig verkleinen, kunnen het enzym zelfs procesiever maken, wat suggereert dat deze wig normaal gesproken fungeert als een gecontroleerde barrière die de timing van het sjabloonverplaatsing regelt.
Nieuwe inzichten in een therapeutisch doelwit
Door structurele momentopnamen te combineren met functietests van gerichte mutaties, stelt de studie een gedetailleerd mechanisch model voor over hoe menselijke telomerase herhaaldelijk telomeren verlengt. Het enzym houdt een zeer korte DNA–RNA-hybride vast, gebruikt een ritsachtig residue om die lengte af te dwingen, en vertrouwt op flexibele RNA-schakels en beweeglijke eiwitelementen om het sjabloon te verplaatsen en het DNA verankerd te houden tijdens meerdere kopieerronden. Voor niet-specialisten is de kernboodschap dat telomerase niet werkt als een statische kopieermachine maar als een fijn afgestelde, veerbelaste inrichting waarvan de geometrie en bewegende onderdelen bepalen hoe lang en hoe efficiënt het telomeren kan onderhouden. Het begrijpen van dit choreografie opent de deur naar geneesmiddelen die telomerase in kankers kunnen dempen of zijn functie kunnen stabiliseren bij ziekten van voortijdige veroudering.
Bronvermelding: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Trefwoorden: telomerase, telomeren, cryo-EM, genoomstabiliteit, kankerbiologie