Clear Sky Science · nl
DNA-methylering en lncRNA reguleren asynchrone DNA-replicatie in specifieke geïmprimeerde gen-domeinen
Waarom het kopieerschema van DNA in de cel ertoe doet
Elke keer dat een cel zich deelt, moet hij zijn volledige DNA kopiëren, maar niet alle regio’s worden op hetzelfde moment verdubbeld. Sommige stukken worden vroeg gekopieerd, andere laat, volgens een nauwkeurig “timetable” voor het genoom. Dit artikel onderzoekt waarom in een paar bijzondere genclusters die onthouden van welke ouder ze afkomstig zijn, de maternale en paternale kopieën op verschillende tijdstippen worden gekopieerd. Inzicht in dit ongebruikelijke tijdschema werpt licht op hoe chemische labels op DNA en lange niet-coderende RNA’s (lncRNA’s) het genoom helpen organiseren en mogelijk ontwikkeling en ziekte beïnvloeden.
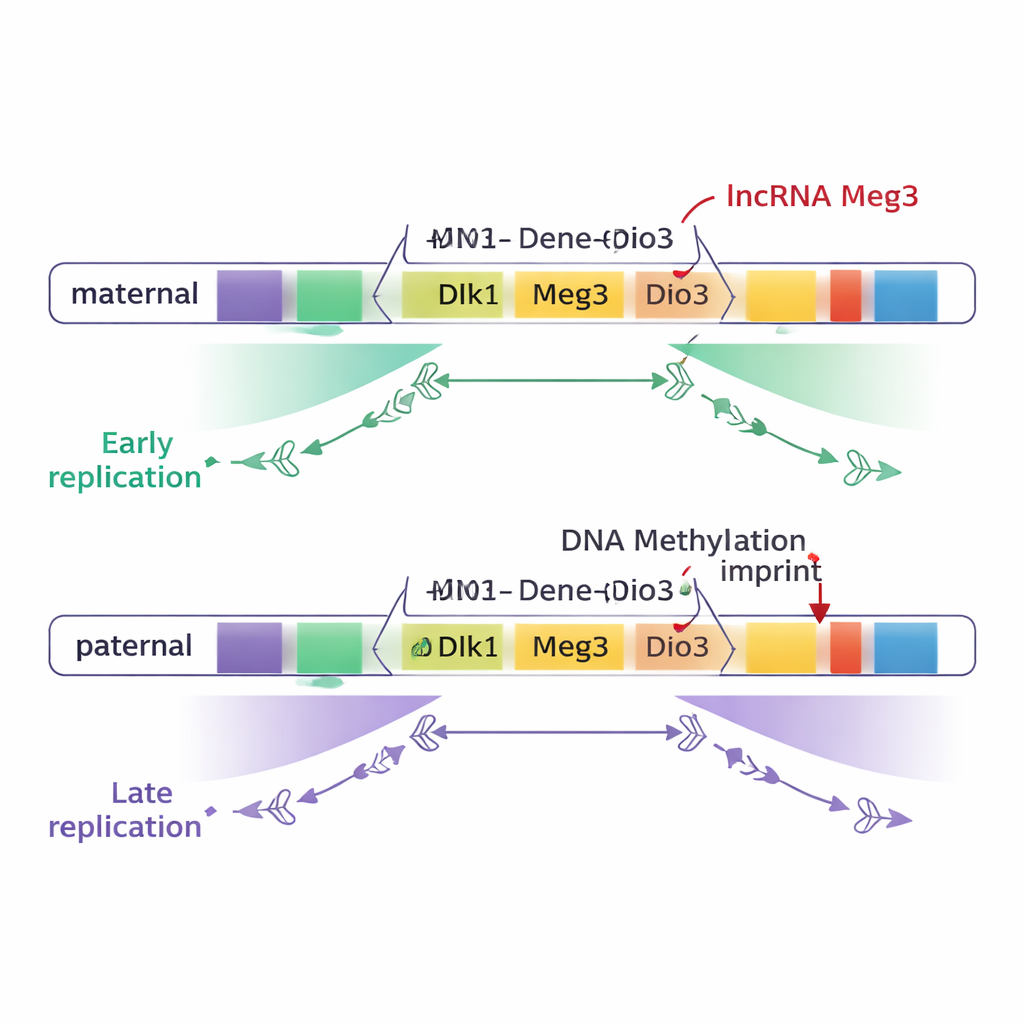
Ouderlijke herinneringen geschreven op DNA
Bij zoogdieren vertonen een klein aantal “geïmprimeerde” gen-domeinen verschillend gedrag, afhankelijk van of ze van de moeder of de vader zijn geërfd. Dit effect van ouderlijke herkomst wordt gereguleerd door DNA-methylering — kleine chemische markeringen die aan specifieke regio’s worden toegevoegd, bekend als differentieel gemethyleerde regio’s (DMR’s) — en door veranderingen in de vouwing van chromosomen. De auteurs bestudeerden muis-embryonale stamcellen, die op zeer vroege embryonale cellen lijken. Ze vergeleken cellen met alleen maternale genomen, alleen paternale genomen, en normale hybriden met één van elk. Door te volgen wanneer stukken DNA tijdens de celcyclus werden gekopieerd, bepaalden ze de replicatietiming over het genoom en zoomden ze in op bekende geïmprimeerde gebieden.
Twee geïmprimeerde gebieden breken de regels
Het grootste deel van het genoom, inclusief de meeste geïmprimeerde domeinen, bleek op hetzelfde moment te worden gekopieerd op maternale en paternale chromosomen. Twee grote geïmprimeerde gebieden sprongen er echter uit: het Dlk1–Dio3-domein op chromosoom 12 en het Snrpn-gebied op chromosoom 7. In deze zones werd een breed stuk DNA — ongeveer driekwart miljoen basenparen bij Dlk1–Dio3 — vroeg gekopieerd op het ene ouderlijke chromosoom en laat op het andere. Cruciaal is dat dit verschil de ouderlijke herkomst volgde, niet de stamachtergrond: de maternale kopie van sleutelgenen zoals Dlk1 en het lncRNA-gen Meg3 replicateerde consequent vroeg, terwijl de paternale kopieën laat replicaeerden.
DNA-methylering stelt de timing-schakelaar in
Om te testen wat dit tijverschil veroorzaakt, maakten de onderzoekers stamcellen waarin het normale methyleringspatroon bij DMR’s ofwel werd uitgewist ofwel op beide ouderlijke chromosomen werd afgedwongen. Wanneer beide ouderlijke kopieën van de Dlk1–Dio3-DMR’s gemethyleerd waren, replikeerde het hele gebied laat op beide chromosomen. Wanneer methylering grotendeels van beide kopieën werd verwijderd, replikeerde datzelfde gebied vroeg op beide. Vergelijkbare experimenten bij Snrpn leidden eveneens tot verlies van timingverschillen. Deze resultaten tonen aan dat ouder-specifieke DNA-methylering essentieel is om het vroeg-tegenover-laat replicatiecontrast tussen maternale en paternale chromosomen te creëren, althans in deze twee domeinen.
Een lang RNA verfijnt vroege replicatie
DNA-methylering alleen bleek echter niet het hele verhaal. Het Dlk1–Dio3-gebied produceert ook een lang niet-coderend RNA genaamd Meg3 als onderdeel van een groot RNA-“polycistron”. Op het maternale chromosoom laten niet-gemethyleerde DMR’s Meg3 tot expressie komen; op het paternale chromosoom houdt methylering het stil. Door precieze deleties te creëren die Meg3 uitschakelden terwijl de DNA-methylering intact bleef, toonden de auteurs aan dat verlies van Meg3-RNA specifieke delen van het maternale domein deed verschuiven van vroeg naar later repliceren. Met andere woorden: Meg3-RNA helpt de vroege kopieering van nabije stukken van het maternale chromosoom te bevorderen en voegt daarmee een tweede regellaag toe bovenop DNA-methylering.
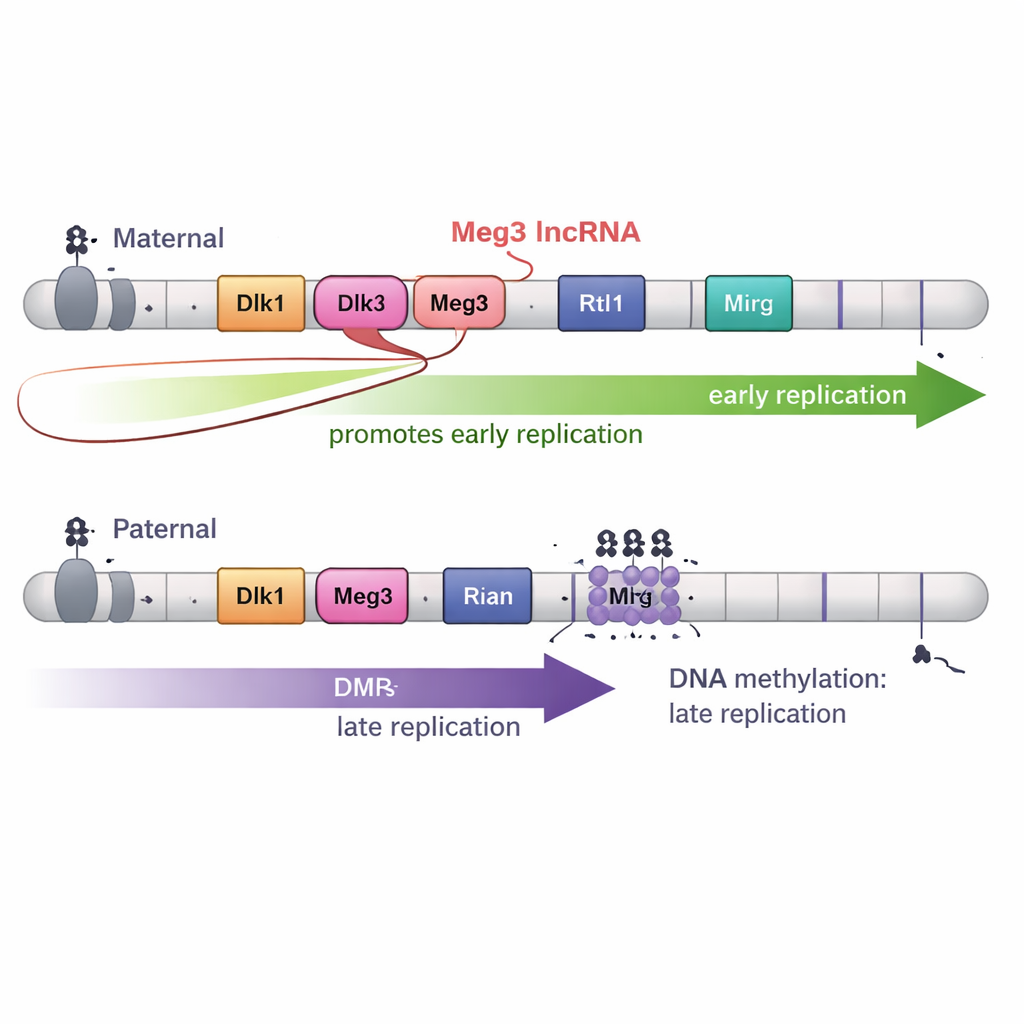
3D-vouwing en ontwikkeling brengen extra wendingen
Aangezien vouwing van het genoom vaak gekoppeld is aan replicatietiming, bracht het team ook de 3D-chromosoomarchitectuur in kaart met hoge resolutie. Verrassend genoeg kwamen in het Dlk1–Dio3-gebied de grenzen van 3D-domeinen niet overeen met de grenzen van vroege en late replicatie. Zelfs wanneer methyleringspatronen werden gewijzigd en de replicatietiming veranderde, verschoof de basisvouwstructuur — topologisch geassocieerde domeinen — op andere manieren. Tenslotte, wanneer de stamcellen werden gedifferentieerd naar neurale voorlopercellen, verdwenen de spectaculaire timingverschillen tussen maternale en paternale kopieën grotendeels, hoewel imprintingsmarkeringen en veel aspecten van de 3D-structuur bleven bestaan. Dit suggereert dat ontwikkelingssignalen het bijzondere vroeg-tegenover-laat patroon in stamcellen kunnen overschrijven.
Wat dit in eenvoudige termen betekent
Deze studie toont aan dat in een paar bijzondere genbuurten die onthouden van welke ouder ze komen, het kopieerschema van het DNA van de cel wordt gereguleerd door een combinatie van chemische labels op DNA en lange niet-coderende RNA’s. DNA-methylering bij geïmprimeerde controlegebieden zet een basis vroege-of-late timing voor elk ouderlijk chromosoom, en het Meg3-lncRNA duwt omliggend maternale DNA verder richting vroegere kopieëring. Deze effecten werken grotendeels onafhankelijk van de 3D-vouw van het chromosoom. Tijdens de ontwikkeling, naarmate cellen specialiseren, vervaagt dit ongebruikelijke tijdschema, wat laat zien dat het een kenmerk is van de pluripotente stamceltoestand. Samen verklaren de resultaten hoe ouderlijke epigenetische “herinneringen” en niet-coderende RNA’s lokaal het gebruikelijke replicatieschema van het genoom kunnen overschrijven.
Bronvermelding: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Trefwoorden: genomische imprinting, DNA-methylering, replicatietiming, lange niet-coderende RNA's, embryonale stamcellen