Clear Sky Science · nl
Endotheliale FUNDC1 reguleert metabolische herprogrammering en de overgang van obesitas naar diabetes via de SIRT3/GATA2/endotheline-1-as
Waarom cellen van bloedvaten ertoe doen bij obesitas en diabetes
Obesitas en type 2 diabetes worden vaak toegeschreven aan vetweefsel, de lever of de alvleesklier. Maar deze studie wijst op een verrassende dader: de dunne laag cellen die onze bloedvaten bekleedt, de endotheelcellen. De onderzoekers laten zien dat een klein mitochondriaal eiwit in deze cellen, FUNDC1 genaamd, het lichaam kan helpen van eenvoudig gewichtstoename naar volledige diabetes te verschuiven door te veranderen hoe bloedvaten communiceren met metabole organen.
Stress op de binnenste “huid” van het lichaam
Endotheelcellen vormen een uitgestrekt, fijnmazig netwerk dat de bloedstroom, de toevoer van voedingsstoffen en signalen naar omliggende weefsels reguleert. In gezonde omstandigheden houden ze ontspannende factoren zoals stikstofoxide in balans met vernauwende factoren zoals endotheline-1 (ET-1). Bij obesitas en beginnende diabetes slaat die balans door naar ET-1, dat niet alleen bloedvaten vernauwt, maar ook verstoort hoe vet-, spier- en levercellen omgaan met suiker en vet. De auteurs tonen eerst aan dat bij muizen vaatfunctiestoornis al optreedt na slechts twee maanden op een vetrijk dieet, voordat duidelijke insulinestatus-achterstand (insulineresistentie) ontstaat, wat suggereert dat beschadigd endothelium metabole ziekte kan helpen veroorzaken in plaats van er alleen op te reageren.
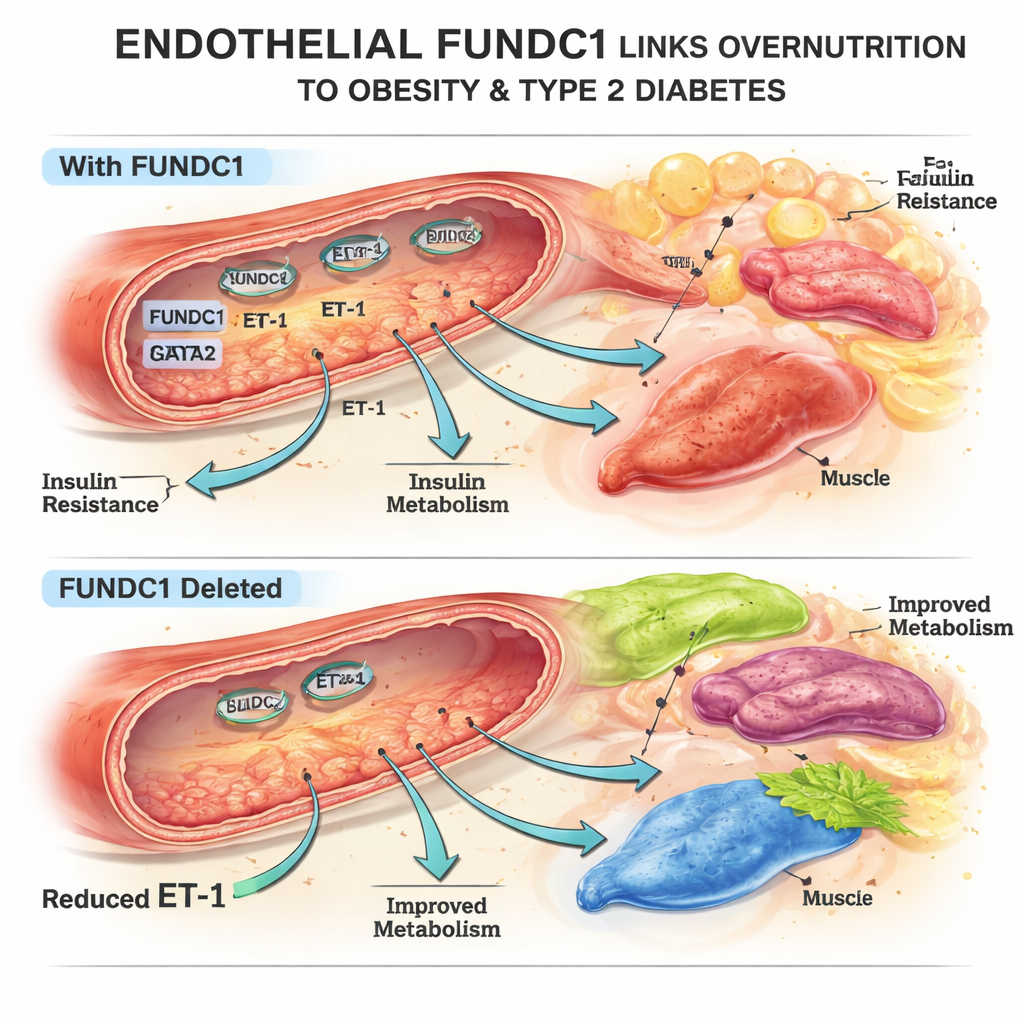
Een mitochondriaire schakelaar die lichaamsvet vormt
Het team richtte zich op FUNDC1, een eiwit aan het oppervlak van mitochondriën, de energiecentrales van de cel. In muis- en menselijke endotheelcellen die aan overtollig vet werden blootgesteld, veranderden de FUNDC1-niveaus in de tijd: ze daalden aanvankelijk en stegen vervolgens sterk bij langdurige overvoeding. Met genetisch gemodificeerde muizen die FUNDC1 alleen in endotheelcellen misten, ontdekten de onderzoekers dat deze dieren deels beschermd waren tegen gewichtstoename door een vetrijk dieet: ze hadden minder lichaamsvet, kleinere vetcellen en betere bloedsuikerregeling. Hun vet-, lever- en bruinvetweefsel reageerden sterker op insuline, hoewel de insulinespiegels zelf niet hoger waren. Deze veranderingen vielen niet te verklaren door verschillen in voedselinname of activiteit, en wijzen in plaats daarvan op de invloed van de vasculatuur op de stofwisseling.
Een chemische boodschapper die insulineresistentie aandrijft
Om te achterhalen hoe endotheliale FUNDC1 verre organen beïnvloedt, schermden de auteurs verschillende stoffen die door endotheelcellen worden uitgescheiden. Eén stof viel op: ET-1. Wanneer FUNDC1 in endotheelcellen werd verwijderd, daalde de ET-1-productie in bloedvaten en in de bloedbaan sterk, zowel onder normale als onder vetrijkedieetcondities. Experimenten in gekweekte vetcellen, levercellen en spiercellen lieten zien dat ET-1 pre-adipocytenstimuleerde, vetopslag en -afbraak veranderde en de vetophoping in lever en spier verergerde bij blootstelling aan veel vet—een patroon dat bekendstaat als bevorderlijk voor insulineresistentie. In levende muizen wist het toedienen van ET-1 aan het begin van een vetrijk dieet de beschermende voordelen van endotheliale FUNDC1-verwijdering teniet te doen: lichaamsgewicht, vetmassa, bloedsuikercontrole en vaatfunctie verslechterden allemaal, waarmee ET-1 wordt bevestigd als een sleutelverbinding tussen endotheel en metabole ziekte.
Een interne signaalas: FUNDC1, SIRT3 en GATA2
De studie brengt vervolgens een gedetailleerde moleculaire keten binnen endotheelcellen in kaart. Bij vethigh-stress verplaatst een lange vorm van het enzym SIRT3 (SIRT3-L), die zowel in de kern als in mitochondriën kan voorkomen, zich met behulp van FUNDC1 en een chaperonne-eiwit genaamd HSC70 van de kern naar mitochondriën. Eenmaal in de mitochondriën is er minder SIRT3-L beschikbaar in de kern om acetylgroepen van GATA2 te verwijderen, een transcriptiefactor die de ET-1-genactiviteit verhoogt. Meer geacetyleerde GATA2 is stabieler en stimuleert meer ET-1-productie. Wanneer FUNDC1 ontbreekt, blijft SIRT3-L in de kern, waar het GATA2 deacetyleert, wat leidt tot afbraak van GATA2 en lagere ET-1-productie. Intrigerend genoeg bevordert SIRT3 op zijn beurt de afbraak van FUNDC1, waardoor een feedbacklus ontstaat die normaal gesproken de route in toom houdt maar tijdens chronische overvoeding ontregeld raakt.
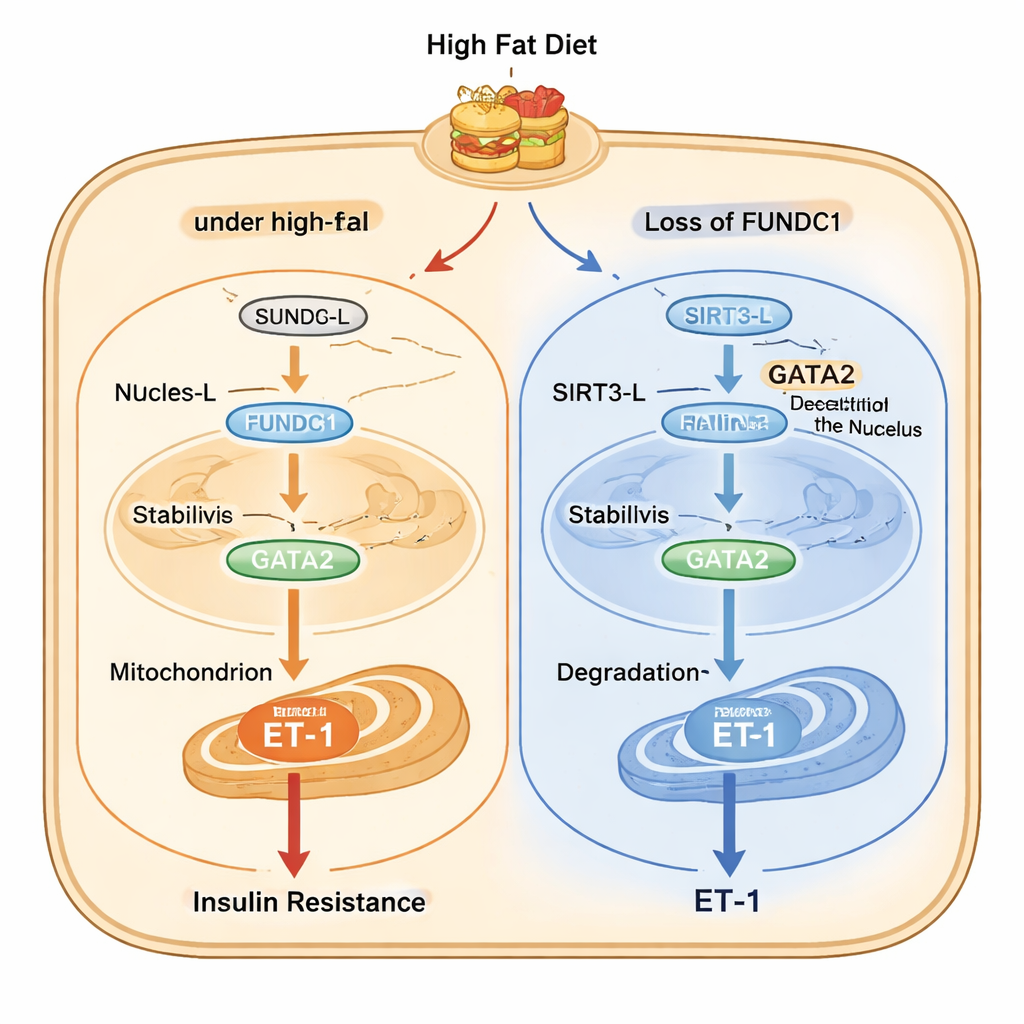
Van muismodellen naar menselijke ziekte
Om te testen of dit mechanisme ook bij mensen relevant is, onderzochten de onderzoekers bloed en kleine slagaders van personen met obesitas en type 2 diabetes en van gezonde vrijwilligers. Patiënten met beide aandoeningen hadden hogere bloedspiegels van ET-1 en hogere expressie van FUNDC1, GATA2 en het ET-1-gen in hun vaatbekleding. De hoeveelheid ET-1 in het bloed correleerde sterk met de body mass index en met de lange-termijn bloedsuikerwaarde (HbA1c), en vaat-ET-1-genlevels correleerden sterk met FUNDC1 en GATA2. Deze patronen spiegelen de bevindingen bij muizen en ondersteunen het idee dat een overactieve FUNDC1–SIRT3–GATA2–ET-1-as werkzaam is in menselijk vasculair weefsel onder metabole stress.
Een nieuw doelwit in de strijd tegen diabetes
Voor niet-specialisten is de kernboodschap dat schade door overeten zich mogelijk eerst manifesteert in de cellen die onze bloedvaten bekleden. Daar helpt een mitochondriaal eiwit, FUNDC1, een regulerend enzym, SIRT3, uit de kern te verplaatsen, waardoor een andere factor, GATA2, de productie van ET-1 kan opvoeren—een krachtige hormoonachtige signaler die zowel vaatversteviging als insulineresistentie bevordert. Het blokkeren van deze route—door de activiteit van endotheliale FUNDC1 te verminderen of ET-1 te remmen—zou kunnen helpen voorkomen dat obesitas overgaat in diabetes en tegelijkertijd bloedvaten beschermen.
Bronvermelding: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
Trefwoorden: endotheelcellen, mitochondriën, endotheline-1, obesitas, type 2 diabetes