Clear Sky Science · nl
Interactie tussen adipocytaire sclerostine loop3 en LRP4 vereist door sclerostine om de vet- en glucosestofwisseling in het hele lichaam te verstoren
Waarom botten ertoe doen voor de bloedsuiker
De meeste mensen zien botten als levenloze steigers, maar botcellen geven stilletjes hormonen af die met de rest van het lichaam communiceren. Deze studie onthult hoe één zo’n botproteïne, sclerostine genoemd, helpt twee veelvoorkomende problemen bij oudere vrouwen met elkaar te verbinden: broze botten (osteoporose) en type 2 diabetes. Door een specifieke “handdruk” tussen sclerostine en vetcellen bloot te leggen, schetsen de onderzoekers een manier om botten te versterken en bloedsuiker en cholesterol te verbeteren zonder extra belasting voor het hart.
Een botsein dat ontspoort
Sclerostine is een eiwit dat vooral door botcellen wordt gemaakt. Normaal remt het de botvorming en helpt het, enigszins verrassend, ook bloedvaten te beschermen. Het team richtte zich op een klein segment van dit eiwit, loop3 genoemd, en onderzocht of het een rol speelt bij verstoord vet- en suikerbeheer. Ze ontdekten dat vrouwen met postmenopauzale osteoporose die ook type 2 diabetes hadden, evenals mensen die net diabetes waren gediagnosticeerd, hogere sclerostinespiegels in hun bloed hadden dan vergelijkbare personen zonder diabetes. Bij muizen die een vetrijk dieet kregen om metabole stress na te bootsen, steeg het sclerostinegehalte eveneens, samen met gewichtstoename, hogere bloedlipiden en slechtere bloedsuikercontrole. Deze patronen suggereerden dat overtollig sclerostine meer kan zijn dan een bijstander bij metabole ziekte.
Een klein lusje met grote effecten ontleden
Om te begrijpen wat loop3 doet, creëerden de onderzoekers muizen waarin sclerostine werd aangepast of het loop3-segment werd verwijderd. Muizen die te veel normaal sclerostine produceerden, stapelden meer vet op in hun witte vetdepots, hadden grotere vetcellen, hogere circulerende vetzuurspiegels en slechtere glucosetolerantie en insulinerespons dan normale muizen. Wanneer loop3 genetisch werd verwijderd of subtiel gemuteerd, verminderden deze problemen: vetkussens waren kleiner, vetcellen krimpten, bloedlipiden daalden en suikerverwerking verbeterde. Opmerkelijk genoeg traden vergelijkbare voordelen op wanneer muizen werden behandeld met een speciaal ontworpen DNA-achtig middel (een aptameer) dat zich vastklampt aan loop3 en het blokkeren, zonder de hoeveelheid sclerostine in het bloed te veranderen.
Hoe vetcellen het botsein ‘horen’
De groep zoomde vervolgens in op vetcellen om te zien hoe loop3 zijn schadelijke boodschap overbrengt. Ze concentreerden zich op een receptorproteïne op het oppervlak van vetcellen, LRP4 genoemd, eerder bekend als hulp bij sclerostinewerking op bot. Met celkweekexperimenten toonden ze aan dat loop3 fysiek bindt aan een specifiek deel van LRP4 op vetcellen. Dit contact veroorzaakte veranderingen die de capaciteit van de cellen vergrootten om vetten op te bouwen en af te breken en om meer glucose uit het bloed op te nemen, wat leidde tot overgroeide, overactieve vetcellen. Wanneer de wetenschappers sleutelbouwstenen in LRP4 subtiel veranderden zodat loop3 zich niet langer kon hechten, of wanneer ze een klein blokkerend peptide toevoegden dat de LRP4-hechtplaats nabootst, nam het effect van sclerostine op vetopslag en suikeropname sterk af. Zowel in cellen als bij muizen herstelde het blokkeren van deze loop3–LRP4-interactie meer normale vetcelgrootte en verbeterde de glucosetolerantie.
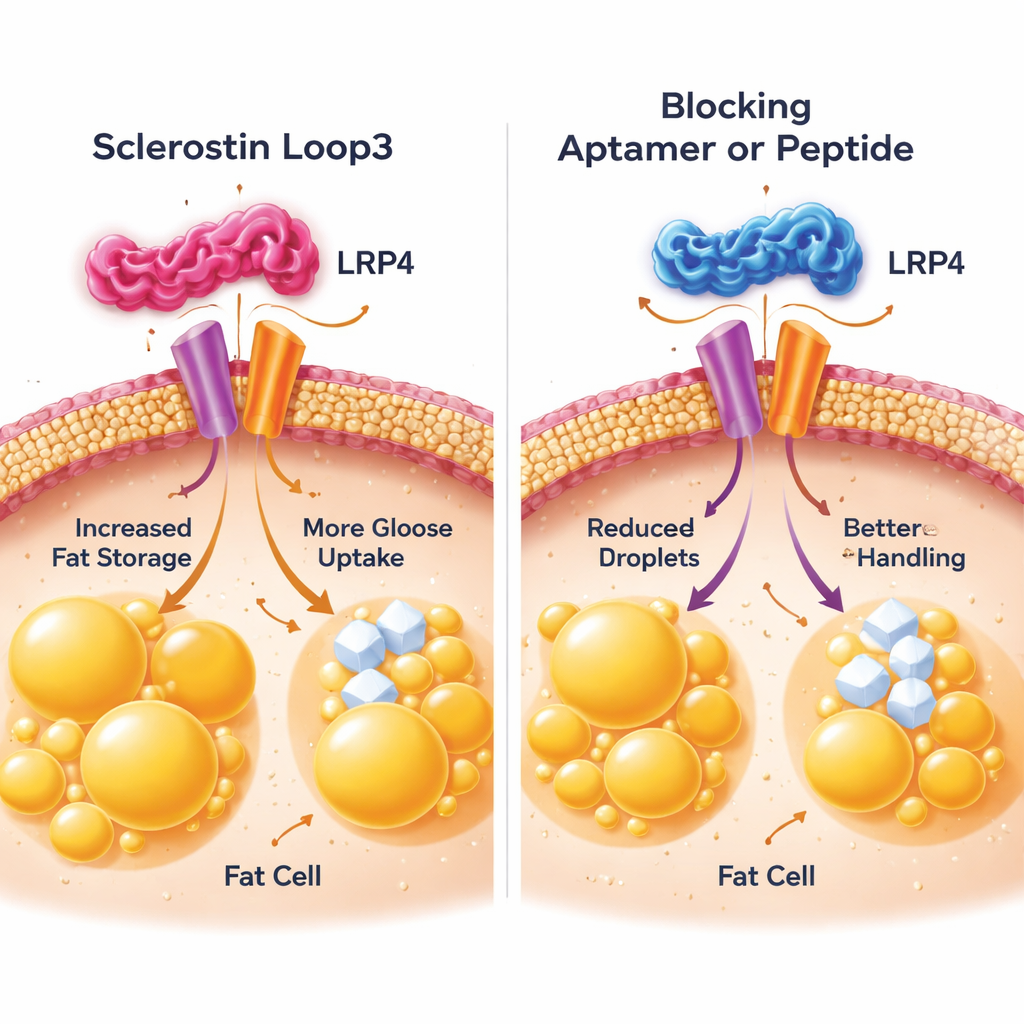
Sterkere botten, gezondere stofwisseling
Een belangrijke zorg bij bestaande sclerostine-blokkerende geneesmiddelen voor osteoporose is dat, hoewel ze bot opbouwen en de stofwisseling verbeteren, toezichthouders hebben gewaarschuwd voor een verhoogd risico op ernstige hartproblemen. Eerder werk van deze groep toonde aan dat loop3 cruciaal is voor sclerostines remming van botvorming, maar niet voor zijn hartbeschermende acties. Hier laten ze verder zien dat het richten op loop3 — hetzij door genetische aanpassingen, hetzij door loop3-gerichte geneesmiddelen — de vet- en suikerstofwisseling in het hele lichaam verbetert in verschillende muismodellen, terwijl ook de botmassa en -sterkte toenemen. In tegenstelling tot huidige medicijnen veroorzaakte deze strategie geen compenserende stijging van een andere botgerelateerde remmer, DKK1, die de voordelen op lange termijn kan afzwakken.
Wat dit voor patiënten kan betekenen
Eenvoudig gezegd betoogt de studie dat een heel klein stukje van één bothormoon zowel slechte botgezondheid als metabole ziekte stimuleert door rechtstreeks met vetcellen te communiceren. Door het gesprek tussen sclerostines loop3-segment en de LRP4-receptor op vetcellen te onderbreken, zou het mogelijk kunnen zijn behandelingen te ontwerpen die botten versterken en bloedlipiden en suikers normaliseren, terwijl de hartbeschermende functies van sclerostine intact blijven. Voor postmenopauzale vrouwen die vaak zowel osteoporose als type 2 diabetes hebben, zouden dergelijke op loop3 gerichte therapieën mogelijk ooit een veiliger, langduriger manier bieden om twee aandoeningen tegelijk te behandelen.
Bronvermelding: Jiang, H., Tao, X., Yu, S. et al. Adipocytic sclerostin loop3-LRP4 interaction required by sclerostin to impair whole-body lipid and glucose metabolism. Nat Commun 17, 1812 (2026). https://doi.org/10.1038/s41467-026-68526-w
Trefwoorden: sclerostine, loop3, LRP4, osteoporose, type 2 diabetes