Clear Sky Science · nl
Palmitinezuur-geïnduceerde palmitoylering van B7H3 bevordert immuunontwijking
Waarom dit onderzoek belangrijk is voor kankerpatiënten
De meeste mensen hebben wel gehoord dat nieuwe immunotherapieën het immuunsysteem kunnen helpen kanker aan te vallen, maar veel patiënten met de veelvoorkomende colorectale (darm)kanker profiteren weinig. Deze studie onthult een verborgen biochemisch trucje dat colorectale tumoren gebruiken om zich te beschermen tegen immuunaanvallen, en wijst op een nieuw soort medicijn — een kort peptide — dat immunotherapie voor deze patiënten effectiever zou kunnen maken.
Een blokkade in de huidige immunotherapie bij darmkanker
Colorectale kanker behoort tot de meest voorkomende kankers wereldwijd. Immunotherapieën die de immuunremmen loslaten, zoals PD‑1- en PD‑L1-remmers, hebben de zorg veranderd voor een minderheid van patiënten wiens tumoren veel DNA-fouten dragen (de zogenaamde MSI‑H tumoren). Helaas zijn de meeste colorectale kankers microsatelliet‑stabiel (MSS) en reageren ze slecht op deze behandelingen. De auteurs concentreerden zich op een andere remmolecuul, B7H3, dat op het oppervlak van tumorcellen zit en de activiteit van dodelijke immuuncellen, vooral CD8+ T‑cellen, dempt. Ze ontdekten dat het B7H3-eiwit sterk verhoogd is in MSS-tumoren en geassocieerd met slechtere overleving, ook al is het onderliggende B7H3-gen niet actiever. Die discrepantie riep een belangrijke vraag op: wat zorgt ervoor dat het B7H3-eiwit zo overvloedig aanwezig blijft op tumorcellen?
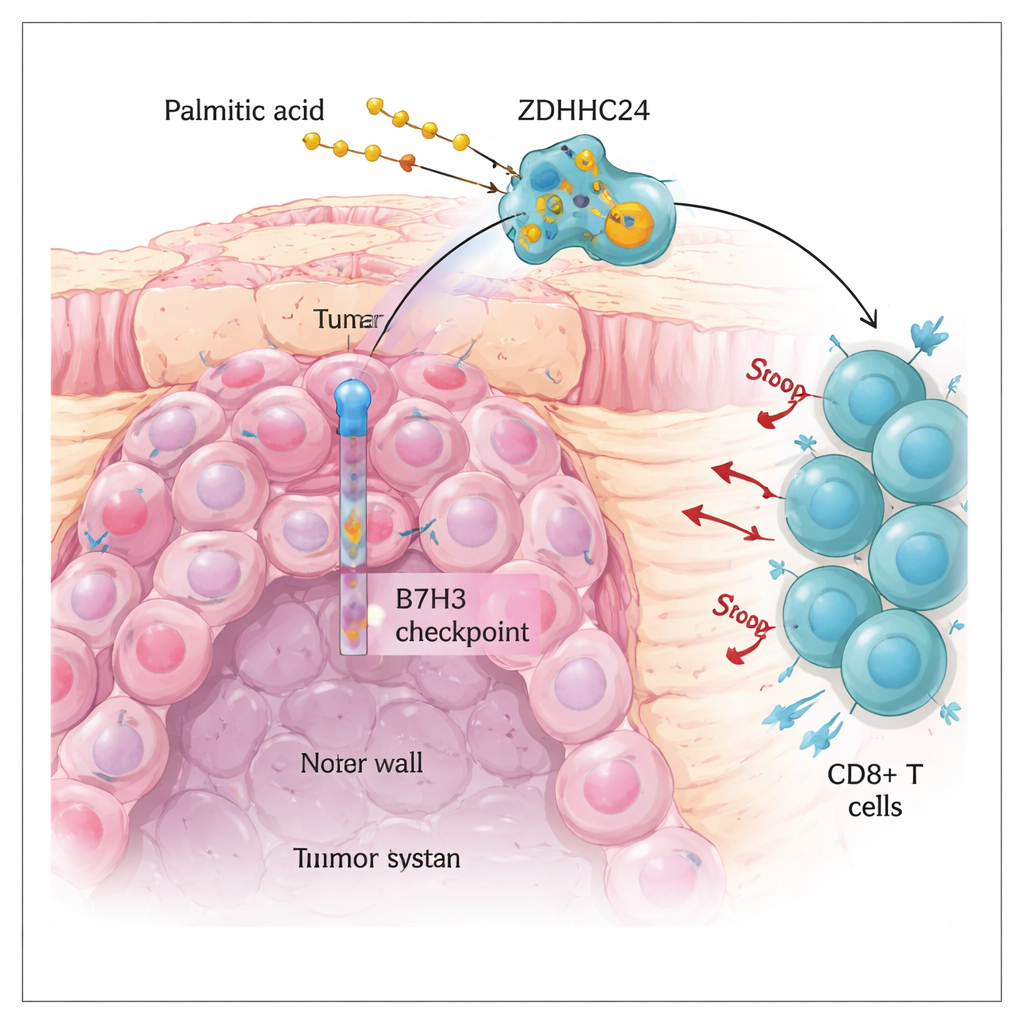
Hoe een veelvoorkomend vet tumoren helpt verbergen
Het team vermoedde dat het tumormetabolisme B7H3 stabiliseert. Door de genactiviteit en kleine-molecuulprofielen van MSS- en MSI‑H-colorectale tumoren te vergelijken, ontdekten ze dat veel vetgerelateerde paden verschillen, waarbij één vetzuur, palmitinezuur, opviel. Wanneer ze colonkankercellen in het laboratorium aan verschillende vetafbraakproducten blootstelden, veroorzaakte alleen palmitinezuur een duidelijke stijging van de B7H3-eiwitniveaus. Verdere experimenten verklaarden waarom: palmitinezuur voedt een chemische modificatie genaamd palmitoylering, waarbij een vetketen aan specifieke plaatsen op eiwitten wordt gehecht. Deze modificatie, uitgevoerd door een enzym genaamd ZDHHC24 op een enkele cysteïne‑positie binnen B7H3, maakte B7H3 stabieler en meer aanwezig op het tumorceloppervlak.
De afvalroute voor een immuunrem blokkeren
Cellen verwijderen normaal ongewenste of beschadigde eiwitten via systemen die functioneren als recycling en vuilnisverwerking. De onderzoekers toonden aan dat B7H3 voornamelijk wordt afgebroken door een cellulair “zelf‑eet” pad dat autophagie heet, en dat de receptor SQSTM1/p62 gebruikt om ladingen voor vernietiging te taggen. Wanneer B7H3 gepalmitoyleerd was, bond het slecht met deze receptor en ontsnapte het aan autophagische afbraak, wat leidde tot aanhoudend hoge niveaus van de immuunrem. Wanneer de palmitoyleringsplaats gemuteerd werd zodat deze het vetlabel niet langer kon dragen, of wanneer het ZDHHC24-enzym werd verwijderd, werd B7H3 efficiënter naar de cellulaire “vuilniszakken” gestuurd en afgebroken. In muizen groeiden tumoren zonder gepalmitoyleerd B7H3 trager, veranderde hun intrinsieke groeisnelheid niet in immuundeficiënte dieren, en vertoonden ze dramatisch meer CD8+ T‑cellen en sterkere tumor‑doderactiviteit. Dit toonde aan dat de modificatie voornamelijk werkt door de immuniteit uit te schakelen, niet door de delingssnelheid van kankercellen te veranderen.
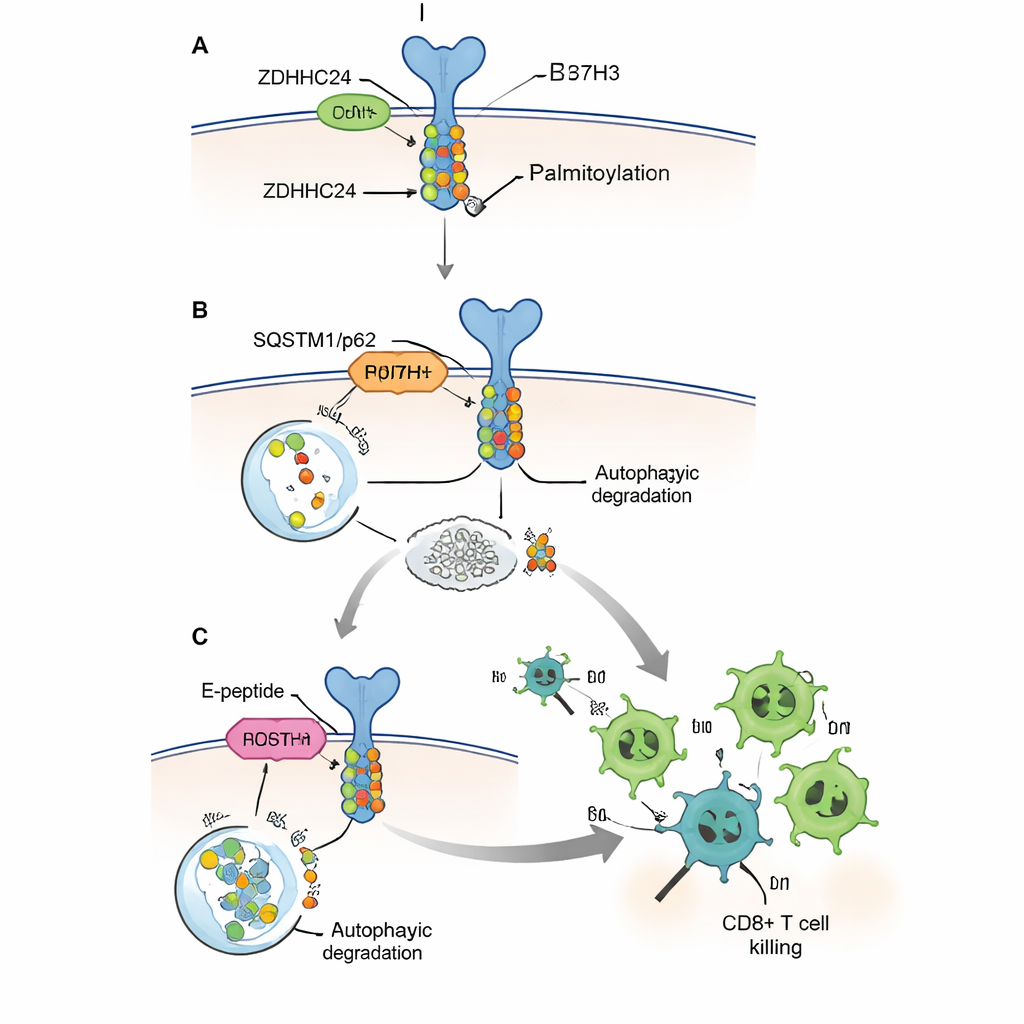
Het schild afzwakken en T‑cellen versterken
Aangezien het volledig elimineren van ZDHHC24 of B7H3 met genetica geen praktische behandeling voor patiënten is, ontwierpen de auteurs een kort, celdoorlaatbaar peptide dat zij het E‑peptide noemen. Het bootst een kleine reeks van het B7H3‑eiwit na die normaal aan ZDHHC24 bindt, en fungeert als lokaas dat voorkomt dat het enzym echte B7H3‑moleculen modificeert. In gekweekte cellen verminderde het E‑peptide B7H3‑palmitoylering en eiwitniveaus, herstelde de herkenning door de autophagie‑machinerie en maakte het menselijke CD8+ T‑cellen in staat tumorcellen efficiënter te doden. In meerdere muismodellen, waaronder een gehumaniseerd model met menselijke immuuncellen en menselijke colorectale tumoren, krimpten tumoren na injecties met E‑peptide, nam het aantal CD8+ T‑cellen in tumoren toe en steeg de productie van belangrijke doder‑moleculen zoals granzyme B en interferon‑gamma.
Een nieuwe partner voor bestaande immunotherapie
Tenslotte onderzochten de onderzoekers of deze strategie samen met standaard PD‑1‑blokkade zou kunnen werken. In muismodellen van colorectale kanker boden zowel E‑peptide alleen als anti‑PD‑1‑antilichaam alleen enige tumorgroei‑controle. Maar in combinatie produceerden de twee behandelingen veel sterkere en langer aanhoudende tumoronderdrukking, waarbij in sommige gevallen tumoren verdwenen en de gemiddelde overleving meer dan verdubbelde vergeleken met controles. Dit suggereert dat het uitschakelen van het B7H3‑schild door het verwijderen van zijn vet «anker» complementair kan zijn aan bestaande remmingsmiddelen die de PD‑1‑route targeten.
Wat dit betekent voor toekomstige kankerbehandelingen
Kort gezegd laat deze studie zien dat een veelvoorkomend voedingsvet, palmitinezuur, door colorectale tumoren kan worden gekaapt om een immuunremmend eiwit (B7H3) chemisch te bepantseren en zo de kanker te helpen verbergen. Door die ene chemische aanhechting te blokkeren, konden de auteurs de bepantsering verwijderen, het celinterne afbraaksysteem B7H3 laten opruimen en CD8+ T‑cellen weer toegang geven om aan te vallen. Hoewel het E‑peptide zelf een experimenteel hulpmiddel in een vroeg stadium is, identificeert het werk B7H3‑palmitoylering — en het enzym ZDHHC24 — als veelbelovende medicijndoelen. Als soortgelijke middelen veilig en effectief blijken bij mensen, zouden ze op termijn meer colorectale kankers kunnen veranderen van “koude” tumoren die immunotherapie negeren naar “hete” tumoren die het immuunsysteem kan herkennen en vernietigen.
Bronvermelding: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Trefwoorden: immunotherapie bij colorectale kanker, B7H3 remmingsmechanisme, palmitinezuurmetabolisme, eiwitpalmitoylering, CD8 T-cel tumorimmuniteit