Clear Sky Science · nl
Macrofagen van zebravissen zetten fysieke verwondingssignalen om in snelle vasculaire permeabiliteit
Hoe een klein visje ons leert over zwelling bij wonden
Wanneer je je knie schaafwond hebt, wordt het gebied snel rood, opgezet en lekt het vocht. Deze snelle verandering in nabijgelegen bloedvaten is cruciaal om infectie te bestrijden en het herstel op gang te brengen, maar precies hoe het lichaam schade waarneemt en binnen enkele seconden reageert, was moeilijk in realtime te volgen. Met behulp van doorschijnende zebravislarven en geavanceerde live-imaging onthult deze studie hoe gespecialiseerde immuuncellen die zich om bloedvaten heen bevinden de fysieke schok van een wond omzetten in vrijwel onmiddellijke lekkage van vaten, wat nieuw inzicht geeft in ontsteking, genezing en zelfs longschade bij mensen.
Waarnemen hoe letsel zich door het lichaam verspreidt
De onderzoekers werkten met jonge zebravissen, wier transparante lichamen wetenschappers in staat stelden cellen en bloedvaten in actie onder de microscoop te volgen. Ze kerfden de punt van de staartvin af en vulden de circulatie met een oplichtende kleurstof die binnen gezonde vaten blijft. Toen de gewonde vissen terug in gewoon zoet water werden geplaatst, veroorzaakte de plotselinge instroom van water in weefsels een “osmische schok” rond de wond. Binnen enkele minuten verwijden nabijgelegen vaten zich en begonnen ze de fluorescerende kleurstof in het omringende weefsel te laten lekken, wat het zwellen en sijpelen nabootst dat rond menselijke wonden optreedt. Door vissen te verplaatsen tussen gewoon en speciaal gebalanceerd zout- of suikervocht toonde het team aan dat deze snelle vasculaire permeabilisatie sterk afhankelijk is van osmotische veranderingen en niet alleen van het fysieke scheuren van weefsel.
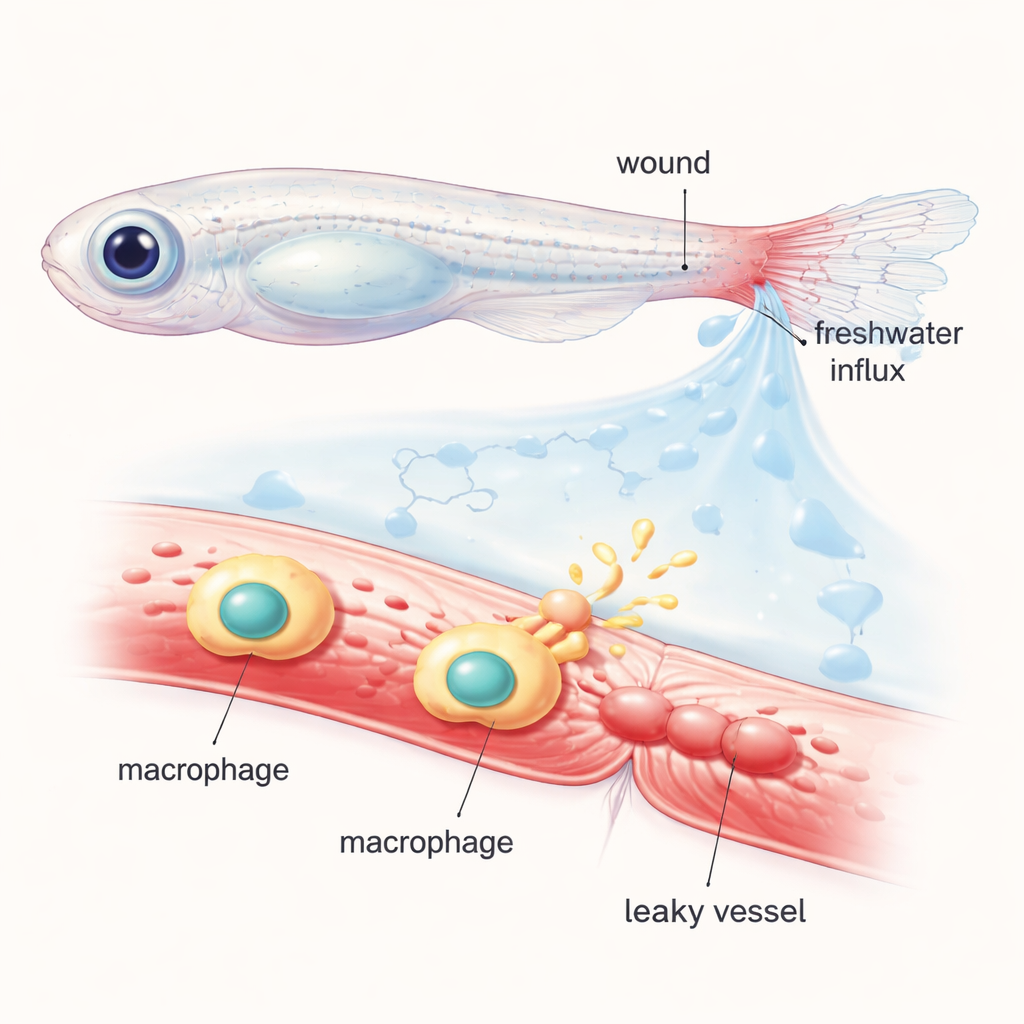
Het chemische boodschappers spoor achter de lekkage
Om te achterhalen welke moleculen de fysieke schok in een lek-signaal veranderen, onderzochten de wetenschappers een familie van vette verbindingen genaamd eicosanoïden, gemaakt uit arachidonzuur. Deze lipiden zijn bekend vanwege hun rol bij ontsteking en bloedstroom. Met genetische mutanten en geneesmiddelen schakelden ze selectief individuele enzymen in de eicosanoïde route uit. Het blokkeren van een sleutelenzym genaamd Alox5a (5-lipoxygenase) of zijn partner Lta4h verminderde sterk hoeveel kleurstof uit bloedvaten ontsnapte na de osmische schok, zonder de wondsluiting zelf te stoppen. Daarentegen had het verstoren van andere verwante enzymen weinig effect. Dit wees op een specifieke tak van de lipidenroute als de belangrijkste motor van de snelle lekkagerespons, die als een chemische klep lijkt te functioneren die op aanvraag geopend of gesloten kan worden.
De verrassende rol van vat-omhelzende immuuncellen
Bloed bevat verschillende typen immuuncellen, en bij zebravislarven zijn neutrofielen en macrofagen de belangrijkste spelers. Het team gebruikte een slimme genetische truc om selectief neutrofielen of macrofagen te vernietigen vóór het verwonden. Het wegnemen van neutrofielen maakte weinig verschil voor vaatlekkage. Maar wanneer macrofagen werden uitgeschakeld, halveerde de lekkagerespons ongeveer, wat het effect van het blokkeren van de Alox5a–Lta4h-lipidenroute weerspiegelt. Belangrijk is dat deze ingrepen de snelle wondsluiting niet stopten, wat laat zien dat leukocytenrecruitment en vaatlekkage enigszins onafhankelijk kunnen worden geregeld. Dit onthulde perivasculaire macrofagen—macrofagen die zich nauw langs de buitenkant van vaten bevinden—als sleutelvertalers tussen fysieke verwonding en vasculair gedrag.
Van kernverrekking naar chemisch signaal
Hoe detecteren deze perivasculaire macrofagen een wond die op enige afstand kan liggen? Het antwoord ligt in de manier waarop hun kernen reageren op mechanische stress. Wanneer de osmische schok van de wond zich door het omliggende weefsel verspreidt, veroorzaakt instroom van water subtiele celzwelling en vervorming van de kern. De onderzoekers tagden een mechanogevoelig enzym genaamd cPla2 met een fluorescerende marker en uitten het specifiek in macrofagen. Na verwonding in normaal zoet water verplaatste cPla2 zich snel naar het binnenoppervlak van het kernmembraan in macrofagen langs een golf die zich door het weefsel bewoog met ongeveer 50 micrometer per seconde, overeenkomend met de verspreiding van opgeloste zouten. Deze translocatie was afhankelijk van hypotonische omstandigheden en was veel zwakker in isotone oplossingen. Macrofagen dicht bij bloedvaten lieten bijzonder scherpe, omkeerbare pulsen van nucleair cPla2-binding zien, die op hun beurt arachidonzuur vrijmaken voor omzetting in de lekkage-inducerende lipiden.
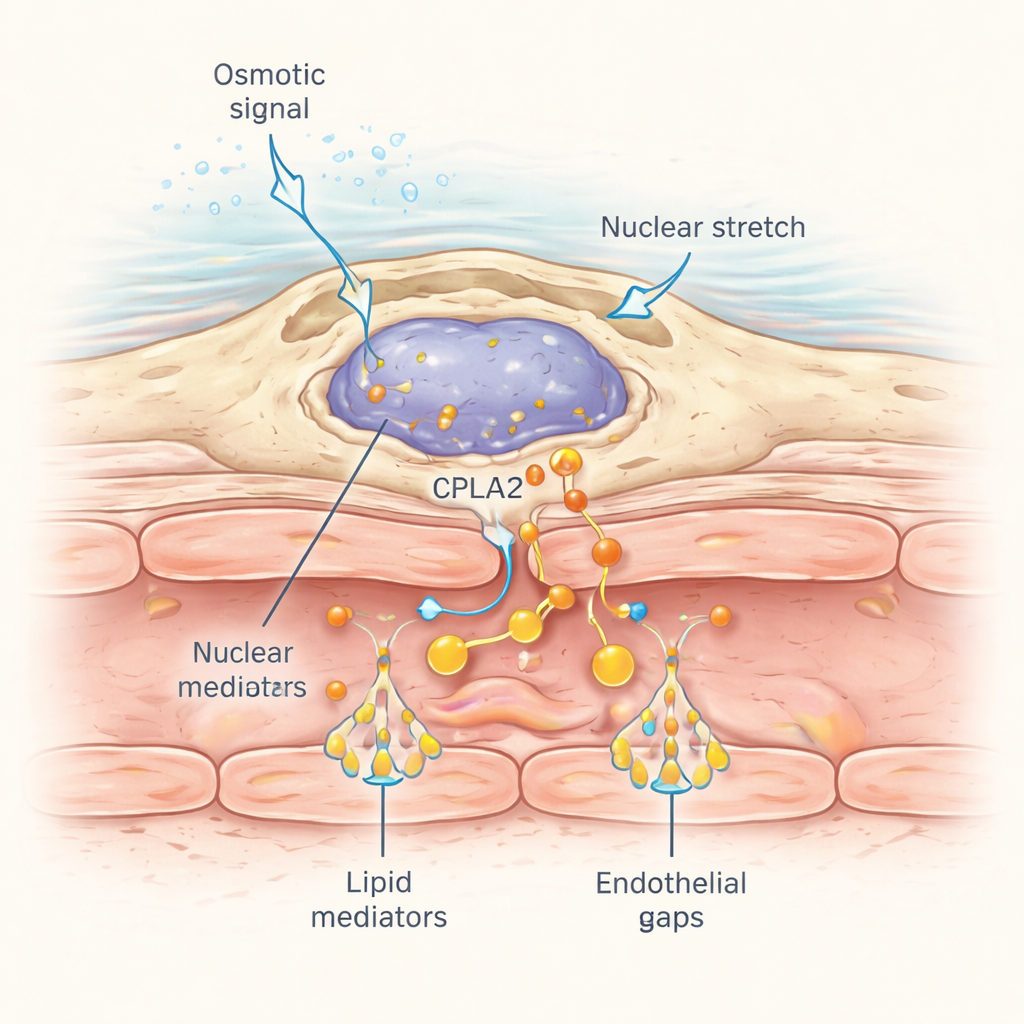
Waarom dit verder reikt dan vissen
Kort gezegd laat deze studie zien dat bepaalde macrofagen fungeren als fysieke wachtposten: ze voelen de rek van weefsel en kernmembranen veroorzaakt door osmotische veranderingen bij een wond, schakelen cPla2 aan op hun kernoppervlak en produceren snel lipideboodschappers die nabijgelegen bloedvaten vertellen de poorten te openen zodat vocht en immuunfactoren binnenstromen. Hoewel zebravissen in zoet water leven en unieke osmotische uitdagingen kennen, werken soortgelijke mechanogevoelige routes waarschijnlijk ook in menselijke weefsels die aan veranderende drukken en stromingen worden blootgesteld, bijvoorbeeld de longen tijdens mechanische ventilatie. Inzicht in hoe kernverrekking en lipidesignalen de vaatgeleidbaarheid in realtime aansturen, kan uiteindelijk behandeling informeren die ontsteking fijn afstemt—hetzij door schadelijke lekkage te dempen bij aandoeningen zoals acuut longletsel, hetzij door nuttige responsen te versterken om weefselherstel te versnellen.
Bronvermelding: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Trefwoorden: wondgenezing, bloedvaten, macrofagen, ontsteking, zebravis