Clear Sky Science · nl
Bionische Janus-hydrogel stimuleert regeneratie van geïnfecteerde achillespezen via mechano-immuun ruimtelijk-temporele sturing
Waarom dit belangrijk is voor beschadigde pezen
Gescheurde achillespezen komen vaak voor bij zowel sporters als oudere volwassenen, en wanneer bacteriën de wond infecteren, verloopt het genezen vaak slecht: de pees kan verzwakken, vastgroeien aan het omliggende weefsel of zelfs opnieuw inscheuren. Deze studie presenteert een nieuwe "slimme" hydrogelpleister, geïnspireerd op de natuurlijke schede van de pees, die tijdens een operatie op een geïnfecteerde pees kan worden aangebracht. Het doel is drie dingen tegelijk te doen: de pees mechanisch beschermen, medicijnresistente bacteriën doden en het immuunsysteem voorzichtig sturen van schadelijke ontsteking naar echte regeneratie.
Een tweezijdige pleister geïnspireerd door de natuur
Gezonde pezen liggen in een gladde schede die ze soepel laat glijden terwijl ze toch stevig verankerd blijven. Chirurgen hebben moeite dit na reparatie te evenaren: materialen die goed aan de pees hechten, blijven vaak ook aan het omliggende weefsel plakken, wat pijnlijke verklevingen veroorzaakt. De onderzoekers kopieerden dit natuurlijke ontwerp van "hechting plus smering" met een Janus (tweepotige) hydrogel genaamd HAPP@H-EXO. De ene zijde grijpt stevig het peesoppervlak vast met reversibele chemische bindingen en waterstofbruggen, wat solide mechanische ondersteuning geeft. De tegenoverliggende zijde is, met een lotusblaadje-achtige behandeling, waterafstotend en laag-frictie gemaakt zodat omliggend weefsel niet blijft plakken. Dit creëert een beschermende mouw die met de pees meebeweegt maar littekenvorming aan de omgeving tegengaat. 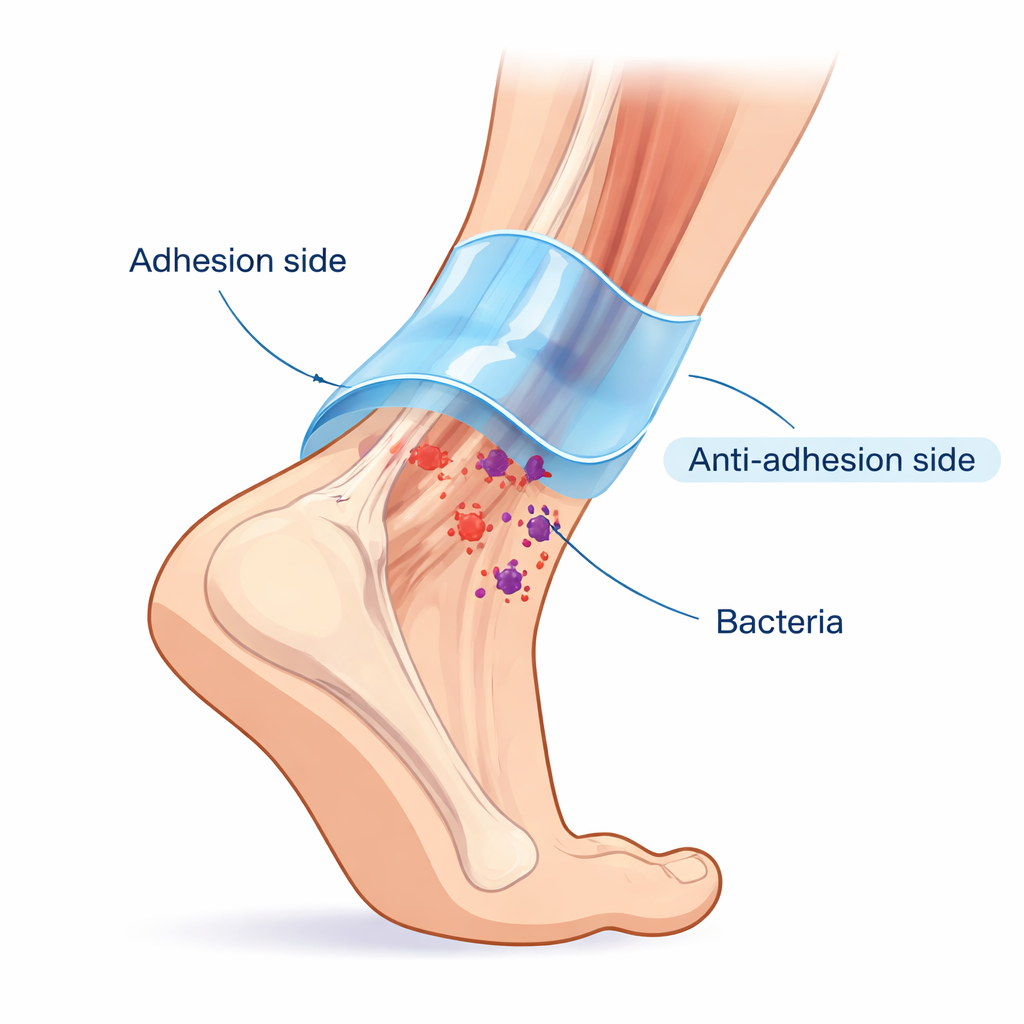
Ontworpen om de belasting te delen en herhaalde rek te doorstaan
In tegenstelling tot veel zachte gels is dit materiaal bedoeld voor een harde mechanische omgeving: iedere stap belast en ontlast de achillespees. Het team combineerde een stijf, permanent gekruislinkt netwerk met een tweede, dynamisch netwerk dat zich onder stress kan herschikken. Tests toonden aan dat de hydrogel kan rekken en comprimeren zonder te scheuren, zijn sterkte behoudt gedurende minstens 100 belastingscycli en weinig energie dissipeert, wat betekent dat hij terugveert in plaats van langzaam te vervormen. Computersimulaties wezen uit dat, wanneer rond een gehechte pees gewikkeld, de gel de hoge spanningen van de hechtingspunten naar de peesranden verspreidt, waardoor de kans op een nieuwe scheur bij de reparatieplaats afneemt. In proefdieren vertaalt dit zich naar gerepareerde pezen met sterkte en stijfheid die de normale weefselwaarden benaderen.
Bacteriën vangen en resistentie weerstaan
Bacteriële infectie is een belangrijke reden waarom peesreparaties mislukken, vooral bij multiresistente stammen zoals MRSA. In plaats van te vertrouwen op traditionele antibiotica vangt en doodt de hydrogel bacteriën fysiek. Een component, een fenylboronzuurgroep, herkent suikerrijke structuren op bacteriële celwanden en vormt reversibele bindingen met deze structuren, waardoor bacteriën uit de omgevende vloeistof worden gehaald. Een andere component, een positief geladen polymeer, destabiliseert vervolgens bacteriële membranen, waardoor ze scheuren. In laboratoriumtests doodde de gel snel MRSA, veelvoorkomende Staphylococcus- en E. coli-stammen, breekte taaie biofilms af en behield zijn antibacteriële kracht over dagen en meerdere gebruikscycli zonder bacteriële resistentie tegen de vang- of doodmechanismen te veroorzaken. 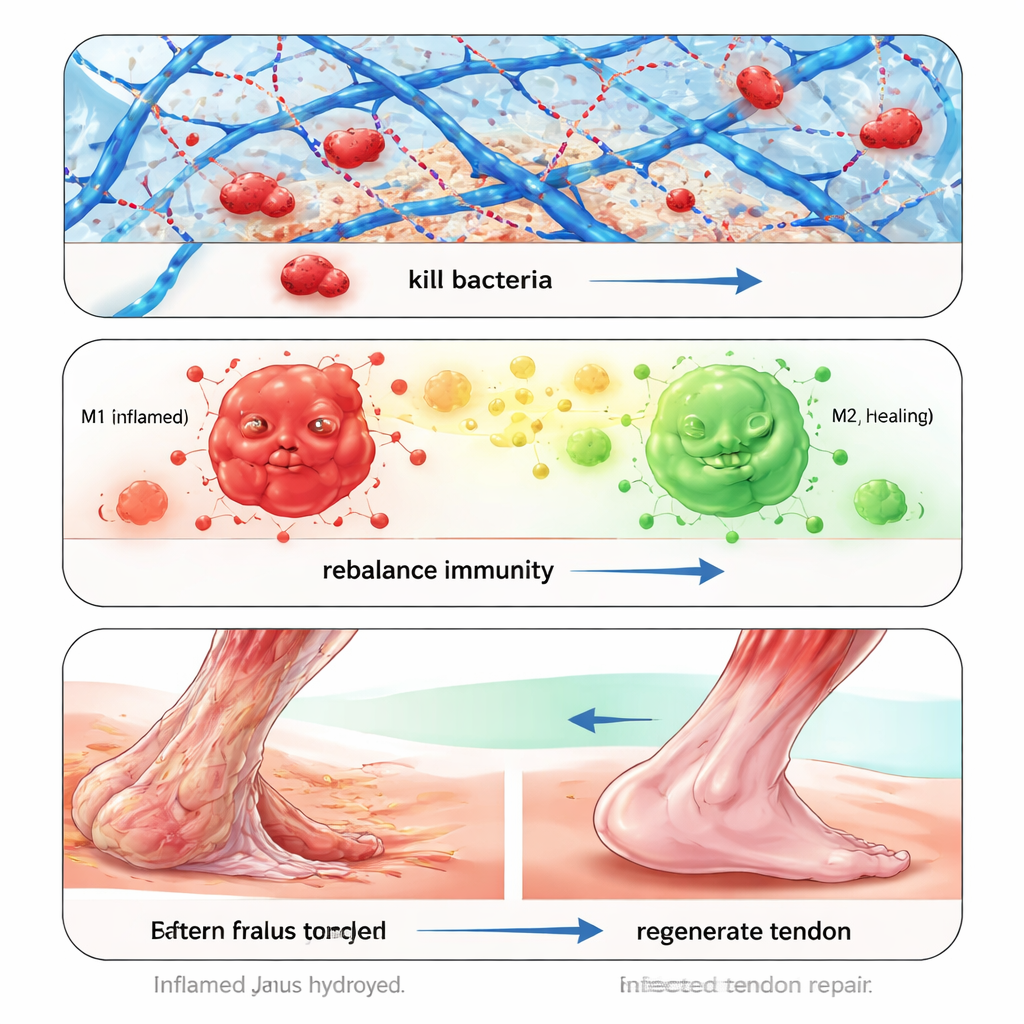
Het immuunsysteem sturen en weefsel herbouwen
Zelfs als bacteriën zijn verwijderd, blijven geïnfecteerde pezen vaak in een staat van oxidatieve stress en chronische ontsteking, wat normaal herstel blokkeert. Om dit aan te pakken, beladen de onderzoekers de hydrogel met kleine membraanzakjes—exosomen—afgescheiden door pees-stamcellen gekweekt onder lage zuurstofomstandigheden. Deze "hypoxische" exosomen zitten vol met anti-inflammatoire en pro-regeneratieve signalen. De chemie van de gel zorgt ervoor dat exosomen sneller vrijkomen in de zure, ontstoken vroege fase en langzamer naarmate de omstandigheden normaliseren. In celexperimenten verminderden exosoom-beladen gels schadelijke reactieve zuurstofsoorten, herstelden ze de mitochondriale functie, stimuleerden ze bloedvatvorming en duwden ze immuuncellen weg van een ontstekingsbevorderende toestand (M1) naar een herstellende toestand (M2). Genanalyse wees op demping van de NF-κB-route, een centrale aanjager van ontsteking.
Van geïnfecteerde ruptuur naar functioneel herstel
In rat- en konijnmodellen van achillesruptuur die opzettelijk met MRSA waren geïnfecteerd, elimineerde het aanbrengen van de Janus-hydrogel tijdens de operatie bijna alle levende bacteriën op de wondplaats binnen een week. In de daaropvolgende weken toonden behandelde pezen minder oxidatieve schade, minder ontstekingsmarkers en meer pro-herstelsignalen dan onbehandelde controles. Microscopie liet beter uitgelijnde, dikkere collageenvezels zien, meer bloedvaten en expressie van sleutelproteïnen die bij peesrijping horen. Belangrijk is dat de buitenzijde van de gel, die niet plakt, verhinderde dat de pees aan omliggend weefsel vastgroeide, bevestigd door beeldvorming en macroscopen onderzoek. Dieren die behandeld werden met de exosoom-beladen versie herwonnen meer normale gangpatronen en een hogere draagkracht van de pees, wat wijst op niet alleen structurele reparatie maar ook functioneel herstel.
Wat dit voor patiënten kan betekenen
Dit werk toont één biomimetisch materiaal dat mechanische ondersteuning, infectiebestrijding en immuunevenwicht geïntegreerd aanpakt. Door een tweezijdig fysiek ontwerp te combineren met bacterievangende chemie en getimede afgifte van regeneratieve exosomen, hielp de Janus-hydrogel geïnfecteerde achillespezen bij dieren sterker genezen, met minder littekens en betere mobiliteit. Hoewel menselijke proeven nog nodig zijn, suggereert de aanpak een toekomst waarin complexe weke-delenletsels, vooral die complicaties door medicijnresistente infecties hebben, behandeld kunnen worden met "slimme" chirurgische verbanden die actief het genezingsproces orkestreren.
Bronvermelding: Li, J., Wang, Z., Yang, W. et al. Bionic Janus hydrogel drives infected Achilles tendon regeneration via mechano-immune spatiotemporal steering. Nat Commun 17, 1805 (2026). https://doi.org/10.1038/s41467-026-68514-0
Trefwoorden: Herstel van achillespees, hydrogel pleister, antibioticaresistente infectie, weefselregeneratie, immuunmodulatie