Clear Sky Science · nl
Mechanische krachten door intercellulaire peptide‑zelfassemblage drijven de vorming van spheroïden
Het bouwen van kleine weefsels in het lab
Wetenschappers haasten zich om miniatuurversies van menselijke weefsels te maken die zich voordoen als het echte werk. Deze levende modellen kunnen het testen van kankertherapieën veiliger maken en nieuwe behandelingen voor diabetes en andere ziektes dichterbij brengen. Deze studie introduceert een slimme manier om cellen ertoe te brengen realistische driedimensionale clusters te vormen, compleet met hun eigen primitieve “bloedvat‑achtige” netwerken die de toevoer van voedingsstoffen en de functie verbeteren.
Cellen helpen hun omgeving te voelen
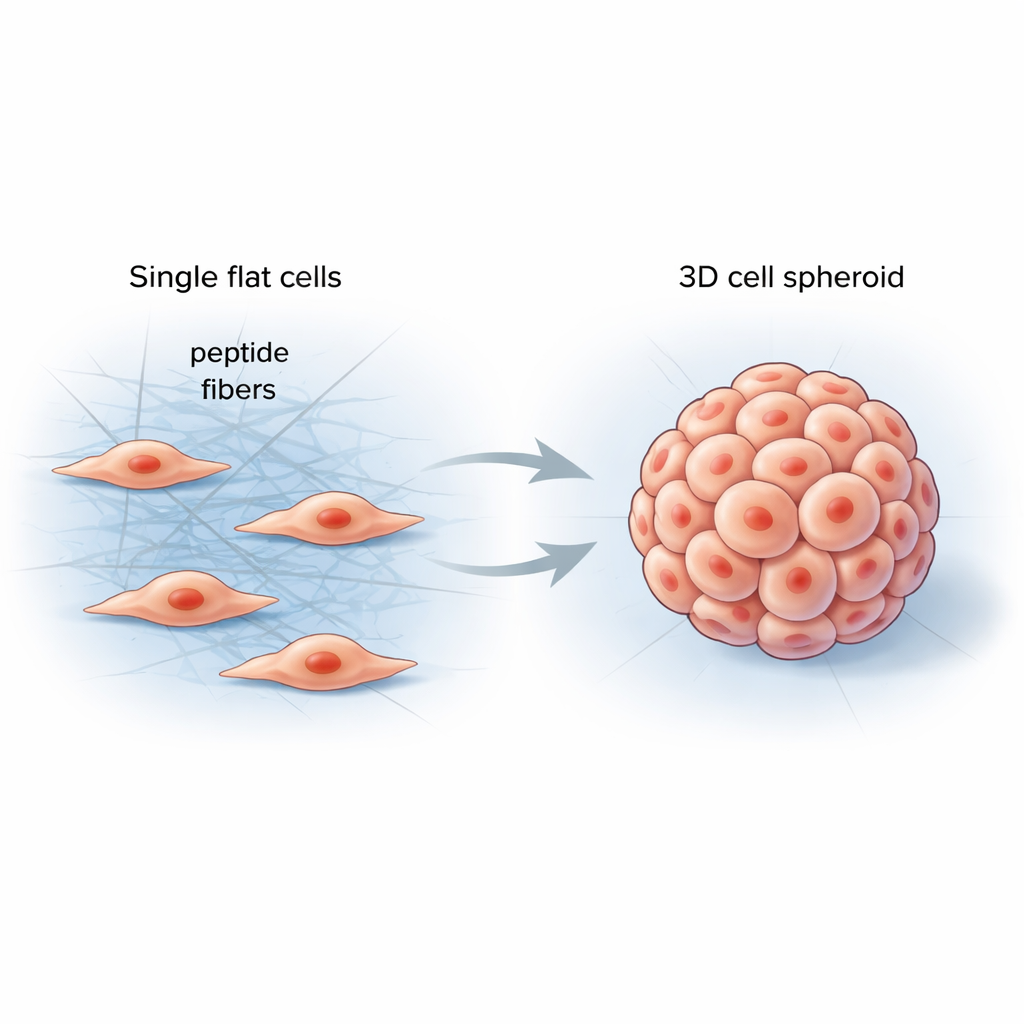
In ons lichaam leven cellen in een zachte maar gestructureerde omgeving die de extracellulaire matrix wordt genoemd — een netwerk van eiwitten dat weefsels ondersteunt en voortdurend mechanische signalen naar cellen stuurt. Conventionele laboratoriummaterialen slagen er vaak niet in deze complexiteit na te bootsen en produceren meestal platte cellagen die zich heel anders gedragen dan echte organen of tumoren. De onderzoekers wilden een eenvoudig, programmeerbaar materiaal ontwerpen dat zich direct tussen cellen vormt, hun omgeving gecontroleerd verhardt en hen aanzet tot natuurlijkere driedimensionale vormen.
Slimme peptiden die zich tussen cellen assembleren
Het team maakte korte eiwitfragmenten, peptiden genoemd, die aan elkaar kunnen koppelen tot lange, dunne vezels wanneer ze specifieke enzymen op celmembranen tegenkomen. Toen deze peptiden aan kankercellen werden toegevoegd, waren ze aanvankelijk inactief, als een heldere oplossing. Zodra de cellen hun eigen enzymen een deel van het molecuul afknipten, assembleerden de peptiden snel tot een fibrillair netwerk dat zich om en tussen naburige cellen wikkelde. Dit nieuwe vezelnetwerk veranderde de lokale mechanische krachten, waardoor cellen aan elkaar trokken, hun interne steigerwerk herkenden en zich verzamelden tot ronde 3D‑spheroïden in plaats van uit te spreiden in een laag.
Van celclust ers naar vat‑achtige netwerken
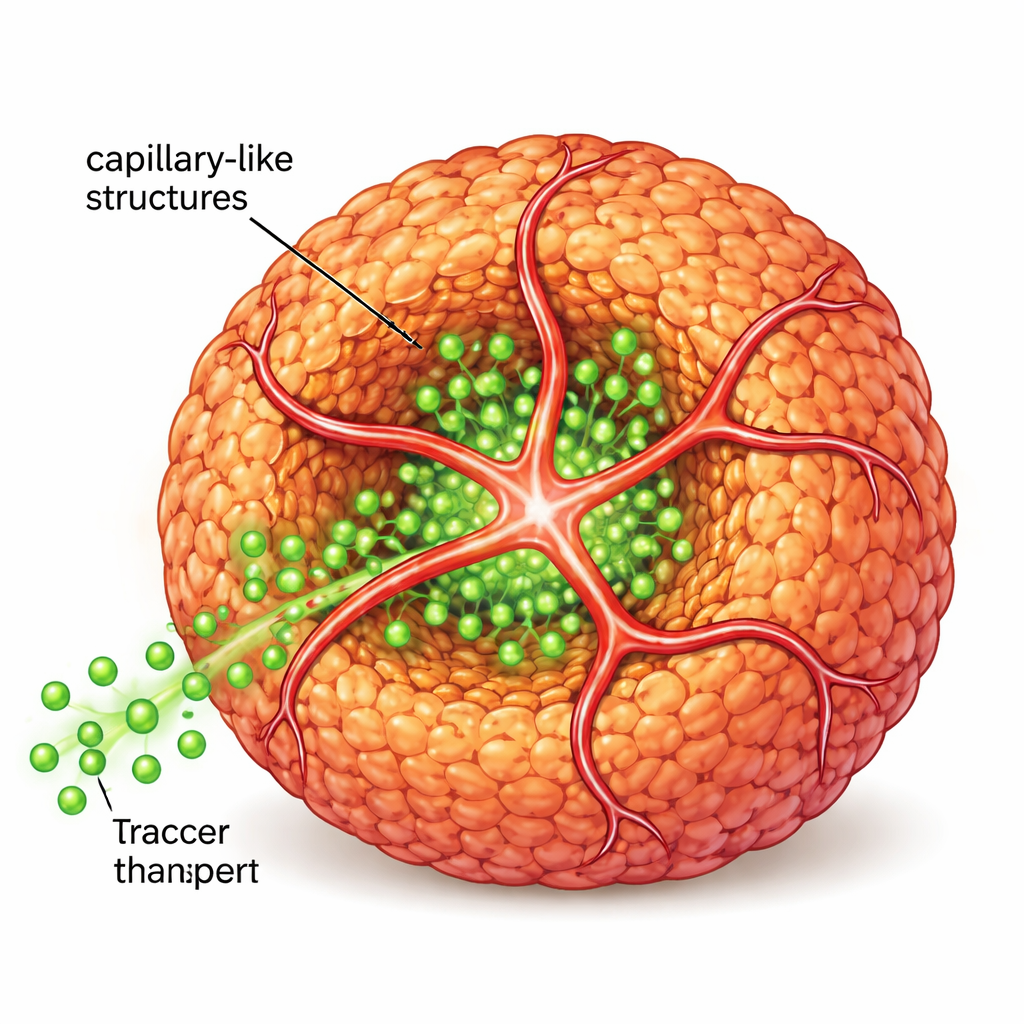
Om dichter bij echt weefsel te komen, introduceerden de wetenschappers vervolgens menselijke endotheelcellen — het type cellen dat normaal bloedvaten bekleedt — samen met een tweede peptide dat een klein “adreslabel” droeg dat deze cellen aantrok. Samen vormden de oorspronkelijke en de gemodificeerde peptiden een gedeeld nanovezel‑skelet. Endotheelcellen gebruikten dit skelet om uit te groeien tot buisachtige uitlopers die de spheroïden omwikkelden en binnendrongen, waardoor capillair‑achtige structuren ontstonden. Toen het team fluorescerende suikerachtige moleculen langs deze structuren liet stromen, zagen ze veel diepere penetratie in de kern van het spheroïde vergeleken met spheroïden zonder deze interne buisjes, wat aantoont dat het transport van voedingsstoffen en signalen aanzienlijk verbeterde.
Dichter bij echte tumoren en functionele eilandjes
Genactiviteitsprofilering toonde aan dat tumorspheroïden met capillair‑achtige structuren meer leken op patiëntstalen van glioblastoom dan traditionele platte culturen of niet‑gevasculariseerde spheroïden. Bij muizen groeiden spheroïden met deze primitieve vaatschakelingen uit tot grotere, meer gevasculariseerde tumoren, wat aangeeft dat het in vitro‑model belangrijke kenmerken van echt tumorgedrag vastlegt. Dezelfde strategie werd toegepast op pancreatische bètacellen, die normaal in sterk gevasculariseerde eilandjes leven en insuline afgeven als reactie op glucose. Wanneer bètacel‑spheroïden werden uitgerust met capillair‑achtige structuren met behulp van het peptide‑systeem en endotheelcellen, toonden ze veel sterkere en fijnmaziger gestuurde insulineafgifte, wat wijst op een krachtig hulpmiddel voor diabetesonderzoek en regeneratieve geneeskunde.
Waarom dit belangrijk is voor toekomstige therapieën
Door eenvoudige peptiden zichzelf tussen levende cellen te laten assembleren, biedt dit werk een algemeen recept voor het bouwen van miniatuur, gevasculariseerde weefsels die meer aanvoelen en functioneren als die in het lichaam. De resulterende spheroïden weerspiegelen patiënttumoren en werkende eilandjes beter, waardoor ze waardevol zijn voor geneesmiddeltests, het bestuderen van ziektemechanismen en het ontwerpen van nieuwe celgebaseerde therapieën. Voor niet‑specialisten is de belangrijkste conclusie dat het geven van het ‘juiste gevoel’ aan in het lab gekweekte cellen en het toevoegen van kleine vat‑achtige netwerken hun vermogen om menselijke weefsels trouw na te bootsen drastisch kan verbeteren, en daarmee het pad van fundamenteel onderzoek naar effectieve behandelingen kan versnellen.
Bronvermelding: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Trefwoorden: weefseltechniek, kankermodellen, angiogenese, organoïden, peptide zelfassemblage