Clear Sky Science · nl
Intermitterend vasten remt Tp53-gedreven gliomen via door het darmmicrobioom gemedieerde methionine-m6A-regulatie
Waarom de darmen even rust gunnen dodelijke hersentumoren kan vertragen
Glioblastoom is een van de meest agressieve hersenkankers, en de huidige behandelingen—operatie, bestraling en chemotherapie—verlengen het leven van patiënten vaak maar beperkt. Deze studie stelt een eenvoudige maar krachtige vraag met grote implicaties voor het dagelijks leven: kan de manier waarop we eten, specifiek intermitterend vasten, onze darmbacteriën en de bloedchemie zodanig veranderen dat bepaalde hersentumoren significant worden vertraagd?
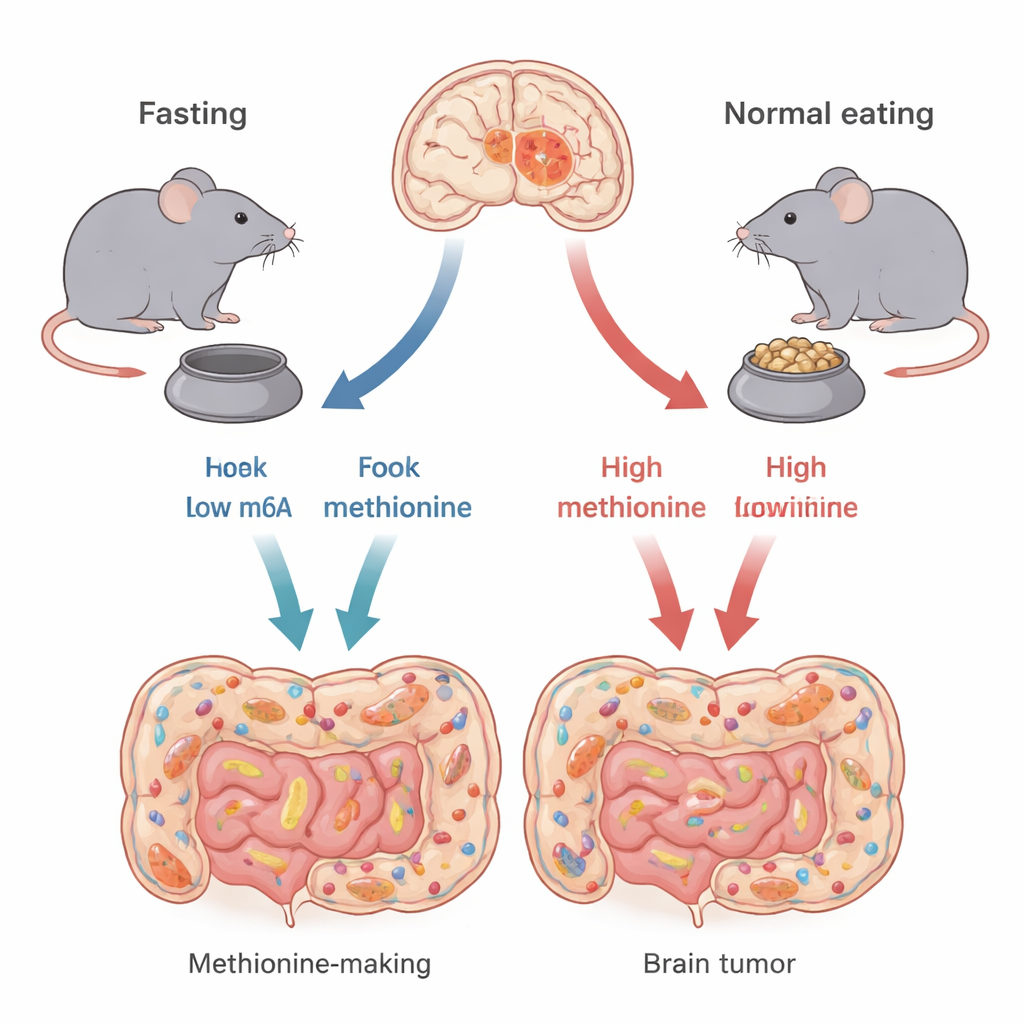
Verschillende varianten van dezelfde hersenkanker
Niet alle glioblastomen zijn hetzelfde. De auteurs richten zich op twee belangrijke genetische typen, gedefinieerd door veranderingen in genen genoemd TP53 en CDKN2A. Deze genen helpen te regelen hoe cellen groeien of afsterven. Met behulp van muismodellen die elk menselijk subtype nauw nabootsen, laten de onderzoekers zien dat intermitterend vasten—24 uur zonder voedsel gevolgd door 24 uur met voedsel—niet alle hersentumoren evenveel helpt. Muizen met TP53-type tumoren leefden langer en hadden kleinere tumoren wanneer ze vastten, terwijl muizen met CDKN2A-type tumoren weinig voordeel toonden. Dit suggereert dat de effectiviteit van vasten sterk kan afhangen van de genetische samenstelling van de tumor.
Van eetpatroon naar darmbacteriën naar hersenchemie
Het team onderzocht vervolgens hoe vasten dit selectieve effect teweegbrengt. Omdat de totale hoeveelheid voedsel tussen de groepen gelijk bleef, was het belangrijkste verschil de timing van het eten. Die timing hervormde krachtig het darmmicrobioom—de uitgestrekte gemeenschap van bacteriën in de darm. Bij vastende TP53-muizen namen bepaalde bacteriegroepen die methionine efficiënt produceren, zoals specifieke Alistipes- en Prevotella-stammen, in aantal af. Omdat methionine een essentieel aminozuur is dat dieren via dieet of darmmicroben moeten verkrijgen, betekende deze microbiele verschuiving minder methionine dat vanuit de darm in de bloedbaan en uiteindelijk in de hersenen terechtkwam.
Hoe één voedingsstof kankersignalen kan bijsturen
Methionine is niet alleen een voedingsstof; het is ook grondstof voor S-adenosylmethionine (SAM), de universele methylgroepdonor van de cel. SAM voedt een chemische etikettering van RNA die m6A wordt genoemd. Deze etiketten helpen bepalen hoe sterk bepaalde genen tot expressie komen. In het TP53-tumormodel verlaagde vasten methionine- en SAM-niveaus in bloed en in hersentumorgebieden. Met meerdere lagen ‘omics’-technologieën—standaard RNA-sequencing, single-cell RNA-profilering, en ruimtelijke kaarten van zowel genactiviteit als metabolieten—vonden de onderzoekers minder m6A-etiketten op sleutel-RNA’s die met kanker verbonden zijn onder vasten. Een belangrijk doelwit was TGFB2, een gen in de TGF‑β-signaleringsroute, dat bekendstaat om het stimuleren van tumorgroei en invasie. Bij vasten werden zowel het enzym METTL3 (dat m6A-markeringen schrijft) als TGFB2 naar beneden bijgesteld, en verzwakte de TGF‑β-signalisatie.
Oorzaak en gevolg aantonen met gerichte interventies
Om verder te gaan dan correlatie, voerden de wetenschappers “rescue”-experimenten uit. Ze blokkeerden METTL3 met een geneesmiddel, of overdroegen darmbacteriën van vastende muizen naar normaal gevoede muizen, en zagen dat tumorgroei vertraagde zelfs zonder vasten—wat ondersteunt dat zowel het microbioom als de m6A-machinerie sleutelspelers zijn. Omgekeerd, wanneer vastende muizen extra methionine kregen of werden behandeld met een stof die m6A-markeringen verhoogt, groeiden hun tumoren meer als die van normaal gevoede muizen en verdween het overlevingsvoordeel. Belangrijk is dat het verstoren van darmbacteriën met breedwerkende antibiotica veel van de vasten-gerelateerde veranderingen deed verdwijnen, wat onderstreept dat de darmgemeenschap een centraal knooppunt is in deze keten van gebeurtenissen.
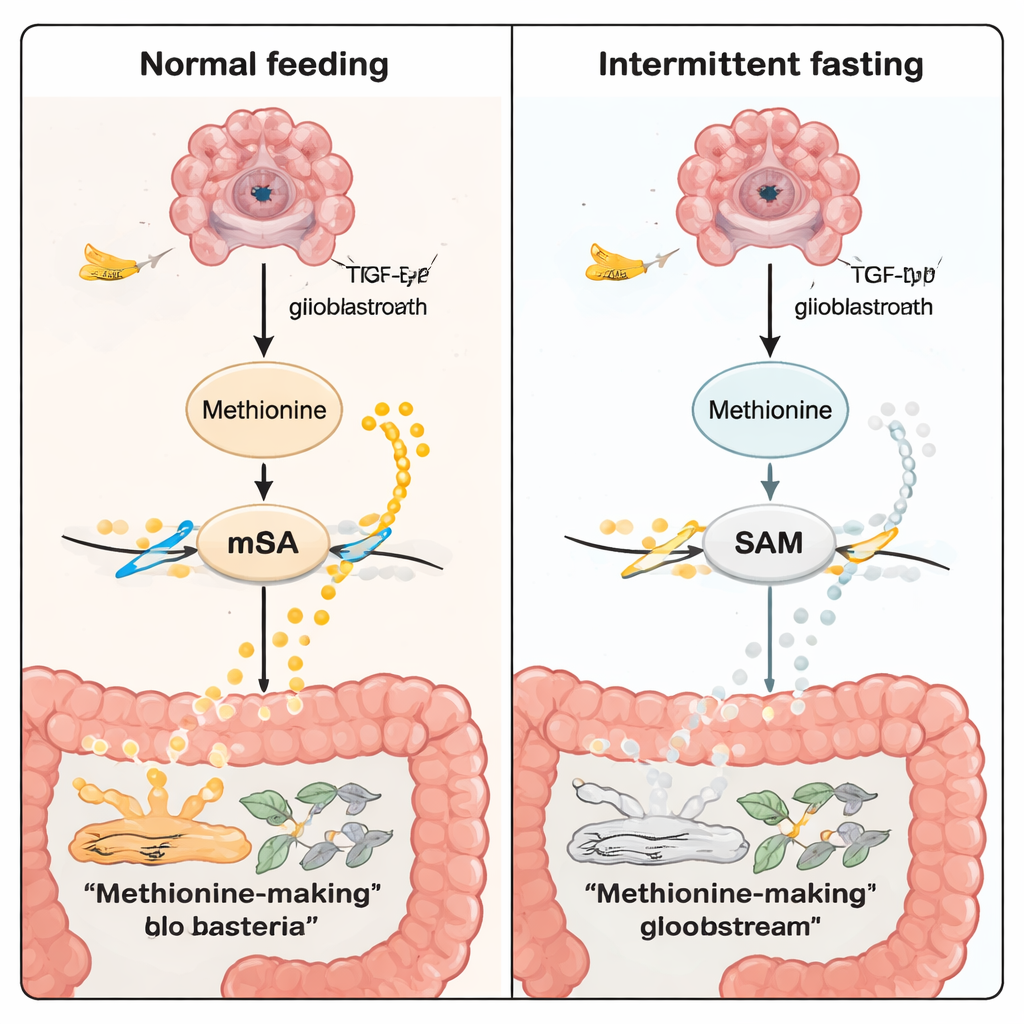
Wat dit betekent voor mensen en toekomstige therapieën
Voor de niet-specialist is de kernboodschap dat niet alle kankers, en zelfs niet alle glioblastomen, op dezelfde manier zullen reageren op een voedingsstrategie zoals intermitterend vasten. Bij TP53-type gliomen lijkt vasten via de darm met de hersenen te communiceren: het herstructureert de darmbacteriën, wat op zijn beurt de methionineproductie verlaagt, RNA-chemische etikettering vermindert en krachtige groeisignalen in tumorcellen dempt. Hoewel dit werk in muizen is uitgevoerd en zorgvuldige klinische vertaling vereist, wijst het op een toekomst waarin eenvoudige leefstijlpatronen, behandelingen op basis van het darmmicrobioom en geneesmiddelen die methionine- of m6A-paden targeten, op maat kunnen worden gemaakt voor het genetische subtype van iemands tumor.
Bronvermelding: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Trefwoorden: intermitterend vasten, glioblastoom, darmmicrobioom, methioninemetabolisme, RNA m6A-modificatie