Clear Sky Science · nl
TET1 als hoofdregelaar die GPX4-afhankelijke en -onafhankelijke ferroptosebewaking aanstuurt bij acute myeloïde leukemie
Waarom dit onderzoek belangrijk is voor kankerbehandeling
Veel nieuwe kankertherapieën proberen kwaadaardige cellen in een zelfdestructiemodus te dwingen die ferroptose heet, een vorm van celdood aangedreven door ijzer en lipidedoorslag. Toch blijven sommige tumoren hardnekkig weerstand bieden. Deze studie onthult hoe een DNA-modificerend eiwit, TET1, leukemiecellen helpt ferroptose te ontwijken via twee afzonderlijke biochemische verdedigingssystemen — en toont aan dat het blokkeren van deze verdedigingslinies zelfs resistente kankers kwetsbaar kan maken.
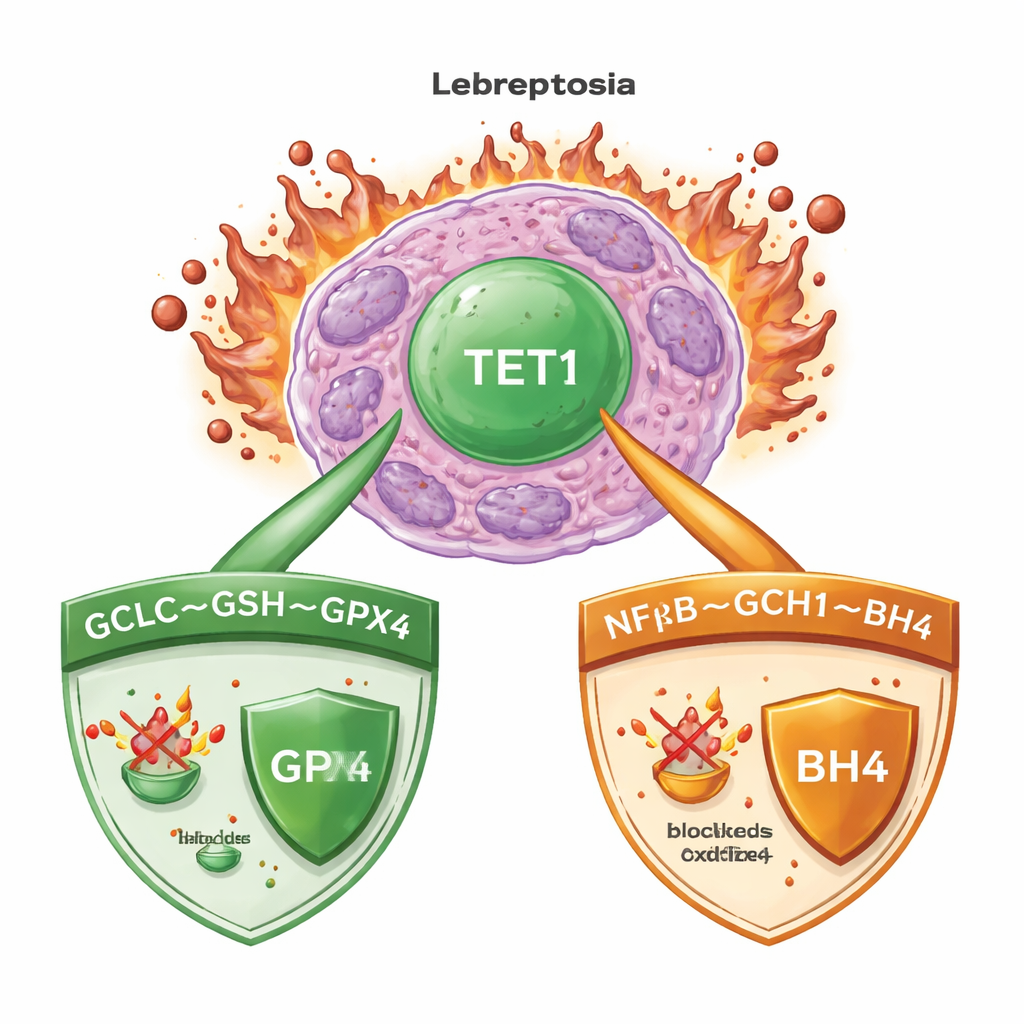
Een dodelijke mix van ijzer en beschadigde vetten
Ferroptose treedt op wanneer ijzer de ongecontroleerde oxidatie van vetten in celmembranen aanjaagt, wat uiteindelijk leidt tot het scheuren van cellen. Bij acute myeloïde leukemie (AML), zoals bij veel kankers, zetten cellen krachtige bewakingssystemen in om dit proces onder controle te houden. Een belangrijke beschermer is het enzym GPX4, dat met behulp van een klein molecuul, glutathion, schadelijke lipideperoxiden neutraliseert. Andere back-upsystemen maken antioxidanten die gevaarlijke radicalen kunnen vangen, zelfs wanneer GPX4 verstoord is. Begrijpen welke schakelaars deze verdedigingen coördineren is cruciaal voor het ontwerpen van therapieën die ferroptose betrouwbaar in kankercellen induceren zonder gezond weefsel te beschadigen.
TET1 verschijnt als een centraal regelpunt
De onderzoekers vergeleken tientallen kankercelmonsters, waaronder veel AML-lijnen en patiëntafgeleide cellen, en zagen een duidelijk patroon: cellen die weerstand boden tegen ferroptose hadden hogere niveaus van TET1, een enzym dat chemische DNA-markeringen wijzigt en genactiviteit beïnvloedt. Wanneer ze TET1-niveaus verlaagden met genetische middelen of de activiteit remden met een klein molecuul, werden kankercellen opvallend gevoeliger voor ferroptose-inducerende middelen. Dit gold zowel in kweek als in muismodellen van AML. Omgekeerd beschermde verhoogde TET1-expressie cellen tegen ferroptotische dood en beperkte de ophoping van reactieve zuurstofsoorten, de chemisch agressieve bijproducten die membraanschade aansturen.
Versterking van het primaire antioxidant schild
Dieper graven liet zien waar TET1 op het genoom werkt en toonde aan dat het rechtstreeks een gen genaamd GCLC activeert. GCLC codeert voor een cruciaal enzym dat de productie van glutathion op gang brengt, de brandstof voor GPX4. Door een specifieke DNA-markering (5-hydroxymethylcytosine) aan het GCLC-promotorgebied te verhogen, zet TET1 de glutathionsynthese krachtiger aan. Onder normale voedingsomstandigheden vergroot dit de centrale antioxidantvoorraad van de cel. Bij cystine-tekort maakt hetzelfde enzymcomplex ook ongebruikelijke γ-glutamyl-peptiden die helpen overtollig glutamaat weg te vangen — een andere manier om ferroptose te temperen. Zowel in gecultiveerde cellen als in muizen leidde verlies van TET1 of farmacologische remming van glutathionsynthese tot een sterke verlaging van glutathionniveaus en deze beschermende peptiden, waardoor leukemiecellen veel kwetsbaarder werden voor ferroptose-uitlokkers.
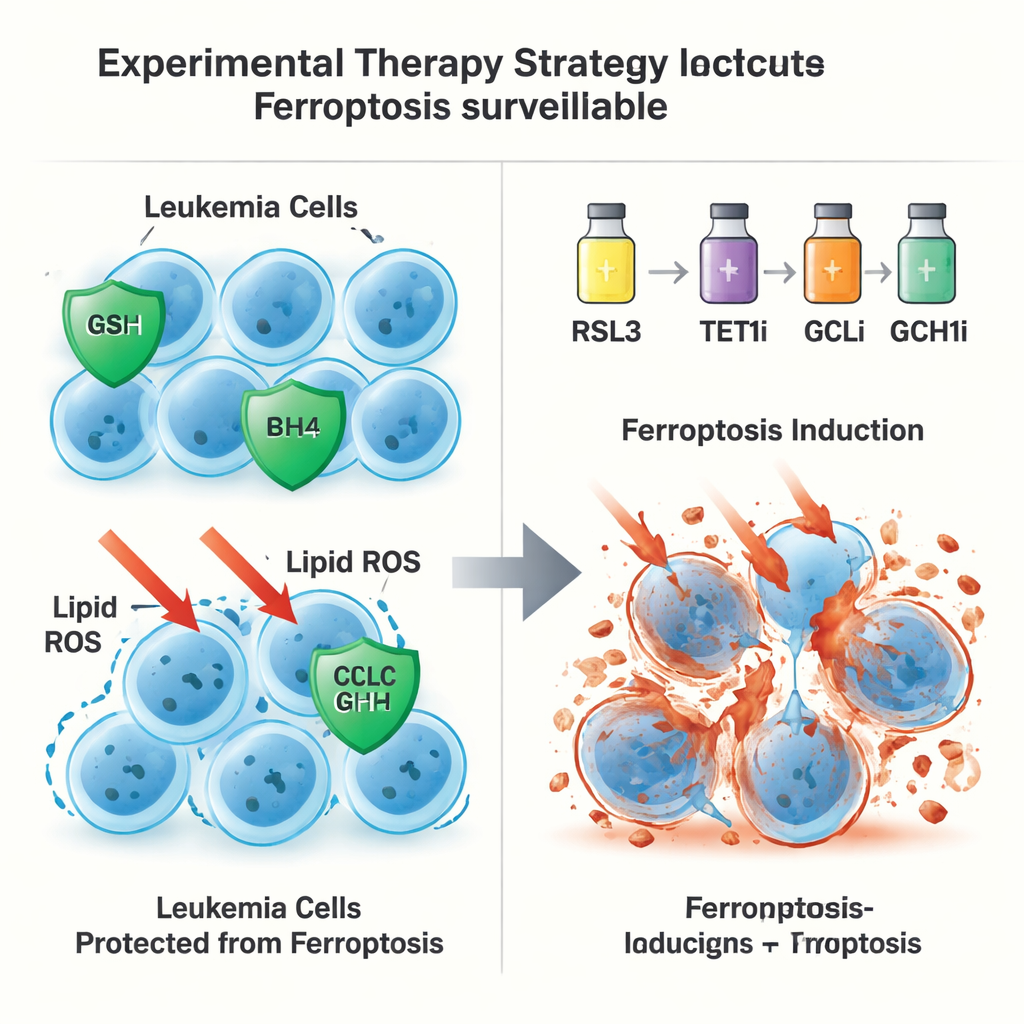
Een tweede, GPX4-onafhankelijke ontsnappingsroute
Verassend genoeg eindigt TET1’s beschermende rol niet bij de glutathion–GPX4-as. Zelfs wanneer GPX4 zelf uit leukemiecellen werd verwijderd, kon extra TET1 nog steeds ferroptotische celdood voorkomen, wat duidde op een tweede verdedigingslijn. De auteurs volgden dit terug naar TET1’s activatie van de NFκB-signaleringsroute, in het bijzonder een component genaamd NFKB2. Dit verhoogt op zijn beurt de expressie van GCH1, een enzym dat het antioxidantmolecuul BH4 produceert. BH4 kan membraanlipiden beschermen tegen oxidatie zonder afhankelijk te zijn van GPX4. Toen GCH1 genetisch werd stilgelegd of chemisch geblokkeerd, verdween het vermogen van TET1 om cellen tegen ferroptose te beschermen deels. Samen definiëren deze bevindingen een TET1–NFKB2–GCH1-route die een GPX4-onafhankelijk ferroptosebewakingssysteem vormt.
Een zwakte veranderen in een therapeutische kans
Gewapend met dit kaartenboek van twee paden testten de onderzoekers of het gelijktijdig stimuleren van ferroptose en verzwakken van TET1-gecontroleerde verdedigingen een therapeutisch voordeel kon opleveren. In muismodellen van AML en patiënt-afgeleide leukemiegrafts in muizen verminderden lage doses van een ferroptose-inducerend middel, gecombineerd met remmers van TET1, GSH-synthese (via GCLC) of GCH1, dramatisch de leukemielast, verlengden de overleving en leidden tot uitputting van leukemie-initiatiecellen. Belangrijk is dat de ferroptose-inducer in fracties van de doses werd gebruikt die in eerdere studies zijn gerapporteerd, waardoor zorgen over toxiciteit voor normale bloedstamcellen afnamen.
Wat dit betekent voor toekomstige kankertherapieën
Voor niet-specialisten is de kernboodschap dat leukemiecellen overleven door twee overlappende antioxidant ‘schilden’ te handhaven, beide gecoördineerd door TET1: één rond glutathion en GPX4, en een andere gebaseerd op GCH1 en BH4. Dit werk toont aan dat door ferroptose bescheiden te activeren terwijl men tegelijkertijd TET1 en zijn downstream partners blokkeert, artsen mogelijk resistentie kunnen overwinnen en selectief kankercellen over de rand kunnen duwen zonder gezond weefsel te overbelasten. Hoewel deze strategieën nog niet klaar zijn voor de kliniek, identificeert de studie TET1 als een krachtig regelknooppunt en een veelbelovend doelwit voor combinatietherapieën bij AML en mogelijk andere moeilijk behandelbare kankers.
Bronvermelding: Yang, L., Lu, J., Yun, W. et al. TET1 as a master regulator controlling GPX4-dependent and -independent ferroptosis surveillance in acute myeloid leukemia. Nat Commun 17, 1800 (2026). https://doi.org/10.1038/s41467-026-68509-x
Trefwoorden: ferroptose, acute myeloïde leukemie, TET1, glutathion, kanker epigenetica