Clear Sky Science · nl
Gelijktijdige sulfide-oxidatie en sulfaatreductie voor intracellulaire redox-homeostase onder zeer zure omstandigheden
Waarom het reinigen van giftige gassen slimme microben vereist
Veel industrieën lozen waterstofsulfide, een giftig gas met de geur van rotte eieren dat apparatuur kan aantasten, de lucht kan vervuilen en werknemers kan schaden. Ingenieurs vertrouwen steeds vaker op microben die sulfide omzetten in veiligere vormen van zwavel. Dit artikel onthult een onverwachte microbiële strategie: een nieuw geïdentificeerde Mycobacterium die twee normaal gesproken tegengestelde chemische routes gelijktijdig uitvoert om sulfide snel te detoxificeren en zich tegelijk te beschermen tegen interne schade, zelfs onder extreem zure omstandigheden.
Een touwtrekken in de zwavelcyclus
In de natuur wordt de zwavelcyclus aangedreven door twee tegengestelde reacties. Sommige microben oxideren sulfide (de meest gereduceerde, toxische vorm) naar minder schadelijke producten zoals elementair zwavel of sulfaat en winnen daardoor energie. Andere organismen gaan de omgekeerde weg en reduceren sulfaat terug naar sulfide om essentiële celcomponenten te bouwen, zoals zwavelhoudende aminozuren. Omdat deze reacties elkaar ongedaan maken, nam men lang aan dat een enkele cel beide processen niet tegelijk zou uitvoeren; dat zou verspilling lijken, vergelijkbaar met het gelijktijdig verwarmen en koelen van een huis met open ramen. 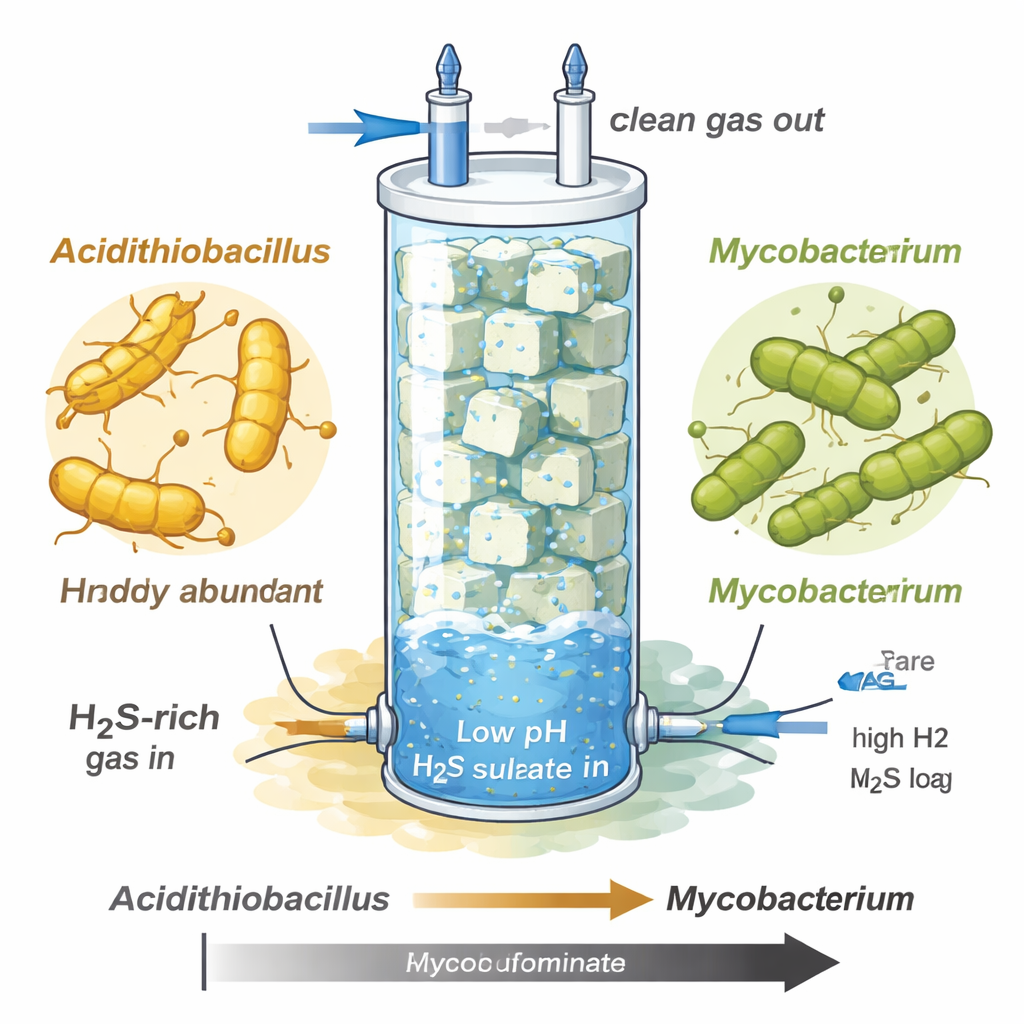
Een overlever in een extreem reactor
De onderzoekers bestudeerden een biotricklingfilter—een hoge glazen kolom gevuld met schuimblokjes—ontworpen om waterstofsulfide uit gasstromen te verwijderen, vergelijkbaar met ruwe biogas- of aardgasstromen. Toen ze de sulfidebelasting opvoerden en het systeem zeer zuur hielden (pH rond 1–1,5), veranderde de microbiële gemeenschap drastisch. Aanvankelijk gedijde een bekende sulfide-oxidizer, Acidithiobacillus, en zette veel van het sulfide om in sulfaat, maar deze soort stortte later in onder de extreme sulfidebelasting. In zijn plaats domineerde een eerder ongekarakteriseerde Mycobacterium-soort, aangeduid als MAG-M116, vrijwel de hele gemeenschap, ondanks dat hij in de vroege, mildere fase trager groeide.
Een microbe die de gebruikelijke regels doorbreekt
Genetische en eiwitniveauanalyse toonden aan dat MAG-M116 een ongebruikelijke metabole opzet heeft. Hij bezit een sleutelenzym, sulfide:quinon-oxidoreductase, dat sulfide slechts tot elementair zwavel oxideert, dat zich ophoopt als kleine vaste deeltjes. Tegelijk heeft de microbe een compleet genenset voor assimilatoire sulfaatreductie, de route die sulfaat de cel in trekt en reduceert om aminozuren zoals cysteïne en methionine te bouwen. Onder hoge sulfidecondities waren beide routes tegelijk actief. Sulfide-oxidatie pompte elektronen in de energiemachines van de cel, terwijl sulfaatreductie een deel van die elektronstroom opnam, waardoor de twee richtingen van de zwavelcyclus binnen één enkele cel met elkaar verbonden werden.
Van een “verspillende” cyclus naar een veiligheidsklep
Het gelijktijdig draaien van beide routes zou in theorie zinloos kunnen lijken—energie verbranden zonder nettowinst. Maar het team toont aan dat dit voor MAG-M116 fungeert als een veiligheidsklep voor overtollige elektronen. Het oxideren van grote hoeveelheden sulfide geeft een golf van elektronen in de respiratoire keten vrij, die kan lekken en reactieve zuurstofsoorten (ROS) kan genereren—schadelijke moleculen die DNA, eiwitten en membranen aantasten. Door actief sulfaat te reduceren tot aminozuren, kanaliseert de cel 10–14% van die elektronen naar constructief werk, waardoor de ophoping van een overgereduceerde, lekgevoelige toestand afneemt. Experimenten met en zonder sulfaat lieten zien dat actieve sulfaatreductie de ROS-productie met maximaal ongeveer 60% verminderde en de ophoping van gereduceerde cofactoren voorkwam die anders oxidatieve schade zouden aanjagen. 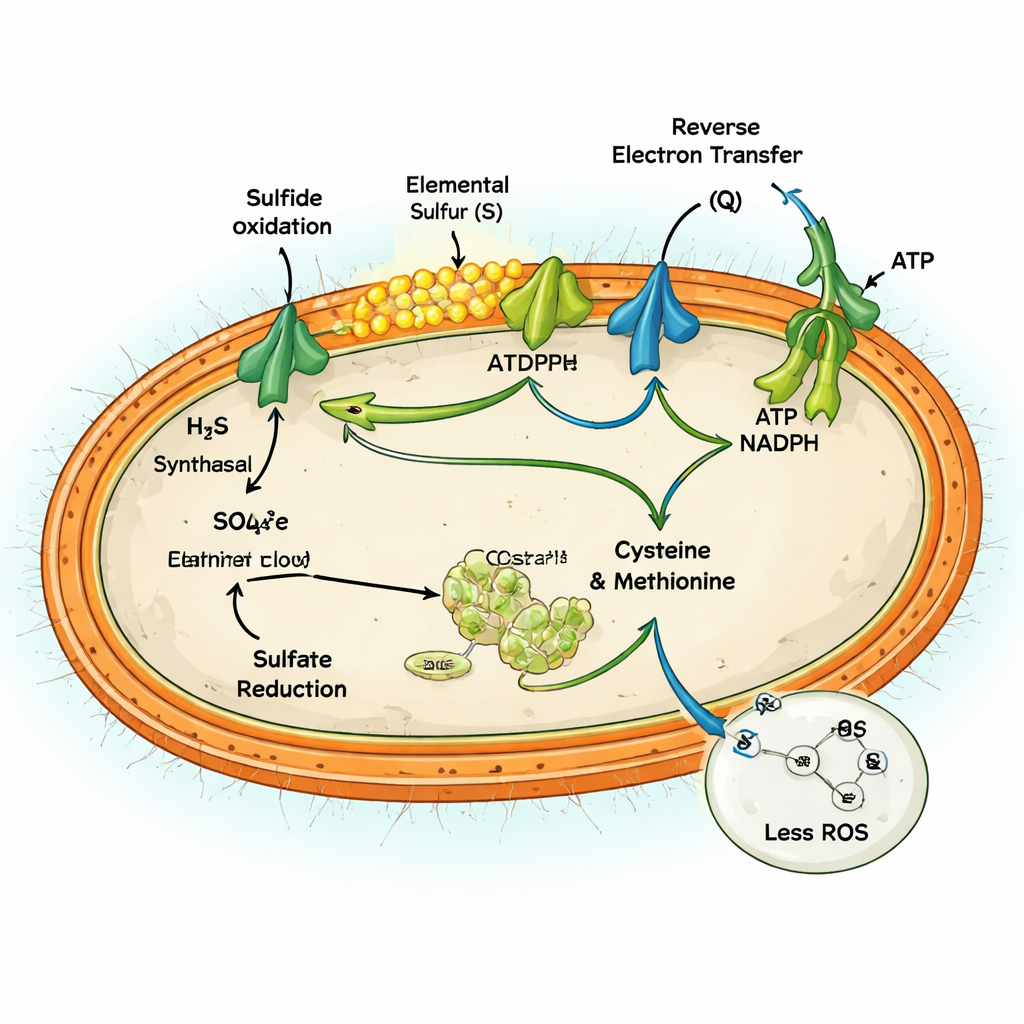
Van giftig gas naar bruikbare producten
In de latere fasen van reactorbedrijf, toen MAG-M116 dominant was, werd bijna alle binnenkomende waterstofsulfide omgezet in vast elementair zwavel, in plaats van in sulfaat. Tegelijk detecteerden de onderzoekers stijgende concentraties cysteïne en methionine in de vloeistoffase, wat erop wijst dat de microbe overtollige zwavelrijke aminozuren in zijn omgeving uitstootte. Deze combinatie—stabiliteit van elementair zwavel plus waardevolle organische zwavelverbindingen—maakt van wat eens een gevaarlijke verontreiniging was een mengsel van terugwinbare producten met toepassingen in landbouw, materialen en energiesystemen.
Wat dit betekent voor gezondheid en technologie
Voor niet-specialisten is de belangrijkste boodschap dat deze Mycobacterium een dubbele opgave heeft opgelost: hij kan hoge concentraties van een toxisch gas opruimen terwijl hij zijn eigen interne chemie in balans houdt. Dit doet hij door “push–pull”-zwavelreacties te voeren die normaal gescheiden zouden blijven, en door de ogenschijnlijk verspillende cyclus te gebruiken als ingebouwde schokdemper voor overtollige elektronen en schadelijke zuurstofradicalen. Deze ontdekking suggereert niet alleen nieuwe manieren om robuuste, laag-pH bioreactoren voor sulfide- en sulfaatverwijdering te ontwerpen, maar duidt ook erop dat verwante microben, waaronder ziekteverwekkende Mycobacterium-soorten, soortgelijke trucs kunnen gebruiken om oxidatieve aanvallen in het menselijk lichaam te overleven.
Bronvermelding: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Trefwoorden: zwavelcyclus, waterstofsulfide, Mycobacterium, redox-homeostase, biodesulfurisatie