Clear Sky Science · nl
Een kunstmatige cel die signaaltransductie mogelijk maakt via ADRB2 voor de regulatie van glycogenolyse
Kleine belletjes leren communiceren
Stel je een microscopische zeepbel voor die een hormoonachtig signaal buiten kan waarnemen en vervolgens "besluit" om opgeslagen brandstof vanbinnen te verbranden, net als een echte menselijke cel. Deze studie bouwt precies zo’n kunstmatige cel en laat zien hoe door mensen gemaakte celimitaties een chemische boodschap kunnen ontvangen en omzetten in gecontroleerde energiegerelateerde chemie. Dergelijk werk brengt ons dichter bij slimme medicijndragers, in het lab gemaakte weefsels en eenvoudige synthetische levensvormen die op hun omgeving kunnen reageren.
Een cel van buiten naar binnen opbouwen
Echte cellen luisteren voortdurend naar hun omgeving via receptoren in hun buitenmembraan. De auteurs wilden één van deze natuurlijke routes nabootsen met alleen gezuiverde componenten en eenvoudige vetbellen, zogenaamde gigantische vesikels. Ze concentreerden zich op een veelvoorkomende menselijke receptor, de β2-adrenerge receptor (ADRB2), die in ons lichaam hartslag, longfunctie en brandstofgebruik helpt regelen. Wanneer deze receptor een medicijn zoals isoproterenol (ISO) tegenkomt, zet dit normaal een interne keten van gebeurtenissen in gang die een boodschappermolecuul genaamd cAMP produceert, dat op zijn beurt regelt hoe cellen glycogeen afbreken, de opgeslagen vorm van glucose in het lichaam. Het reproduceren van deze hele volgorde in een kunstmatige cel was eerder niet bereikt.
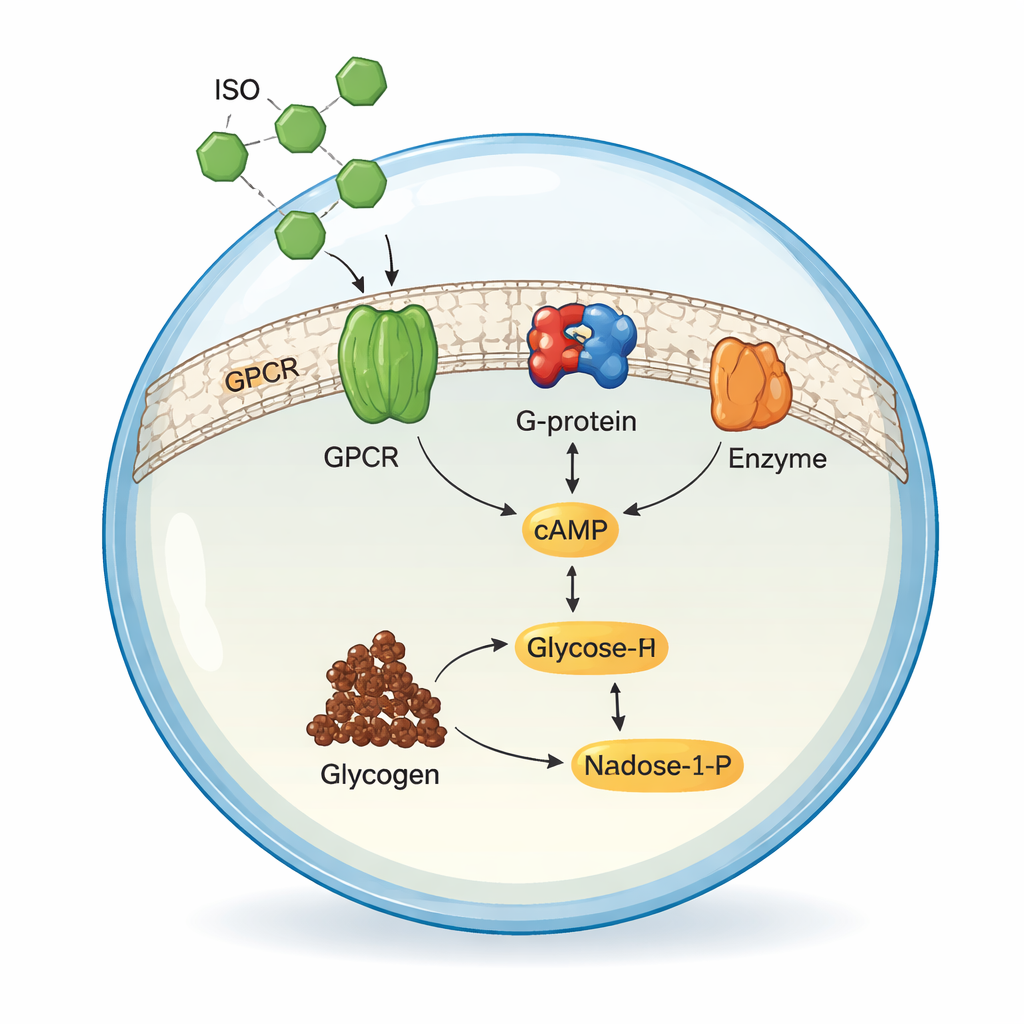
Het eerste signaalrelais namaken
Het team bouwde eerst de vroege stadia van de signaalroute na in oplossing, buiten elk membraan. Ze produceerden drie humane eiwitten in insectencellen: ADRB2, het bijbehorende G-proteïnesubunit (Gsα) en een enzym genaamd adenylate cyclase V (ADCY5), dat cAMP maakt uit ATP. Wanneer ze deze componenten onder zorgvuldig afgestemde condities met ISO mengden, leidde activering van de adrenerge receptor ertoe dat ADCY5 ATP in cAMP omzette. Door cAMP te meten met high-performance liquid chromatography optimaliseerden de onderzoekers pH, temperatuur en magnesiumgehalte en constateerden dat hun gereconstrueerde systeem even efficiënt werkte als, of beter dan, veel eerdere preparaten, wat bevestigt dat de kern van de signaalchemie aanwezig was.
Echte receptoren in kunstmatige membranen plaatsen
Vervolgens plaatsten de auteurs de drie eiwitten in de membranen van gigante unilamellaire vesikels—celgrote lipidebellen die dienen als chassis voor kunstmatige cellen. Ze tagden ADRB2 en ADCY5 fluorescerend om te verifiëren dat de eiwitten in het membraan zaten, vrij konden bewegen en in grote aantallen aanwezig waren, ongeveer 1,8 miljoen receptoren per vesikel. Enzymatische behandeling toonde aan dat meer dan 94% van deze receptoren de juiste kant op gericht was, met hun bindingsplaatsen naar de buitenkant toe. Een fluorescerende GTP-probe bevestigde dat ISO-binding aan het membraan echt G-proteïnen binnen de vesikels activeerde. Dit betekende dat de kunstmatige cellen in principe een extern ISO-signaal over hun membraan konden doorgeven, net zoals natuurlijke cellen doen.
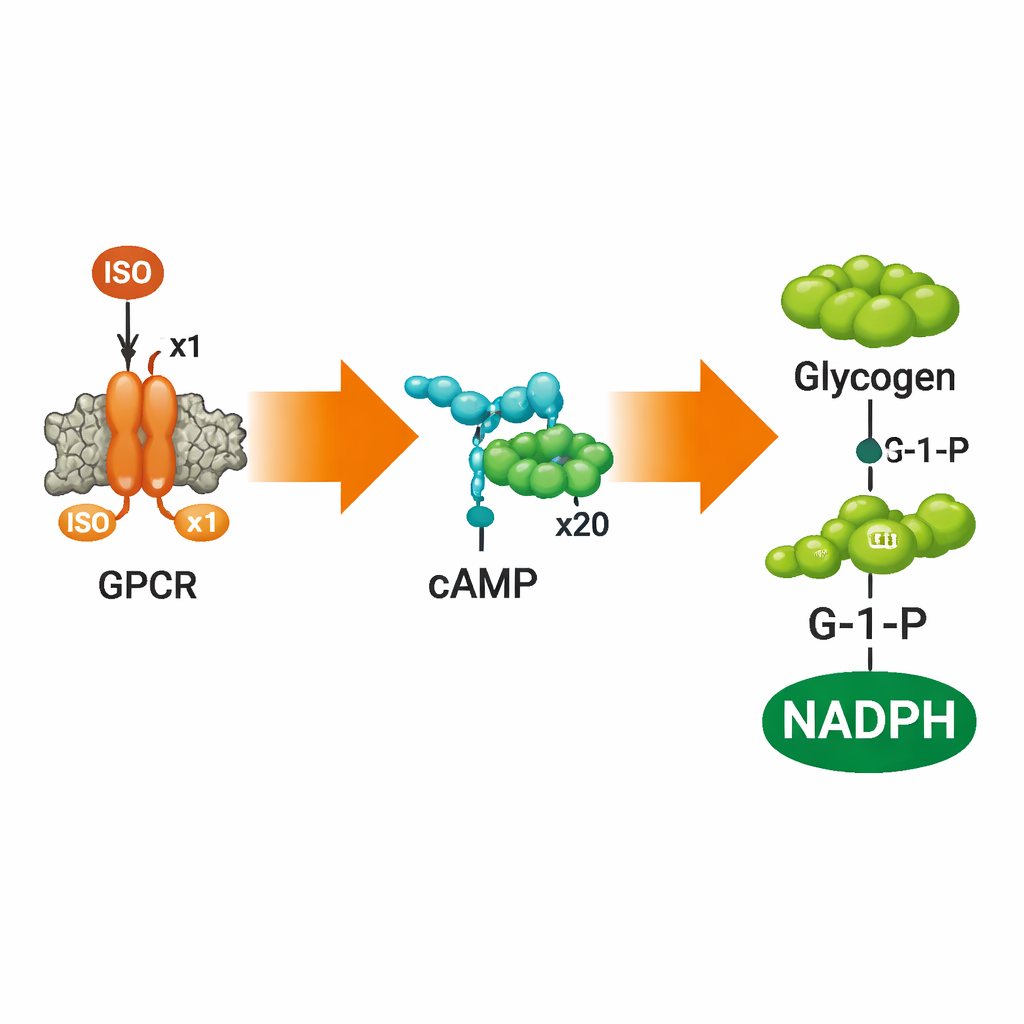
Signalen omzetten in brandstofafbraak
Om te onderzoeken of deze synthetische cellen iets nuttigs met het signaal konden doen, voegde het team een sensor voor cAMP toe en vervolgens een volledige glycogeen-afbreekroute binnen de vesikels. Met een FRET-gebaseerde cAMP-probe toonden ze aan dat het toevoegen van ISO buiten de vesikels leidde tot stijgende cAMP-niveaus binnen, afhankelijk van de dosis, en vervolgens een plateau bereikte toen de receptoren verzadigden—een klassieke eigenschap van natuurlijke G-eiwitgekoppelde receptoren. Middelen die ADRB2 blokkeren of stilleggen—alprenolol en carazolol—zetten deze respons precies zoals verwacht uit. Toen de auteurs ook vijf enzymen inkapselden die normaal glycogeen omzetten in glucose-1-fosfaat (G-1-P) en vervolgens in NADPH, leidde ISO-stimulatie tot meetbare productie van zowel G-1-P als NADPH binnen de kunstmatige cellen, gevolgd via massaspectrometrie, chromatografie en fluorescentie.
Een fluistering versterken tot een schreeuw
Een belangrijke bevinding is hoe sterk de interne respons werd versterkt. Een bescheiden hoeveelheid ISO buiten de vesikels produceerde ruwweg 22 keer meer cAMP-moleculen dan er ISO-moleculen waren, en deze versterking nam verder toe verderop in de route. Tegen de tijd dat het signaal glycogeenafbraak en omzetting naar 6‑fosfogluconolacton met bijbehorende NADPH had aangedreven, overschreed de totale versterking honderdvoud. Deze stapsgewijze versterking is een kenmerk van natuurlijke hormoonsignalering en laat zien dat het kunstmatige systeem meer doet dan alleen ISO detecteren—het verwerkt en versterkt de boodschap tot een robuuste metabole output.
Waarom dit ertoe doet voor toekomstige synthetische levensvormen
Voor niet‑specialisten valt de technische inhoud terug te brengen tot een eenvoudig idee: de onderzoekers hebben een minimale, door mensen gemaakte cel geleerd te luisteren en te reageren als een levende cel. Een buitenmolecuul dockt aan op een realistische menselijke receptor, een signaal wordt door een synthetisch membraan doorgegeven en een intern enzymnetwerk reageert door opgeslagen chemische energie vrij te maken. Het demonstreren van deze volledige keten—van receptoractivering tot gecontroleerd metabolisme—in een uitgekleed artificieel systeem is een belangrijke stap naar autonome synthetische cellen die kunnen waarnemen, beslissen en handelen op nuttige manieren, bijvoorbeeld door hun eigen energievoorziening aan te passen of therapieën alleen af te leveren wanneer ze de juiste chemische signalen detecteren.
Bronvermelding: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
Trefwoorden: kunstmatige cellen, signaaltransductie, GPCR, glycogenolyse, synthetische biologie