Clear Sky Science · nl
Het UFL1–AKT-cascade richten onderdrukt de progressie van triple-negatieve borstkanker
Waarom dit onderzoek ertoe doet
Triple-negatieve borstkanker (TNBC) is een van de dodelijkste vormen van borstkanker omdat het geen hormoon- of groeifactor-schakelaars bevat waarop veel moderne geneesmiddelen mikken. Patiënten krijgen vaak alleen traditionele chemotherapie, die haar werk kan verliezen naarmate tumoren resistent worden. Deze studie onthult een voorheen verborgen moleculair "motor" die TNBC-cellen helpt groeien en chemotherapie te weerstaan, en stelt een nieuw type geneesmiddel voor dat deze motor rechtstreeks blokkeert.
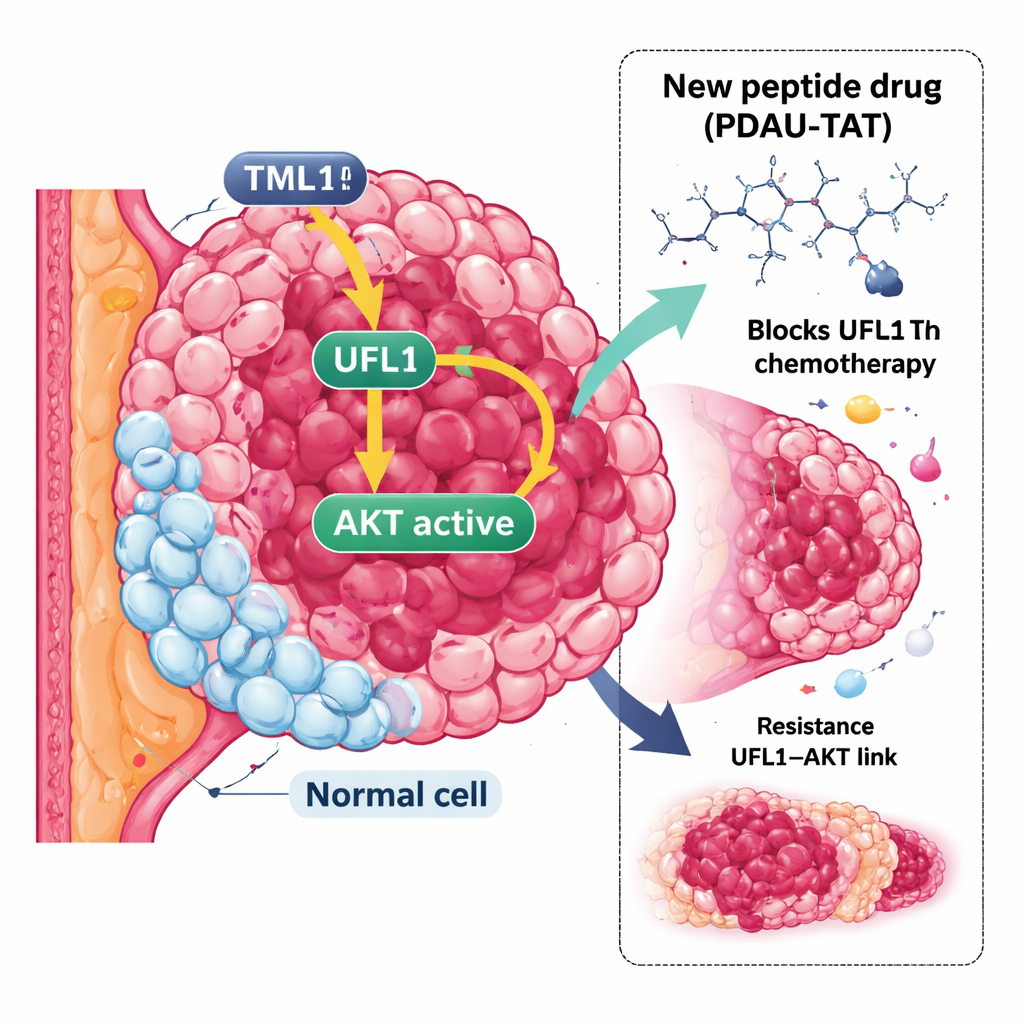
Een hardnekkige vorm van borstkanker
TNBC wordt gedefinieerd door het ontbreken van drie veelvoorkomende markers: de oestrogeenreceptor, de progesteronreceptor en de HER2-groeireceptor. Zonder deze markers zijn veel succesvolle gerichte therapieën simpelweg niet van toepassing. In plaats daarvan worden standaardmiddelen zoals cisplatine en doxorubicine gebruikt, maar TNBC-tumoren tonen vaak resistentie of passen zich snel aan deze behandelingen aan en hebben een grotere kans om uit te zaaien. Dit schept een urgente behoefte aan nieuwe strategieën die verder kijken dan de gebruikelijke verdachten en andere kwetsbaarheden in de controlemechanismen van de tumor opzoeken.
Een weinig bekend eiwit met grote impact
De onderzoekers richtten zich op UFL1, een eiwit dat een klein label, UFM1 genoemd, aan andere eiwitten vastmaakt in een proces dat bekendstaat als UFMylatie. Dit labelingsysteem is pas recent ontdekt en de rol ervan bij kanker was onduidelijk en soms zelfs tegenstrijdig. Door patiëntgegevens en tumormonsters te analyseren, toonde het team aan dat UFL1 duidelijk verhoogd is in TNBC vergeleken met normaal borstweefsel. Wanneer ze UFL1-niveaus verlaagden in TNBC-celijnen en in muismodellen met tumoren, vermenigvuldigden kankercellen zich langzamer en werden ze veel gevoeliger voor chemotherapie, wat suggereert dat UFL1 in deze context een tumorbevorderende rol speelt.
UFL1 koppelen aan een meester-schakelaar voor groei
Dieper gravend ontdekten de wetenschappers dat UFL1 direct bindt aan AKT, een centraal signaaleiwit dat celgroei, -overleving en -metabolisme aanstuurt en vaak hyperactief is in kankers. In TNBC is AKT vaak overactief, zelfs wanneer de gebruikelijke upstream-mutaties ontbreken. Het team ontdekte dat UFL1 AKT chemisch labelt op drie specifieke posities, waardoor het voor de activerende partners van AKT gemakkelijker wordt om het te activeren, terwijl het tegelijkertijd afgeschermd wordt van enzymen die het normaal zouden uitschakelen. Cellen zonder UFL1 of cellen die een geconstrueerde vorm van AKT tot expressie brachten die deze labels niet kan ontvangen, vertoonden veel lagere AKT-activiteit, tragere groei en grotere kwetsbaarheid voor chemotherapie in zowel celkweken als diermodellen.
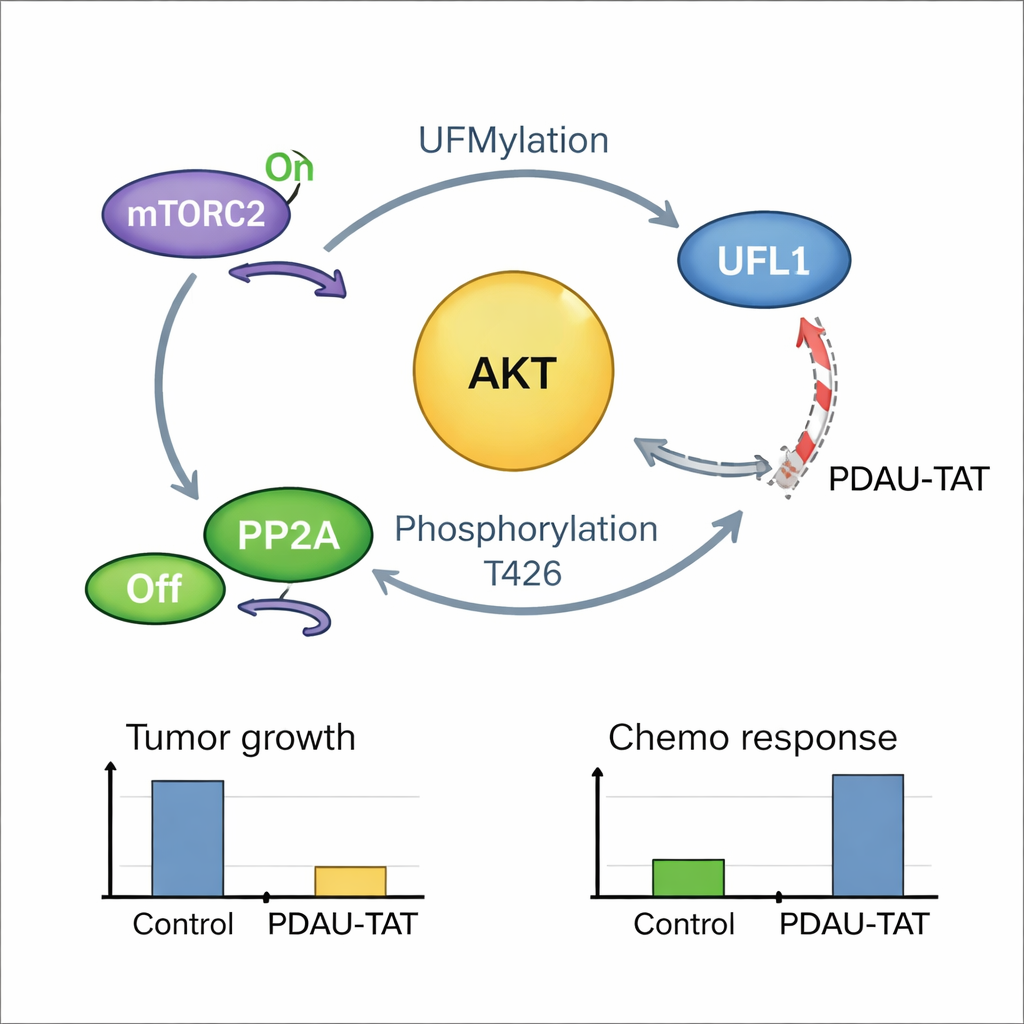
Een zichzelf versterkende kankerlus en een manier om die te doorbreken
Het verhaal bleek nog nauwer verbonden: zodra AKT geactiveerd is, geeft het terugkoppeling en modificeert het UFL1 op één cruciale plaats, waardoor UFL1’s labelingsactiviteit op AKT en andere doelwitten toeneemt. Dit creëert een positieve feedbacklus waarin UFL1 AKT activeert en actief AKT op zijn beurt UFL1 extra aanjaagt. Patiëntentumor-monsters lieten zien dat hoge niveaus van gemodificeerd UFL1 sterk correleren met hoge niveaus van actief AKT, wat het bestaan van deze lus bij mensen ondersteunt. Om deze kwetsbaarheid te benutten, ontwierp het team een kort, celpenetreerbaar peptide, PDAU-TAT genoemd, dat een klein gebied van UFL1 imiteert en zich tussen UFL1 en AKT klemzet. Dit peptide verstoort hun interactie, vermindert AKT-activatie, vertraagt tumorgroei en maakt TNBC-cellen en patiënt-afgeleide tumoren gevoeliger voor chemotherapie, zonder duidelijke schade aan belangrijke organen bij muizen.
Wat dit voor patiënten zou kunnen betekenen
In eenvoudige bewoordingen hebben de onderzoekers een verborgen bekabelingsschema binnen TNBC-cellen blootgelegd: UFL1 en AKT zitten vast in een zichzelf versterkende lus die groeisignalen in de "aan"-stand houdt en tumoren helpt behandelingen te weerstaan. Door een klein peptide te ontwikkelen dat in deze lus glipt en UFL1 van AKT loskoppelt, laten ze een plausibele nieuwe manier zien om TNBC-tumoren te verzwakken terwijl normale cellen, die doorgaans lagere UFL1-niveaus hebben, worden gespaard. Hoewel dit werk nog in de preklinische fase verkeert, wijst het op een nieuwe klasse gerichte therapieën die niet mikken op de gebruikelijke receptoren maar op de eiwit–eiwitverbindingen die sommige van de meest agressieve vormen van borstkanker aandrijven.
Bronvermelding: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Trefwoorden: triple-negatieve borstkanker, AKT-signaalwegen, UFMylatie, UFL1, peptide-kankertherapie